Clear Sky Science · pl
Składany HaloTag o wysokim powinowactwie do znakowania białek w żywych komórkach
Widzenie ukrytych mechanizmów wewnątrz żywych komórek
Współczesna biologia opiera się na możliwości obserwowania pojedynczych białek działających we wnętrzu żywych komórek, lecz dołączenie jasnych molekularnych „latarenek” do tych białek bez zakłócania ich funkcji jest zaskakująco trudne. W tym badaniu przedstawiono nowy system znakowania, który umieszcza malutki znacznik w białku, a następnie „zapalaja˛” go przy pomocy silnych barwników chemicznych, pozwalając badaczom śledzić nawet rzadkie, wrażliwe cele w czasie rzeczywistym za pomocą najnowocześniejszych mikroskopów.
Mały znacznik spotyka potężne światło
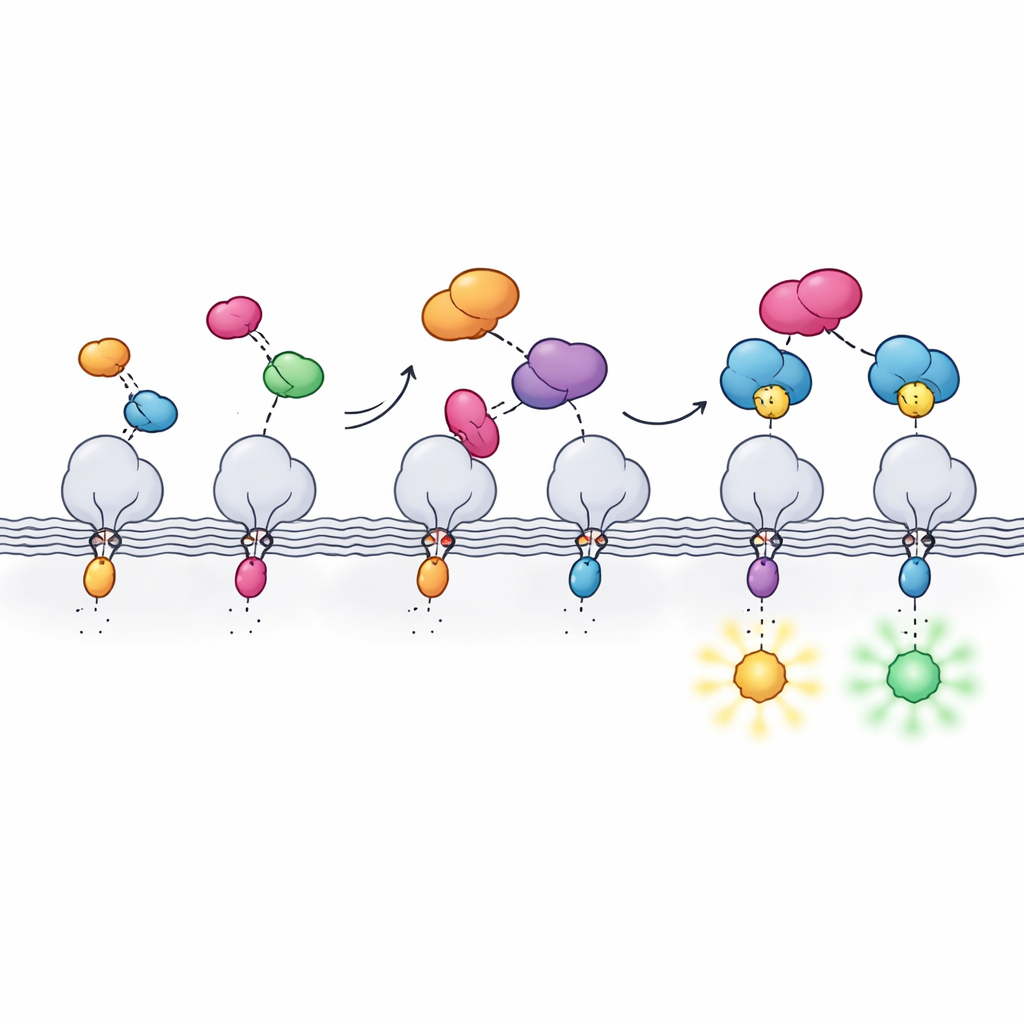
Praca opiera się na HaloTag, powszechnie stosowanym znaczniku białek, który tworzy trwałe wiązanie ze specjalnymi barwnikami fluorescencyjnymi. HaloTag jest jasny i wszechstronny, ale jednocześnie masywny, co może zaburzać normalne zachowanie białka, z którym jest związany. Autorzy rozwiązują ten problem, dzieląc HaloTag na dwie części: bardzo mały peptyd nazwany Hpep, mający tylko 14 reszt, oraz większy partnerowy białkowy fragment zwany cpHaloΔ3. Mały Hpep można włączyć bezpośrednio do białka docelowego, podczas gdy cpHaloΔ3 dostarcza się oddzielnie. Kiedy spotykają się wewnątrz komórki, dwie części ściśle się łączą z bardzo wysokim powinowactwem i odtwarzają aktywny HaloTag zdolny do wychwytywania jasnych barwników.
Projektowanie składanego włącznika światła
Aby uczynić ten system praktycznym, zespół musiał jednocześnie wyważyć kilka właściwości. Hpep i cpHaloΔ3 musiały rozpoznawać się ekstremalnie mocno, tak by nawet pojedyncza kopia na białku o niskiej obfitości została znakowana, lecz cpHaloΔ3 sam w sobie powinien pozostawać niemal nieaktywny, by uniknąć niepożądanego tła fluorescencyjnego. Wykorzystując prezentację na drożdżach i sortowanie komórek o wysokiej przepustowości, badacze przesiewali biblioteki nieznacznie zmodyfikowanych fragmentów cpHalo w poszukiwaniu wariantów, które były ciche w pojedynkę, lecz szybkie i wydajne po związaniu z Hpep. Końcowa wersja, cpHaloΔ3, łączyła powinowactwo w nanomolowym zakresie, niskie niezamierzone znakowanie oraz szybkie reagowanie z barwnikami po złączeniu obu części. Warianty Hpep również zostały dostrojone tak, że po związaniu subtelnie zmieniały zachowanie przymocowanych barwników, wpływając zarówno na jasność, jak i na czas życia fluorescencji.
Oświetlanie rzeczywistych struktur komórkowych
Następnie badacze pokazali, że ich składany HaloTag działa w szerokim spektrum ustawień komórkowych. Przyłączyli Hpep do białek oznaczających jądro komórkowe, powierzchnię mitochondriów i otoczkę jądrową oraz wspólnie ekspresowali cpHaloΔ3 w komórkach ludzkich. Po dodaniu przenikających do komórki barwników HaloTag, zrekonstruowany znacznik dał ostre obrazy oczekiwanych struktur z bardzo małym tłem pochodzącym od niepowiązanego cpHaloΔ3. Kluczowe znaczenie miało to, że Hpep jest tak mały, iż można go było wstawić bezpośrednio do własnych genów komórki za pomocą CRISPR bez konieczności klonowania dużych konstrukcji DNA. Zespół zademonstrował bezproblemowe „knock-iny” dla wielu różnych białek endogennych, od komponentów strukturalnych jak wimentyna, po kanały błonowe i klatrinę, oraz pokazał, że można je wzbogacać i analizować za pomocą cytometrii przepływowej i mikroskopii.
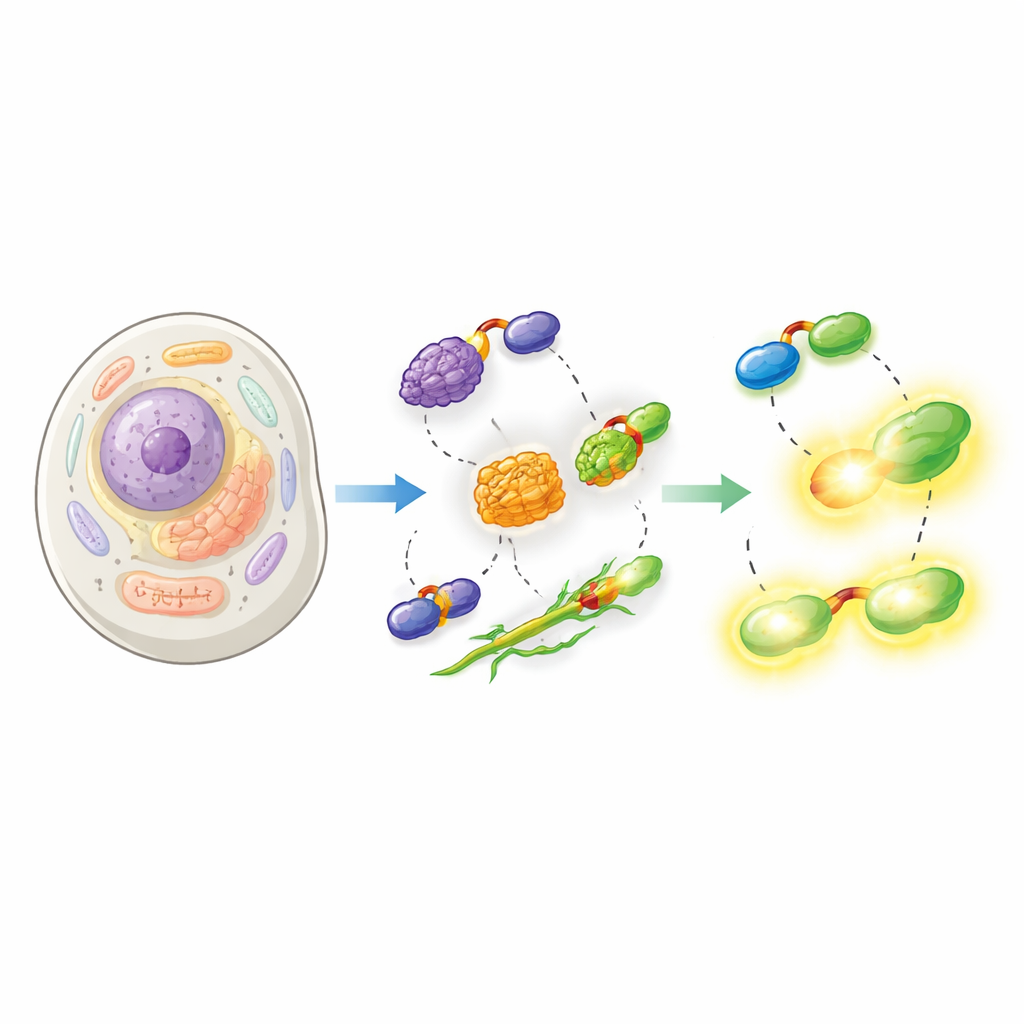
Przepychanie granic nowoczesnej mikroskopii
Poza standardową mikroskopią fluorescencyjną, nowy znacznik testowano w niektórych z najbardziej wymagających technik optycznych. Przy użyciu specjalnych barwników zgodnych z mikroskopią superrozdzielczą i metodami wygaszania, autorzy rozdzielili błony mitochondrialne i mikrotubule z detalami znacznie poniżej konwencjonalnego limitu dyfrakcji, w niektórych przypadkach w komórkach żywych. Połączyli też system z mikroskopią ekspansyjną, fizycznie powiększając zakonserwowane komórki, aby ujawnić drobne struktury, oraz z obrazowaniem czasu życia fluorescencji. Różne warianty Hpep zmieniały czas pozostawania barwnika w stanie wzbudzonym, co pozwalało rozróżnić dwa białka znakowane tym samym kolorem wyłącznie na podstawie ich czasów życia i umożliwiało obrazowanie wieloparametrowe z użyciem jednego partnera cpHaloΔ3.
Dlaczego ten nowy znacznik ma znaczenie
Te osiągnięcia razem tworzą zwarte, elastyczne narzędzie do znakowania, które łączy genetyczną wygodę malutkich peptydowych znaczników z optyczną siłą syntetycznych barwników. Mały rozmiar Hpep ułatwia jego wstawianie do genów endogennych i zmniejsza prawdopodobieństwo zakłócenia funkcji białka, podczas gdy cpHaloΔ3 dostarcza jasne, stabilne kolory wtedy i tam, gdzie są potrzebne. W efekcie powstaje sposób obserwacji białek w żywych komórkach o wysokim kontraście i niskim tle, kompatybilny z zaawansowanymi mikroskopami i eksperymentami wielocelowymi. Zestaw narzędzi split-HaloTag powinien pomóc badaczom w mapowaniu organizacji komponentów komórkowych i ich zmian w czasie w zdrowiu i chorobie.
Cytowanie: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Słowa kluczowe: znakowanie białek, mikroskopia żywych komórek, HaloTag, etykietowanie CRISPR, mikroskopia superrozdzielcza