Clear Sky Science · nl
Een high-affinity split-HaloTag voor eiwitlabeling in levende cellen
Het verborgen mechanisme in levende cellen zichtbaar maken
Moderne biologie hangt af van het kunnen volgen van individuele eiwitten in levende cellen, maar heldere moleculaire “zaklampen” aan die eiwitten koppelen zonder ze te verstoren blijkt verrassend lastig. Deze studie introduceert een nieuw labelingssysteem dat een klein merkteken in een eiwit plaatst en dat vervolgens met krachtige chemische kleurstoffen inschakelt, waardoor onderzoekers zelfs zeldzame, kwetsbare doelen in realtime met geavanceerde microscopen kunnen volgen.
Een klein merkteken ontmoet een krachtig licht
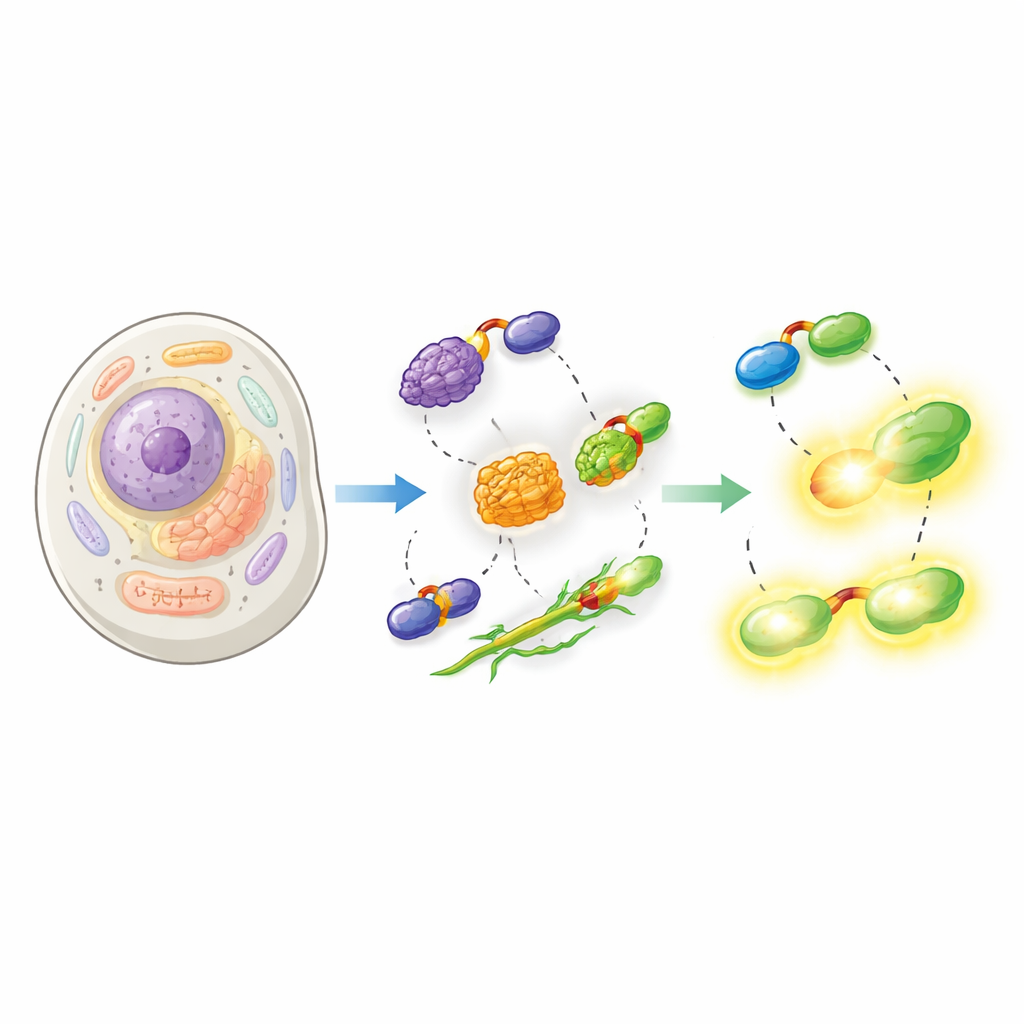
Het werk bouwt voort op HaloTag, een veelgebruikt eiwitlabel dat een permanente binding vormt met speciale fluorescerende kleurstoffen. HaloTag is helder en veelzijdig, maar ook omvangrijk, wat het normale gedrag van het gefuseerde eiwit kan verstoren. De auteurs lossen dit op door HaloTag in twee delen te splitsen: een zeer klein peptide genaamd Hpep, slechts 14 bouwstenen lang, en een groter partner-eiwit genaamd cpHaloΔ3. Het kleine Hpep kan direct in het doel-eiwit worden ingebouwd, terwijl cpHaloΔ3 apart wordt geleverd. Wanneer ze elkaar in de cel ontmoeten, klikken de twee delen met zeer hoge affiniteit in elkaar en vormen ze een actief HaloTag dat heldere kleurstoffen kan binden.
Het ontwerpen van een klik-schakelaar voor licht
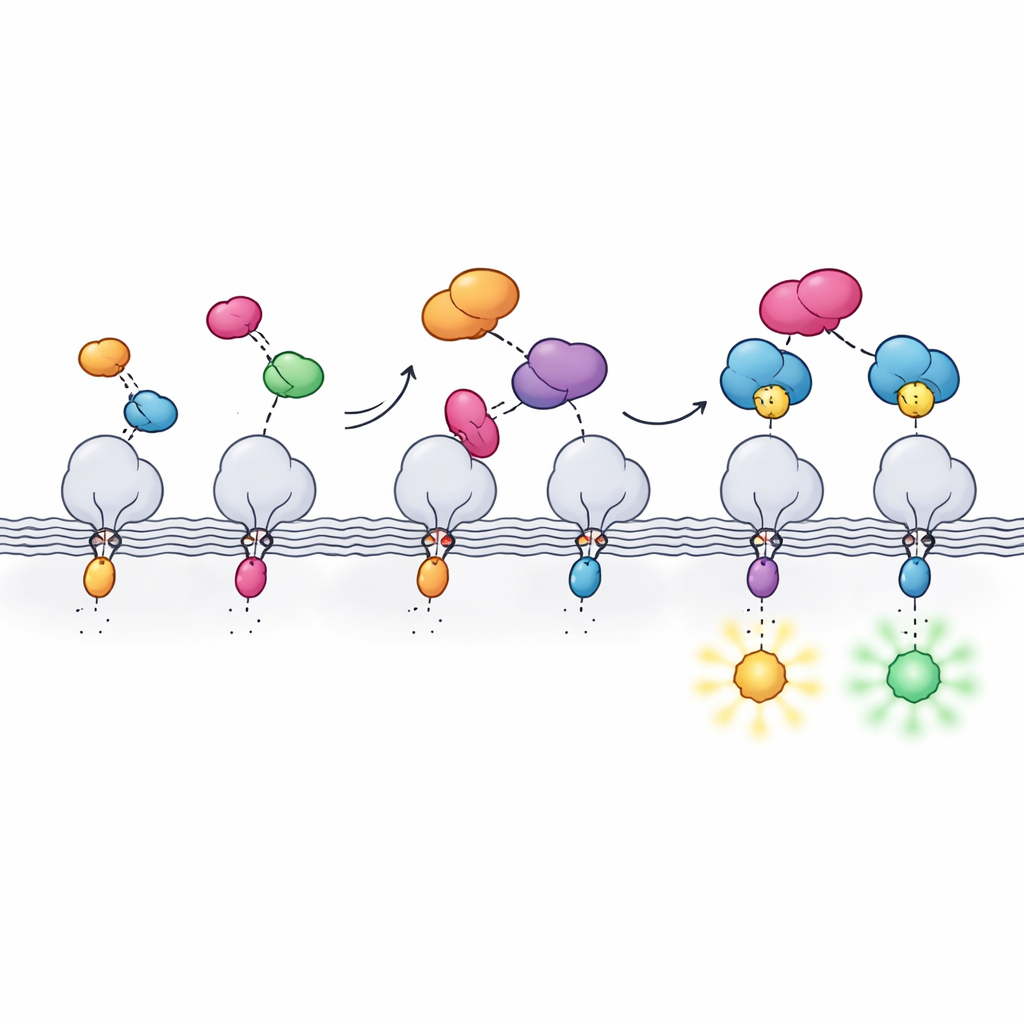
Om dit split-systeem praktisch te maken, moest het team meerdere eigenschappen tegelijk afwegen. Hpep en cpHaloΔ3 moesten elkaar extreem goed herkennen zodat zelfs een enkel exemplaar op een eiwit met lage abundanties gelabeld zou worden, maar cpHaloΔ3 op zichzelf moest vrijwel inactief blijven om ongewenste achtergrondgloed te vermijden. Met behulp van gistdisplay en hoogdoorvoersortering van cellen screeneden ze bibliotheken met licht gewijzigde cpHalo-fragmenten op varianten die stil waren in isolatie maar snel en efficiënt actief werden zodra ze aan Hpep gebonden waren. De uiteindelijke versie, cpHaloΔ3, combineerde nanomolaire bindingssterkte, lage onbedoelde labeling en een snelle reactie met kleurstoffen zodra de twee delen weer verenigd waren. Varianten van Hpep werden ook afgestemd zodat ze, eenmaal gebonden, subtiel het gedrag van gebonden kleurstoffen veranderden en zowel helderheid als fluorescentieduur beïnvloedden.
Cellulaire structuren echt laten oplichten
De onderzoekers toonden vervolgens aan dat hun split-HaloTag werkt in een breed scala aan cellulaire contexten. Ze plaatsten Hpep op eiwitten die de kern, het mitochondriale oppervlak en de kernmembraan markeren, en co-exprimeerden cpHaloΔ3 in menselijke cellen. Na toevoeging van celdoorlaatbare HaloTag-kleurstoffen produceerde het gereconstrueerde label scherpe beelden van de verwachte structuren met zeer weinig achtergrond van niet-gebonden cpHaloΔ3. Cruciaal is dat Hpep zo klein is dat het direct in de eigen genen van de cel kon worden ingevoegd met CRISPR zonder grote DNA-constructen te hoeven kloneren. Het team liet naadloze “knock-ins” zien voor veel verschillende endogene eiwitten, van structurele componenten zoals vimentine tot membranaire kanalen en clathrine, en toonde aan dat deze konden worden verrijkt en geanalyseerd met flowcytometrie en microscopie.
De grenzen van moderne microscopie verleggen
Naast standaard fluorescentiebeeldvorming werd het nieuwe label getest met enkele van de veeleisendste optische technieken. Met speciale kleurstoffen die compatibel zijn met superresolutie- en depletion-microscopie resolveerden de auteurs mitochondriale membranen en microtubuli met details ver onder de conventionele diffractielimiet, in sommige gevallen in levende cellen. Ze combineerden het systeem ook met expansion-microscopie, waarbij geconserveerde cellen fysiek worden opgezwollen om fijne structuren te onthullen, en met fluorescentieduurbeeldvorming. Verschillende Hpep-varianten veranderden hoe lang de kleurstof in de geëxciteerde toestand bleef, waardoor twee eiwitten die met dezelfde kleur waren gelabeld puur op hun levensduur te onderscheiden waren en multiplexbeeldvorming met een enkele cpHaloΔ3-partner mogelijk werd.
Waarom dit nieuwe label ertoe doet
Gezamenlijk creëren deze verbeteringen een compact, flexibel labelingssysteem dat het genetische gemak van kleine peptide-tags combineert met de optische kracht van synthetische kleurstoffen. De kleine omvang van Hpep maakt het eenvoudig in te voegen in endogene genen en minder waarschijnlijk om eiwitfunctie te verstoren, terwijl cpHaloΔ3 heldere, stabiele kleuren levert wanneer en waar ze nodig zijn. Het resultaat is een hoogcontrast- en laag-achtergrondmethode om eiwitten in levende cellen te observeren, compatibel met geavanceerde microscopen en experimenten met meerdere doelen. Deze split-HaloTag-toolkit zou onderzoekers moeten helpen in kaart te brengen hoe cellulaire componenten georganiseerd zijn en hoe ze in de loop van de tijd veranderen bij gezondheid en ziekte.
Bronvermelding: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Trefwoorden: eiwitlabeling, beeldvorming in levende cellen, HaloTag, CRISPR-tagging, superresolutiemicroscopie