Clear Sky Science · pt
Um split-HaloTag de alta afinidade para marcação de proteínas em células vivas
Vendo a maquinaria oculta dentro de células vivas
A biologia moderna depende da capacidade de observar proteínas individuais em ação dentro de células vivas, mas anexar “lanternas” moleculares brilhantes a essas proteínas sem perturbá-las é surpreendentemente difícil. Este estudo introduz um novo sistema de marcação que insere uma pequena etiqueta numa proteína e a ilumina com corantes químicos potentes, permitindo aos pesquisadores acompanhar alvos escassos e frágeis em tempo real com microscópios de ponta.
Uma etiqueta minúscula encontra uma luz poderosa
O trabalho baseia-se no HaloTag, um rótulo proteico amplamente usado que forma uma ligação permanente a corantes fluorescentes especiais. O HaloTag é brilhante e versátil, mas também volumoso, o que pode interferir no comportamento normal da proteína à qual é fundido. Os autores resolvem isso dividindo o HaloTag em duas partes: um peptídeo muito pequeno chamado Hpep, com apenas 14 blocos de construção, e uma proteína parceira maior chamada cpHaloΔ3. O pequeno Hpep pode ser inserido diretamente na proteína de interesse, enquanto o cpHaloΔ3 é fornecido separadamente. Quando se encontram dentro da célula, as duas partes se unem com afinidade muito alta e recriam um HaloTag ativo capaz de capturar corantes brilhantes.
Projetando um interruptor de luz que se encaixa
Para tornar esse sistema dividido prático, a equipe teve que equilibrar várias propriedades ao mesmo tempo. Hpep e cpHaloΔ3 precisavam se reconhecer com extrema afinidade para que até uma única cópia em uma proteína de baixa abundância fosse marcada, mas o cpHaloΔ3 por si só deveria permanecer quase inativo para evitar brilho indesejado de fundo. Usando exibição em levedura e triagem celular de alto rendimento, eles selecionaram bibliotecas de fragmentos cpHalo ligeiramente alterados em busca de variantes que fossem silenciosas sozinhas, mas rápidas e eficientes quando ligadas ao Hpep. A versão final, cpHaloΔ3, combinou afinidade na faixa de nanomolar, baixa marcação não intencional e reação rápida com corantes uma vez que as duas peças se reuniam. Variantes de Hpep também foram ajustadas para que, quando ligadas, alterassem sutilmente o comportamento dos corantes anexados, modificando tanto o brilho quanto o tempo de vida da fluorescência.
Iluminando estruturas celulares reais
Os pesquisadores então demonstraram que seu split-HaloTag funciona em uma ampla variedade de contextos celulares. Eles anexaram Hpep a proteínas que marcam o núcleo, a superfície mitocondrial e o envelope nuclear, e co-expressaram cpHaloΔ3 em células humanas. Após adicionar corantes HaloTag permeáveis à célula, a etiqueta reconstituída produziu imagens nítidas das estruturas esperadas com muito pouco fundo proveniente do cpHaloΔ3 não ligado. Crucialmente, porque Hpep é tão pequeno, ele pôde ser inserido diretamente nos próprios genes da célula usando CRISPR sem necessidade de clonar grandes construtos de DNA. A equipe demonstrou ‘knock-ins’ perfeitos para muitas proteínas endógenas diferentes, desde componentes estruturais como vimentina até canais de membrana e clatrina, e mostrou que essas populações podiam ser enriquecidas e analisadas por citometria de fluxo e microscopia.
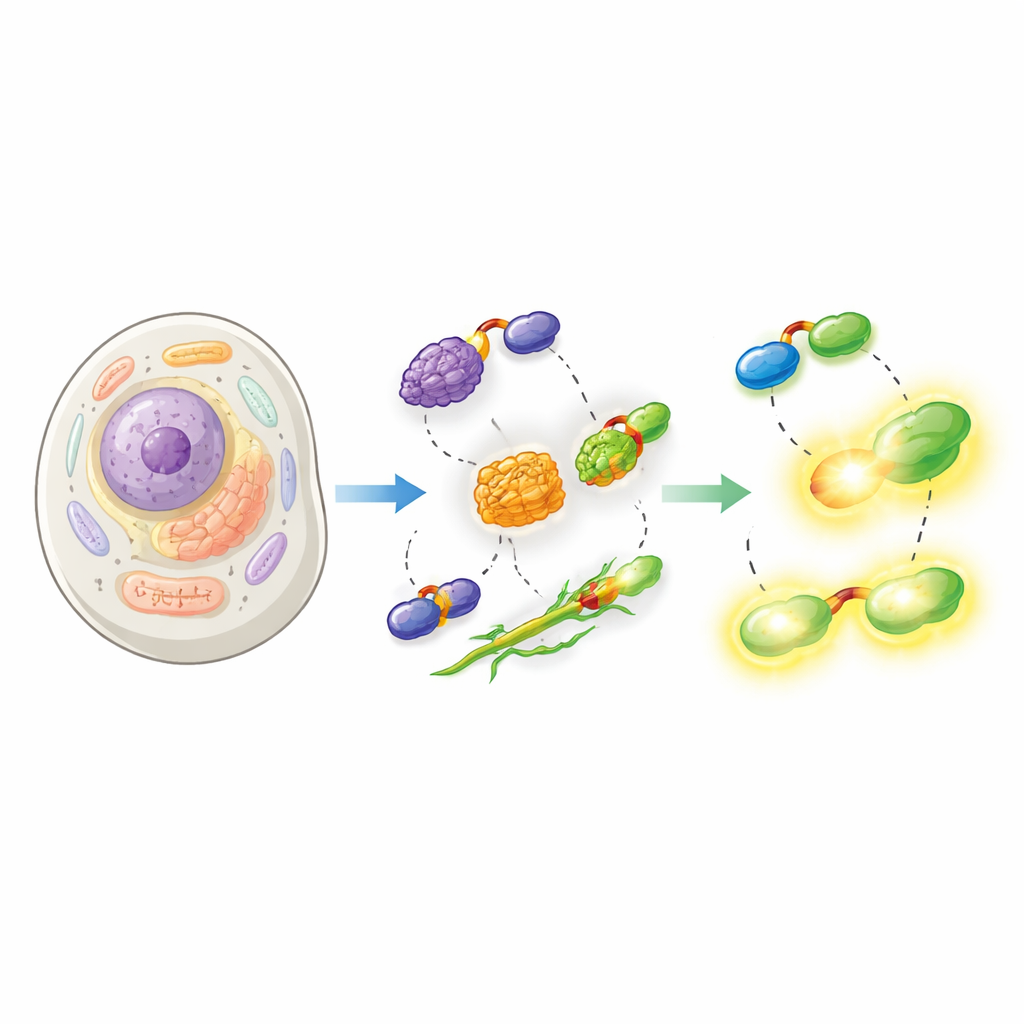
Levando ao limite a microscopia moderna
Além da imagem de fluorescência padrão, a nova etiqueta foi testada com algumas das técnicas ópticas mais exigentes. Usando corantes especiais compatíveis com super-resolução e microscopia de depleção, os autores resolveram membranas mitocondriais e microtúbulos com detalhes bem abaixo do limite de difração convencional, em alguns casos em células vivas. Eles também combinaram o sistema com microscopia de expansão, inchando fisicamente células preservadas para revelar estruturas finas, e com imageamento por tempo de vida de fluorescência. Diferentes variantes de Hpep alteraram quanto tempo o corante permanecia em seu estado excitado, permitindo distinguir duas proteínas marcadas com a mesma cor puramente por seus tempos de vida e possibilitando imageamento multiplexado com um único parceiro cpHaloΔ3.
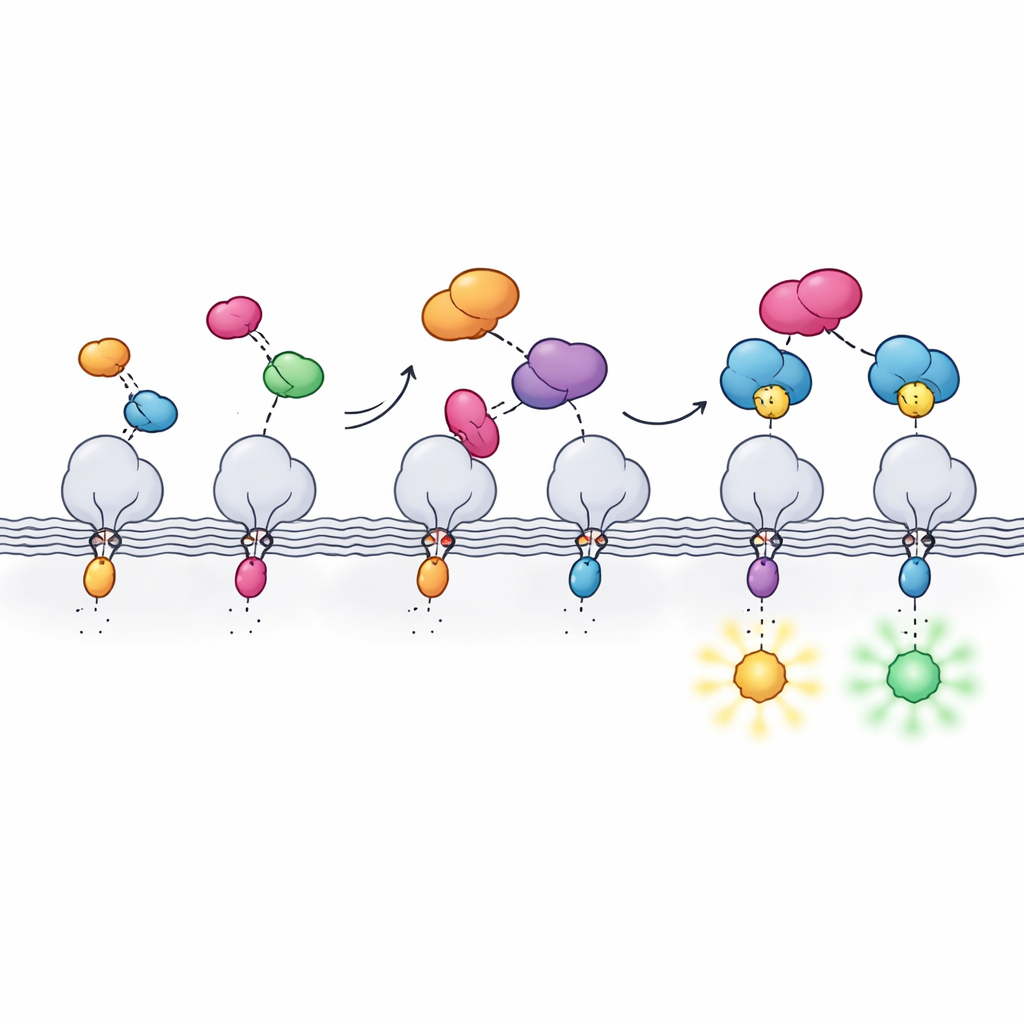
Por que essa nova etiqueta é importante
Juntas, essas melhorias criam um sistema de marcação compacto e flexível que combina a conveniência genética de etiquetas peptídicas minúsculas com o poder óptico de corantes sintéticos. O tamanho reduzido do Hpep facilita sua inserção em genes nativos e diminui a probabilidade de perturbar a função proteica, enquanto o cpHaloΔ3 fornece cores brilhantes e estáveis quando e onde são necessárias. O resultado é uma maneira de alto contraste e baixo ruído de observar proteínas dentro de células vivas, compatível com microscópios avançados e experimentos com múltiplos alvos. Esse kit split-HaloTag deve ajudar pesquisadores a mapear como os componentes celulares são organizados e como mudam ao longo do tempo em saúde e doença.
Citação: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Palavras-chave: marcação de proteínas, imagem em células vivas, HaloTag, marcação por CRISPR, microscopia de super-resolução