Clear Sky Science · de
Ein hochaffiner geteilte-HaloTag für die Proteinmarkierung in lebenden Zellen
Das verborgene Innenleben lebender Zellen sehen
Die moderne Biologie ist darauf angewiesen, einzelne Proteine bei der Arbeit in lebenden Zellen beobachten zu können. Es ist jedoch überraschend schwierig, diesen Proteinen helle molekulare „Taschenlampen“ anzubringen, ohne sie zu stören. Diese Studie stellt ein neues Markierungssystem vor, das ein winziges Tag in ein Protein einbettet und es anschließend mit leistungsfähigen chemischen Farbstoffen zum Leuchten bringt. So können Forschende selbst seltene, empfindliche Zielproteine in Echtzeit mit hochmodernen Mikroskopen verfolgen.
Ein winziges Tag trifft auf ein starkes Licht
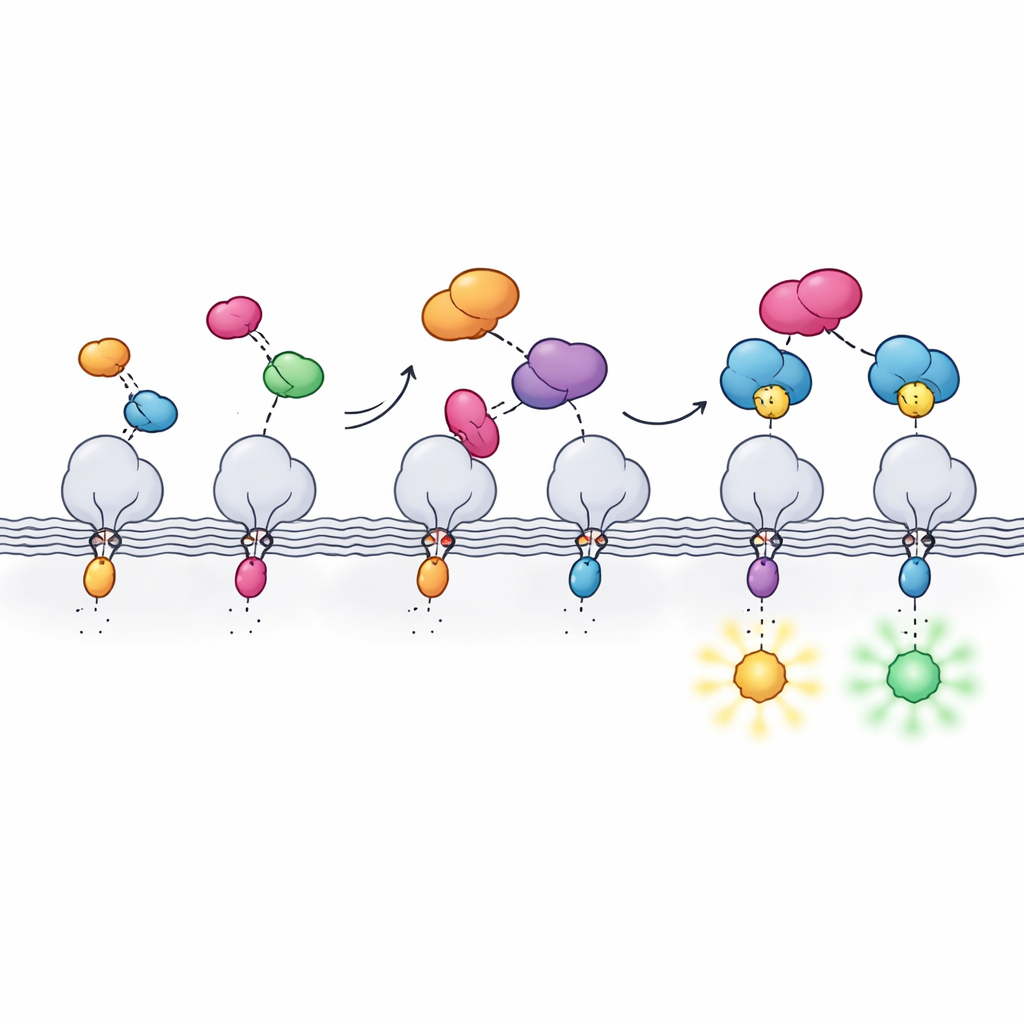
Die Arbeit baut auf HaloTag auf, einem weitverbreiteten Proteinlabel, das eine permanente Bindung zu speziellen fluoreszierenden Farbstoffen eingeht. HaloTag ist hell und vielseitig, aber auch sperrig, was das normale Verhalten des fusionierten Proteins stören kann. Die Autoren lösen dieses Problem, indem sie HaloTag in zwei Teile aufspalten: ein sehr kleines Peptid namens Hpep, nur 14 Aminosäuren lang, und ein größeres Partnerprotein namens cpHaloΔ3. Das kleine Hpep kann direkt in das Zielprotein eingebaut werden, während cpHaloΔ3 separat bereitgestellt wird. Treffen die beiden Teile in der Zelle aufeinander, schnappen sie mit sehr hoher Affinität zusammen und rekonstituieren einen aktiven HaloTag, der helle Farbstoffe binden kann.
Design eines zusammenklickenden Lichtschalters
Um dieses geteilte System praktisch nutzbar zu machen, musste das Team mehrere Eigenschaften gleichzeitig austarieren. Hpep und cpHaloΔ3 mussten sich extrem zuverlässig erkennen, sodass selbst eine einzelne Kopie an einem wenig abundanten Protein markiert würde, gleichzeitig sollte cpHaloΔ3 isoliert nahezu inaktiv bleiben, um unerwünschtes Hintergrundleuchten zu vermeiden. Mithilfe von Hefe‑Display und Hochdurchsatz‑Zellsortierung screente man Bibliotheken leicht veränderter cpHalo‑Fragmente nach Varianten, die allein ruhig sind, aber schnell und effizient arbeiten, sobald sie an Hpep binden. Die finale Version, cpHaloΔ3, vereinte nanomolare Bindungsstärke, geringe unerwünschte Markierung und schnelle Reaktion mit Farbstoffen nach Wiedervereinigung der beiden Teile. Auch Hpep‑Varianten wurden so abgestimmt, dass sie nach Bindung das Verhalten angehängter Farbstoffe subtil änderten und sowohl Helligkeit als auch Fluoreszenzlebensdauer beeinflussten.
Reale zelluläre Strukturen zum Leuchten bringen
Die Forschenden zeigten anschließend, dass ihr geteiltes HaloTag in einer Vielzahl zellulärer Kontexte funktioniert. Sie hängten Hpep an Proteine, die den Zellkern, die mitochondriale Oberfläche und die Kernhülle markieren, und coexprimierten cpHaloΔ3 in menschlichen Zellen. Nach Zugabe zellgängiger HaloTag‑Farbstoffe ergab das rekonstituierte Tag scharfe Bilder der erwarteten Strukturen mit sehr geringem Hintergrund durch ungebundenes cpHaloΔ3. Entscheidend ist, dass sich Hpep wegen seiner geringen Größe direkt in die körpereigenen Gene mittels CRISPR integrieren ließ, ohne große DNA‑Konstrukte klonen zu müssen. Das Team demonstrierte nahtlose Knock‑ins für viele endogene Proteine, von Strukturkomponenten wie Vimentin bis zu Membrankanälen und Clathrin, und zeigte, dass diese mittels Durchflusszytometrie und Mikroskopie angereichert und analysiert werden konnten.
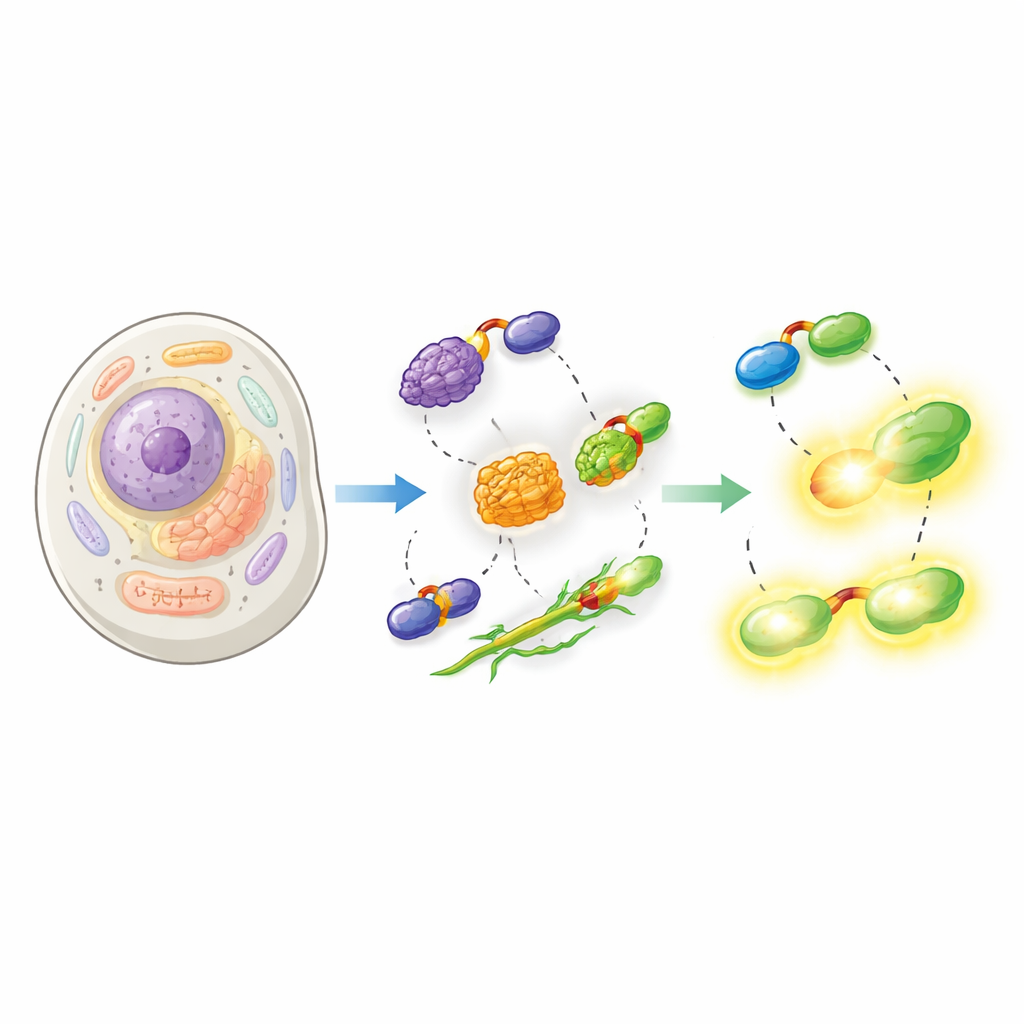
Die Grenzen moderner Mikroskopie verschieben
Über die Standard‑Fluoreszenzbildgebung hinaus wurde das neue Tag mit einigen der anspruchsvollsten optischen Techniken getestet. Mit speziellen Farbstoffen, die für Superauflösung und STED‑/Depletionsmikroskopie geeignet sind, konnten die Autoren mitochondriale Membranen und Mikrotubuli mit Details unterhalb der klassischen Beugungsgrenze auflösen, in manchen Fällen sogar in lebenden Zellen. Sie kombinierten das System außerdem mit Expansion Microscopy, bei der fixierte Zellen physikalisch aufgequollen werden, um feine Strukturen sichtbar zu machen, sowie mit Fluoreszenzlebensdauer‑Bildgebung. Verschiedene Hpep‑Varianten veränderten die Verweildauer des Farbstoffs im angeregten Zustand, sodass zwei mit derselben Farbe markierte Proteine allein nach ihrer Lebensdauer unterschieden werden konnten und multiplexe Bildgebung mit nur einem cpHaloΔ3‑Partner ermöglicht wurde.
Warum dieses neue Tag wichtig ist
In ihrer Summe ergeben diese Fortschritte ein kompaktes, flexibles Markierungssystem, das die genetische Bequemlichkeit winziger Peptid‑Tags mit der optischen Leistungsfähigkeit synthetischer Farbstoffe verbindet. Hpeps geringe Größe erleichtert das Einfügen in native Gene und reduziert die Wahrscheinlichkeit, die Proteinfunktion zu stören, während cpHaloΔ3 dort helle, stabile Farben bereitstellt, wo und wann sie gebraucht werden. Das Ergebnis ist eine hochkontrastige, gegen Hintergrundrauschen weitgehend unempfindliche Methode, um Proteine in lebenden Zellen zu beobachten, kompatibel mit fortgeschrittenen Mikroskopen und Mehrziel‑Experimenten. Dieses Split‑HaloTag‑Werkzeugset dürfte Forschenden helfen, die Organisation zellulärer Komponenten und ihre zeitlichen Veränderungen in Gesundheit und Krankheit genauer zu kartieren.
Zitation: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Schlüsselwörter: Proteinmarkierung, Live‑Cell‑Imaging, HaloTag, CRISPR‑Markierung, Superauflösungsmikroskopie