Clear Sky Science · ru
Разделённый HaloTag с высокой аффинностью для мечения белков в живых клетках
Наблюдая скрытую «машинерию» внутри живых клеток
Современная биология опирается на возможность наблюдать отдельные белки в действии внутри живых клеток, но прикрепить к этим белкам яркие молекулярные «фонарики», не нарушив их работу, оказывается задачей не из простых. В этой работе представлен новый метод мечения, который встраивает крошечный пептидный тег в белок и затем подсвечивает его мощными химическими красителями, позволяя исследователям в реальном времени отслеживать даже редкие и хрупкие мишени на современных микроскопах.
Крошечный тег встречает мощный свет
Исследование опирается на HaloTag — широко используемую метку белков, образующую прочную связь со специальными флуоресцентными красителями. HaloTag яркий и универсальный, но сравнительно громоздкий, что может мешать нормальной функции белка, к которому он присоединён. Авторы решили эту проблему, разделив HaloTag на две части: очень маленький пептид Hpep длиной всего 14 аминокислот и более крупный партнёрный белок cpHaloΔ3. Небольшой Hpep можно напрямую встроить в белок интереса, а cpHaloΔ3 поставляется отдельно. Когда они встречаются в клетке, две части с высокой аффинностью сцепляются и восстанавливают активный HaloTag, способный захватывать яркие красители.
Проектирование «светового выключателя», сцепляющегося вмиг
Чтобы сделать эту разделённую систему практичной, команде пришлось одновременно уравновесить несколько свойств. Hpep и cpHaloΔ3 должны были распознавать друг друга крайне прочно, чтобы пометить даже одиночную копию белка с низкой экспрессией, но при этом cpHaloΔ3 в одиночку должен оставаться практически неактивным, чтобы избежать нежелательного фонового свечения. С помощью дисплея на дрожжах и высокопроизводительной сортировки клеток они отбирали библиотеки немного модифицированных фрагментов cpHalo в поисках вариантов, которые молчали в одиночестве, но быстро и эффективно реагировали при связывании с Hpep. Итоговая версия, cpHaloΔ3, сочетала наномолярную силу связывания, низкое непреднамеренное мечение и быструю реакцию с красителями после воссоединения двух частей. Варианты Hpep также были настроены так, чтобы при связывании они тонко меняли поведение прикреплённых красителей, влияя как на яркость, так и на время жизни флуоресценции.
Подсветка реальных клеточных структур
Затем исследователи продемонстрировали, что их разделённый HaloTag работает в самых разных клеточных условиях. Они прикрепили Hpep к белкам, маркирующим ядро, поверхность митохондрий и ядерную оболочку, и со-экспрессировали cpHaloΔ3 в человеческих клетках. После добавления проникающих в клетки красителей HaloTag восстановленный комплекс давал чёткие изображения ожидаемых структур с очень низким фоном от несвязанного cpHaloΔ3. Критически важно, что благодаря малому размеру Hpep его можно было встраивать напрямую в геном клетки с помощью CRISPR без необходимости клонировать крупные участки ДНК. Команда показала гладкие «нока-ины» для множества эндогенных белков — от структурных компонентов вроде виментинa до мембранных каналов и кластерина — и продемонстрировала, что их можно обогащать и анализировать с помощью проточной цитометрии и микроскопии.
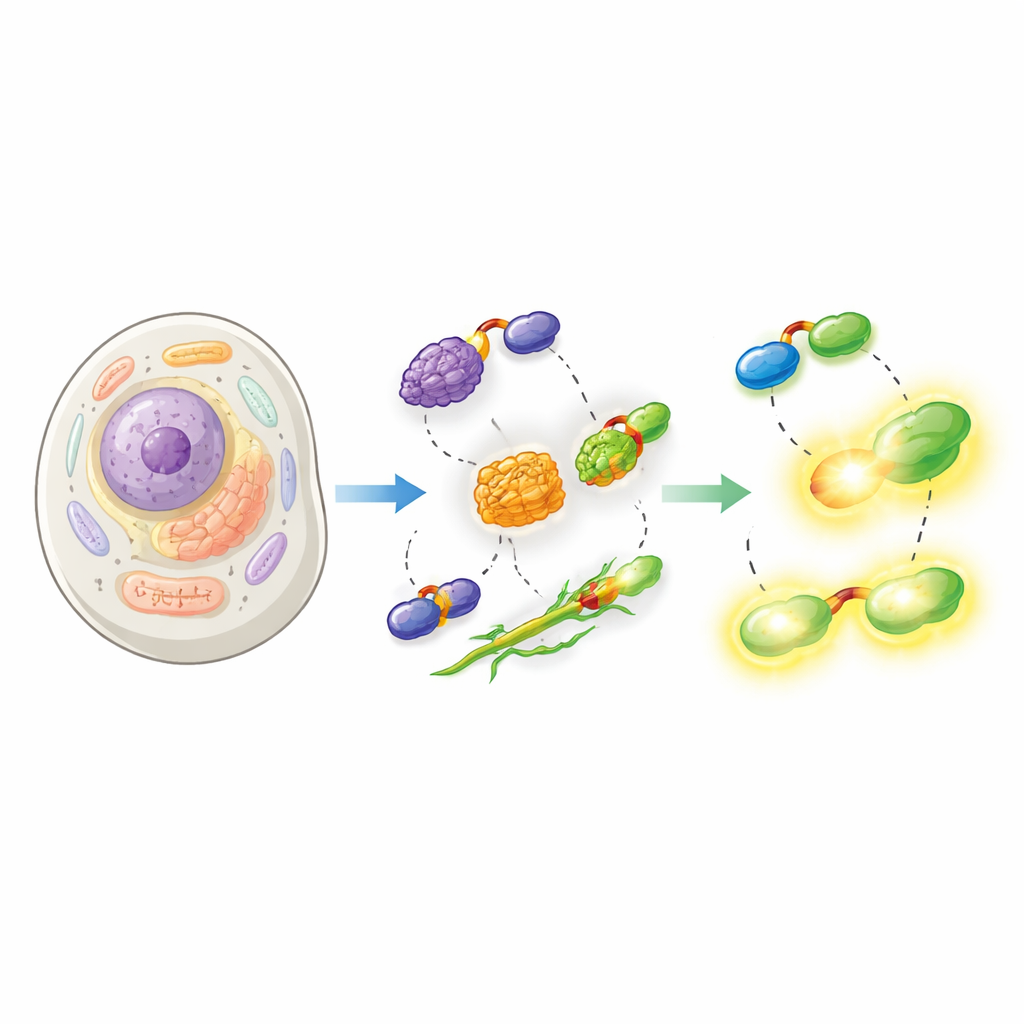
Раздвигая пределы современной микроскопии
Помимо стандартной флуоресцентной визуализации, новый тег протестировали с одними из самых требовательных оптических методов. Используя специальные красители, совместимые с сверхразрешающей и деплеционной микроскопией, авторы разрешали мембраны митохондрий и микротрубочки с детализацией существенно ниже классического дифракционного предела, в ряде случаев в живых клетках. Они также комбинировали систему с микроскопией расширения (expansion microscopy), физически увеличивая фиксированные клетки для выявления тонкой структуры, и с визуализацией времени жизни флуоресценции (FLIM). Различные варианты Hpep изменяли время пребывания красителя в возбужденном состоянии, позволяя отличать два белка, помеченных одним и тем же цветом, исключительно по временам жизни, что обеспечивает мультиплексную визуализацию с одним партнёром cpHaloΔ3.
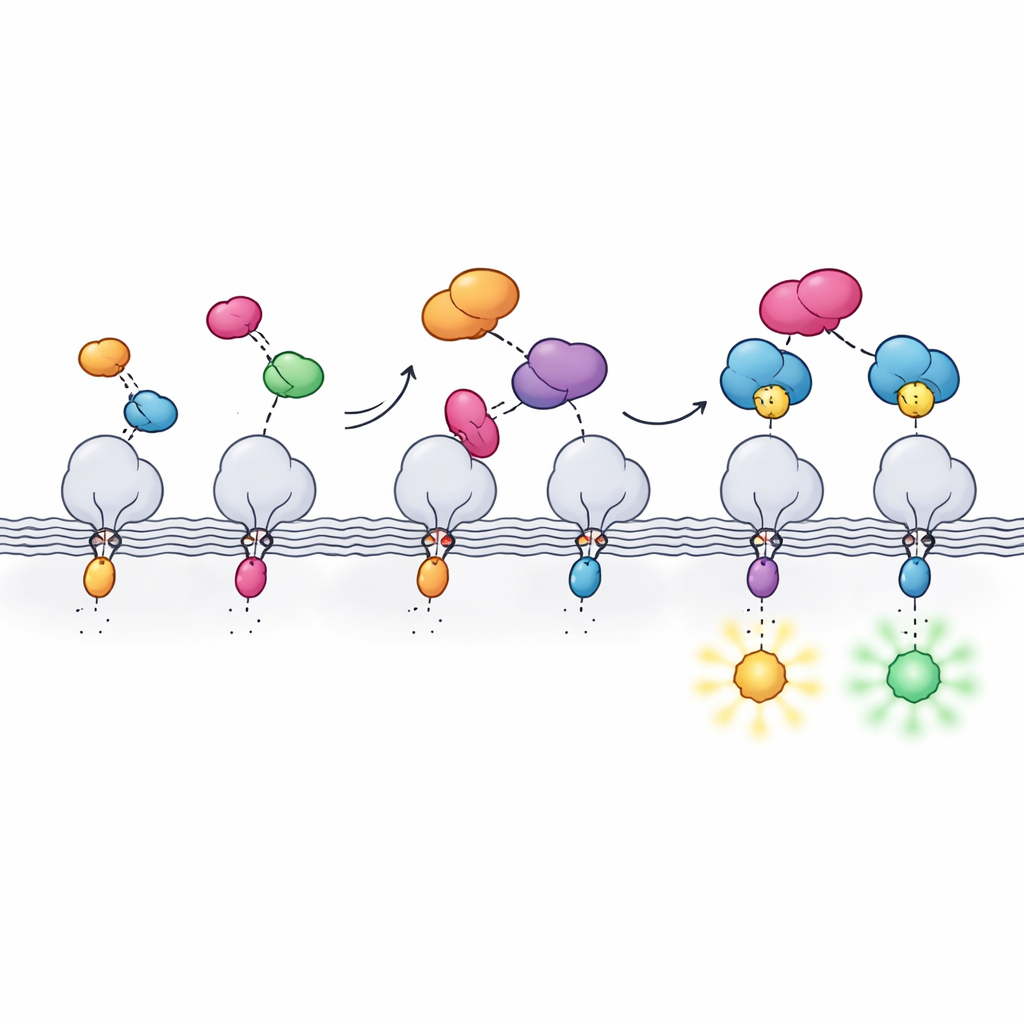
Почему этот новый тег важен
В совокупности эти достижения создают компактную и гибкую систему мечения, которая объединяет генетическое удобство крошечных пептидных тегов с оптической мощью синтетических красителей. Малый размер Hpep облегчает его вставку в нативные гены и снижает вероятность нарушения функции белка, в то время как cpHaloΔ3 приносит яркие, стабильные цвета туда и тогда, где они необходимы. В результате получаем высококонтрастный метод с низким фоновым сигналом для наблюдения белков в живых клетках, совместимый с современными микроскопами и многомишенными экспериментами. Этот набор инструментов разделённого HaloTag поможет исследователям картировать организацию клеточных компонентов и их изменения с течением времени в норме и при заболеваниях.
Цитирование: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Ключевые слова: мечение белков, имиджинг живых клеток, HaloTag, CRISPR-мечение, сверхразрешающая микроскопия