Clear Sky Science · es
Un split‑HaloTag de alta afinidad para el marcaje de proteínas en células vivas
Ver la maquinaria oculta dentro de las células vivas
La biología moderna depende de poder observar proteínas individuales en acción dentro de células vivas, pero unir “linternas” moleculares brillantes a esas proteínas sin alterarlas resulta sorprendentemente difícil. Este estudio presenta un nuevo sistema de marcaje que inserta una etiqueta diminuta en una proteína y luego la ilumina con colorantes químicos potentes, permitiendo a los investigadores seguir objetivos escasos y delicados en tiempo real con microscopios de última generación.
Una etiqueta diminuta se encuentra con una luz poderosa
El trabajo se basa en HaloTag, una etiqueta proteica ampliamente usada que forma un enlace permanente con colorantes fluorescentes especiales. HaloTag es brillante y versátil, pero también voluminoso, lo que puede interferir con el comportamiento normal de la proteína a la que se fusiona. Los autores solucionan esto dividiendo HaloTag en dos piezas: un péptido muy pequeño llamado Hpep, de solo 14 residuos, y una proteína compañera mayor llamada cpHaloΔ3. El pequeño Hpep puede integrarse directamente en la proteína de interés, mientras que cpHaloΔ3 se suministra por separado. Cuando se encuentran dentro de la célula, las dos piezas se ensamblan con muy alta afinidad y recrean un HaloTag activo capaz de capturar colorantes brillantes.
Diseñar un interruptor luminoso que encaje
Para que este sistema partido fuera práctico, el equipo tuvo que equilibrar varias propiedades a la vez. Hpep y cpHaloΔ3 necesitaban reconocerse con extrema afinidad para que incluso una copia única en una proteína de baja abundancia fuera etiquetada, pero cpHaloΔ3 por sí solo debía permanecer casi inactivo para evitar un resplandor de fondo indeseado. Usando display en levadura y clasificación celular de alto rendimiento, cribaron bibliotecas de fragmentos cpHalo ligeramente alterados en busca de variantes que fueran silenciosas en solitario pero rápidas y eficientes una vez unidas a Hpep. La versión final, cpHaloΔ3, combinó afinidad en el rango nanomolar, bajo etiquetado no deseado y reacción rápida con colorantes una vez reunidas las dos piezas. También se ajustaron variantes de Hpep para que, al unirse, modificaran sutilmente el comportamiento de los colorantes unidos, alterando tanto el brillo como el tiempo de vida fluorescente.
Iluminando estructuras celulares reales
Los investigadores mostraron que su split‑HaloTag funciona en una amplia gama de contextos celulares. Colocaron Hpep en proteínas que marcan el núcleo, la superficie mitocondrial y la envoltura nuclear, y co‑expresaron cpHaloΔ3 en células humanas. Tras añadir colorantes permeables a la célula para HaloTag, la etiqueta reconstituida produjo imágenes nítidas de las estructuras esperadas con muy poco fondo procedente de cpHaloΔ3 no unido. De forma crucial, debido al tamaño diminuto de Hpep, pudo insertarse directamente en los genes endógenos mediante CRISPR sin necesidad de clonar grandes constructos de ADN. El equipo demostró inserciones “knock‑in” sencillas para muchas proteínas endógenas distintas, desde componentes estructurales como la vimentina hasta canales de membrana y clatrina, y mostró que estas etiquetas podían enriquecerse y analizarse mediante citometría y microscopía.
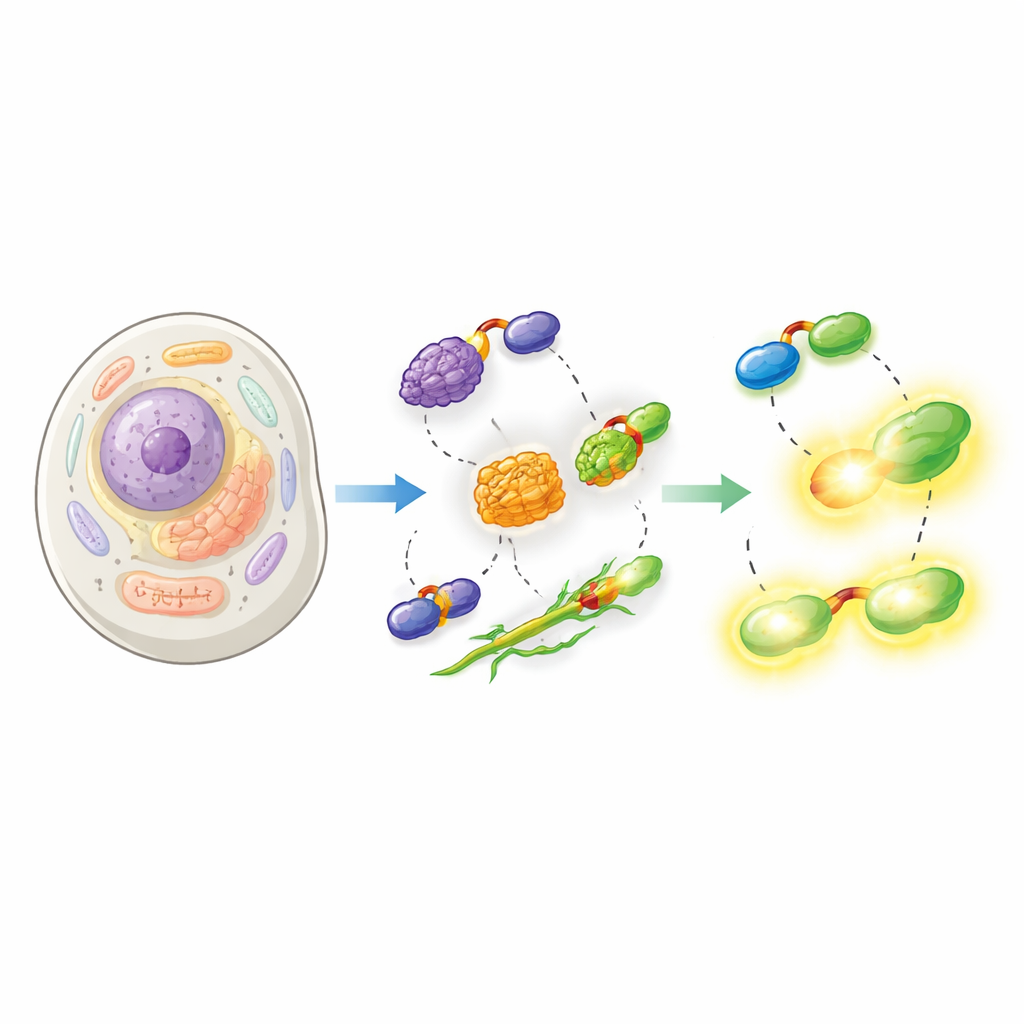
Empujando los límites de la microscopía moderna
Más allá de la imagen fluorescente estándar, la nueva etiqueta se probó con algunas de las técnicas ópticas más exigentes. Usando colorantes especiales compatibles con microscopía de superresolución y microscopía por agotamiento, los autores resolvieron membranas mitocondriales y microtúbulos con detalles muy por debajo del límite de difracción convencional, en algunos casos en células vivas. También combinaron el sistema con microscopía de expansión, hinchando físicamente células preservadas para revelar estructura fina, y con imágenes por tiempo de vida fluorescente. Distintas variantes de Hpep modificaron cuánto tiempo permanecía el colorante en su estado excitado, permitiendo distinguir dos proteínas etiquetadas con el mismo color únicamente por sus tiempos de vida y habilitando imagen multiplexada con un único socio cpHaloΔ3.
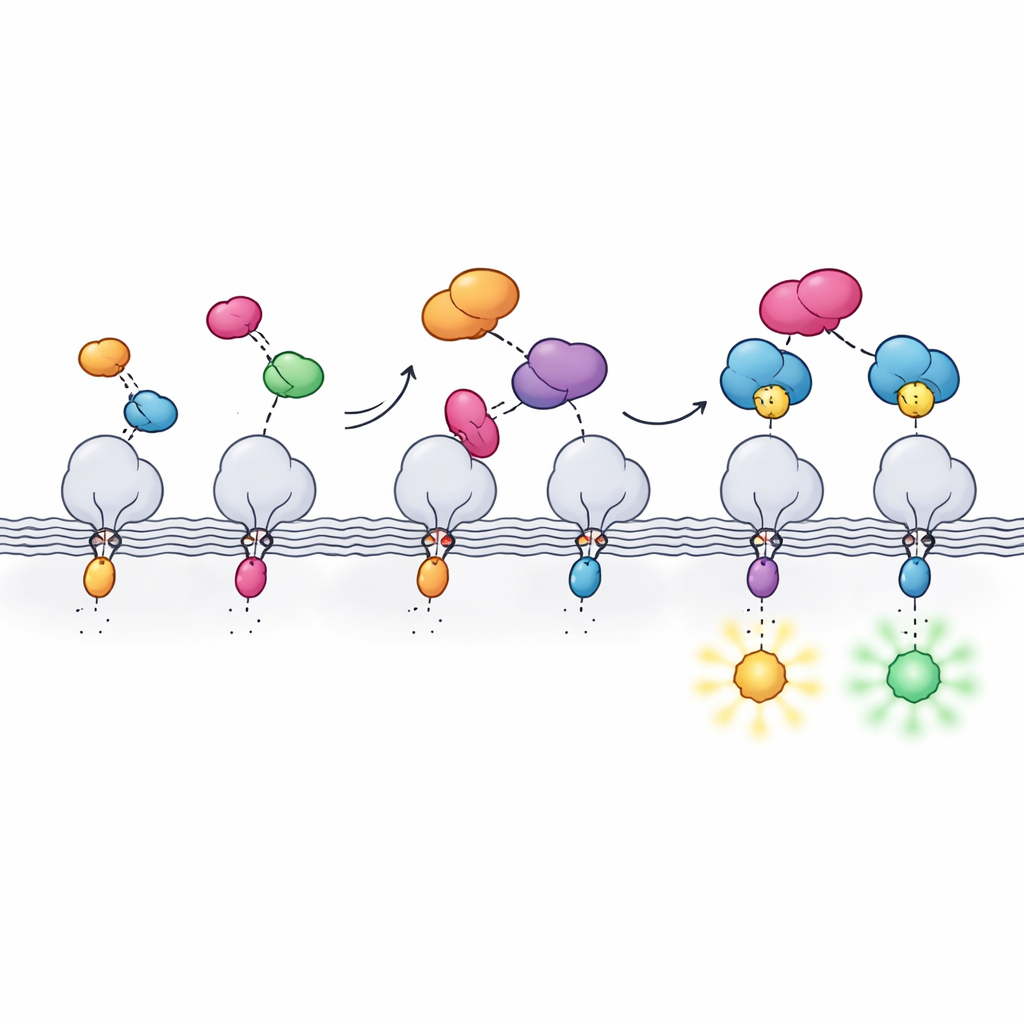
Por qué importa esta nueva etiqueta
En conjunto, estos avances crean un sistema de marcaje compacto y flexible que fusiona la comodidad genética de las etiquetas peptídicas diminutas con la potencia óptica de los colorantes sintéticos. El tamaño reducido de Hpep facilita su inserción en genes nativos y reduce la probabilidad de alterar la función proteica, mientras que cpHaloΔ3 aporta colores brillantes y estables cuando y donde se necesitan. El resultado es una forma de alto contraste y bajo fondo para observar proteínas dentro de células vivas, compatible con microscopios avanzados y experimentos multietiqueta. Este conjunto de herramientas split‑HaloTag debería ayudar a los investigadores a cartografiar cómo se organizan los componentes celulares y cómo cambian con el tiempo en salud y enfermedad.
Cita: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Palabras clave: marcaje de proteínas, imagen en células vivas, HaloTag, marcado CRISPR, microscopía de superresolución