Clear Sky Science · fr
Un split-HaloTag à haute affinité pour le marquage protéique en cellules vivantes
Voir la machinerie cachée à l’intérieur des cellules vivantes
La biologie moderne repose sur la capacité à observer des protéines individuelles à l’œuvre à l’intérieur de cellules vivantes, mais attacher des « lampes » moléculaires lumineuses à ces protéines sans les perturber est surprenamment difficile. Cette étude présente un nouveau système de marquage qui glisse une petite étiquette dans une protéine puis l’illumine avec des colorants chimiques puissants, permettant aux chercheurs de suivre en temps réel des cibles rares et fragiles avec des microscopes de pointe.
Une petite étiquette rencontre une lumière puissante
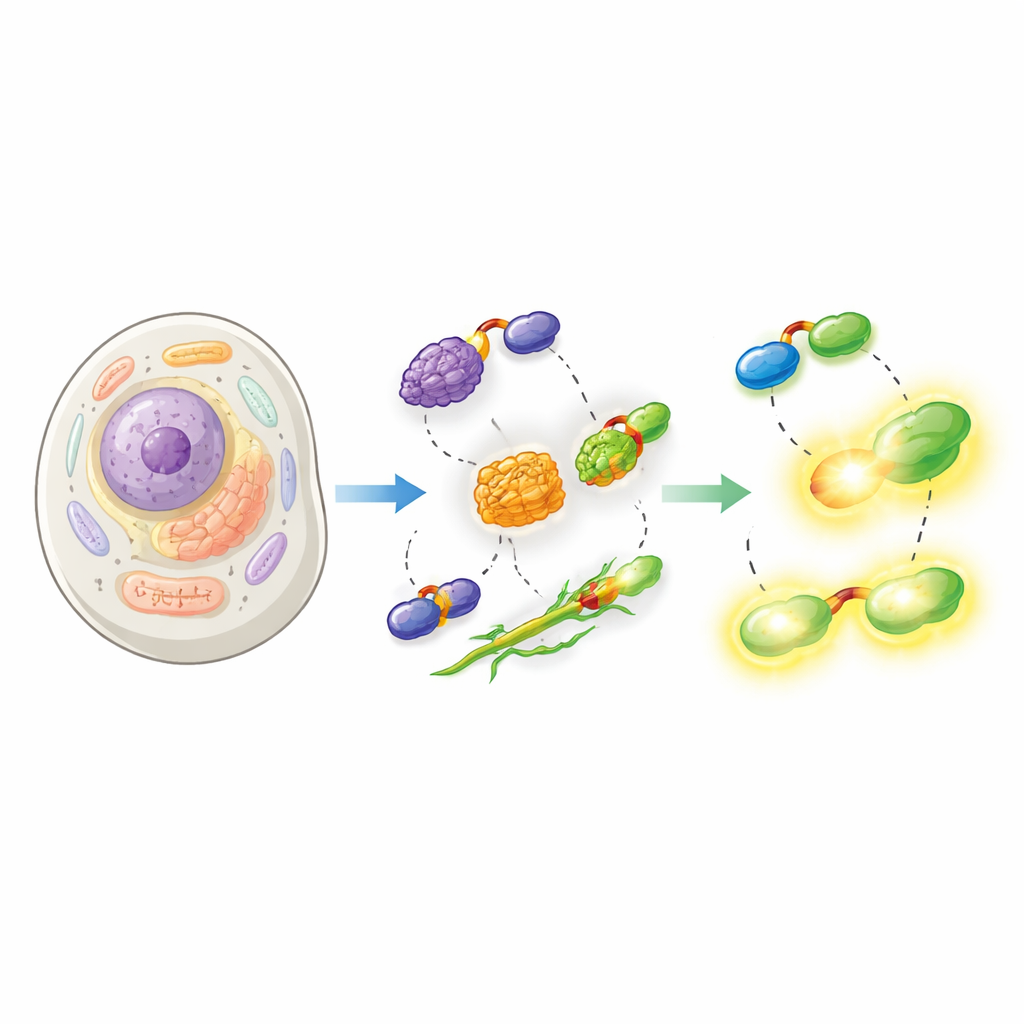
Le travail s’appuie sur HaloTag, un marqueur protéique largement utilisé qui forme une liaison permanente avec des colorants fluorescents spéciaux. HaloTag est lumineux et polyvalent mais il est aussi encombrant, ce qui peut interférer avec le comportement normal de la protéine à laquelle il est fusionné. Les auteurs résolvent ce problème en scindant HaloTag en deux morceaux : un très petit peptide appelé Hpep, d’à peine 14 acides aminés, et une protéine partenaire plus grande appelée cpHaloΔ3. Le petit Hpep peut être inséré directement dans la protéine d’intérêt, tandis que cpHaloΔ3 est fourni séparément. Lorsqu’ils se rencontrent à l’intérieur d’une cellule, les deux morceaux se rejoignent avec une affinité très élevée et recréent un HaloTag actif capable de capturer des colorants lumineux.
Concevoir un interrupteur lumineux qui s’emboîte
Pour rendre ce système scindé pratique, l’équipe a dû équilibrer plusieurs propriétés à la fois. Hpep et cpHaloΔ3 devaient se reconnaître extrêmement fortement afin que même une copie isolée sur une protéine de faible abondance soit marquée, mais cpHaloΔ3 seul devait rester presque inactif pour éviter un halo de fond indésirable. En utilisant l’affichage sur levure et le tri cellulaire à haut débit, ils ont criblé des bibliothèques de fragments cpHalo légèrement modifiés à la recherche de variantes silencieuses seules mais rapides et efficaces une fois liées à Hpep. La version finale, cpHaloΔ3, associe une affinité nanomolaire, un faible marquage non spécifique et une réaction rapide avec les colorants dès que les deux morceaux se retrouvent. Des variantes de Hpep ont aussi été ajustées de sorte que, une fois liées, elles modifient subtilement le comportement des colorants attachés, altérant à la fois la brillance et la durée de vie de la fluorescence.
Illuminer de véritables structures cellulaires
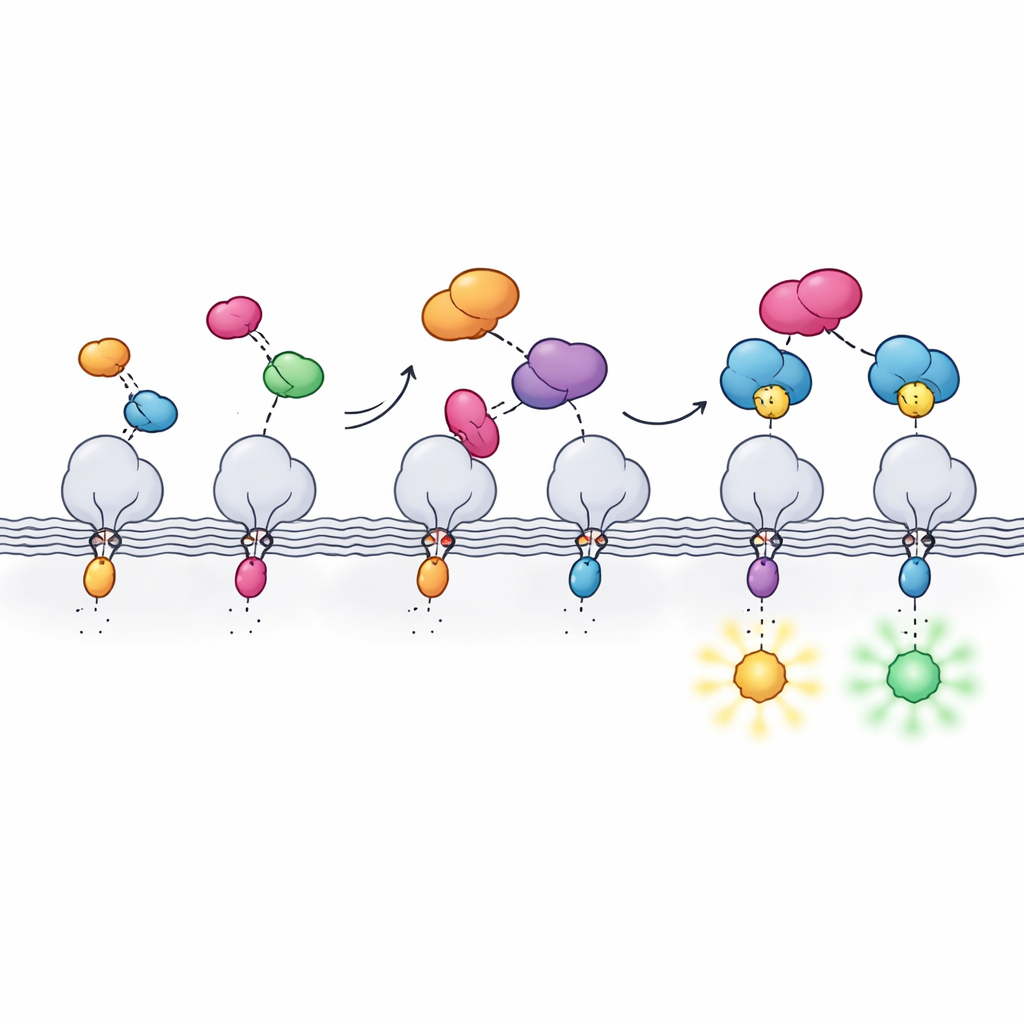
Les chercheurs ont ensuite montré que leur split-HaloTag fonctionne dans une large gamme de contextes cellulaires. Ils ont attaché Hpep à des protéines marquant le noyau, la surface mitochondriale et l’enveloppe nucléaire, et ont co-exprimé cpHaloΔ3 dans des cellules humaines. Après ajout de colorants HaloTag perméables aux cellules, l’étiquette reconstituée a produit des images nettes des structures attendues avec très peu de fond provenant du cpHaloΔ3 non lié. De manière cruciale, comme Hpep est si petit, il a pu être inséré directement dans les gènes endogènes par CRISPR sans nécessiter le clonage de gros fragments d’ADN. L’équipe a démontré des « knock-ins » sans couture pour de nombreuses protéines endogènes différentes, depuis des composants structuraux comme la vimentine jusqu’à des canaux membranaires et la clathrine, et a montré que ces cibles pouvaient être enrichies et analysées par cytométrie en flux et microscopie.
Repousser les limites de la microscopie moderne
Au-delà de l’imagerie de fluorescence standard, la nouvelle étiquette a été testée avec certaines des techniques optiques les plus exigeantes. En utilisant des colorants spéciaux compatibles avec la super-résolution et la microscopie par déplétion, les auteurs ont résolu les membranes mitochondriales et les microtubules avec des détails bien en dessous de la limite de diffraction conventionnelle, dans certains cas dans des cellules vivantes. Ils ont également combiné le système avec la microscopie d’expansion, gonflant physiquement des cellules préservées pour révéler la structure fine, et avec l’imagerie du temps de vie de fluorescence. Différentes variantes de Hpep ont modifié la durée pendant laquelle le colorant restait à l’état excité, permettant de distinguer deux protéines marquées avec la même couleur uniquement par leurs temps de vie et autorisant l’imagerie multiplexée avec un seul partenaire cpHaloΔ3.
Pourquoi cette nouvelle étiquette est importante
Ensemble, ces avancées créent un système de marquage compact et flexible qui réunit la commodité génétique des petits peptides avec la puissance optique des colorants synthétiques. La petite taille de Hpep facilite son insertion dans les gènes natifs et réduit le risque de perturber la fonction protéique, tandis que cpHaloΔ3 apporte des couleurs lumineuses et stables au moment et à l’endroit voulus. Le résultat est une méthode à fort contraste et faible bruit de fond pour observer les protéines à l’intérieur de cellules vivantes, compatible avec des microscopes avancés et des expériences multi-cibles. Cette boîte à outils split-HaloTag devrait aider les chercheurs à cartographier l’organisation des composants cellulaires et leur évolution dans le temps en santé et en maladie.
Citation: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Mots-clés: marquage des protéines, imagerie en cellules vivantes, HaloTag, étiquetage CRISPR, microscopie super-résolution