Clear Sky Science · it
Un sistema split‑HaloTag ad alta affinità per l’etichettatura di proteine in cellule vive
Osservare la macchina nascosta all’interno delle cellule vive
La biologia moderna dipende dalla possibilità di osservare singole proteine al lavoro dentro cellule vive, ma fissare a quelle proteine “torce” molecolari luminose senza alterarne il comportamento è sorprendentemente difficile. Questo studio introduce un nuovo sistema di etichettatura che inserisce un piccolo tag nella proteina e poi lo illumina con potenti coloranti chimici, permettendo ai ricercatori di seguire in tempo reale bersagli rari e fragili con microscopi all’avanguardia.
Un tag minuscolo incontra una luce potente
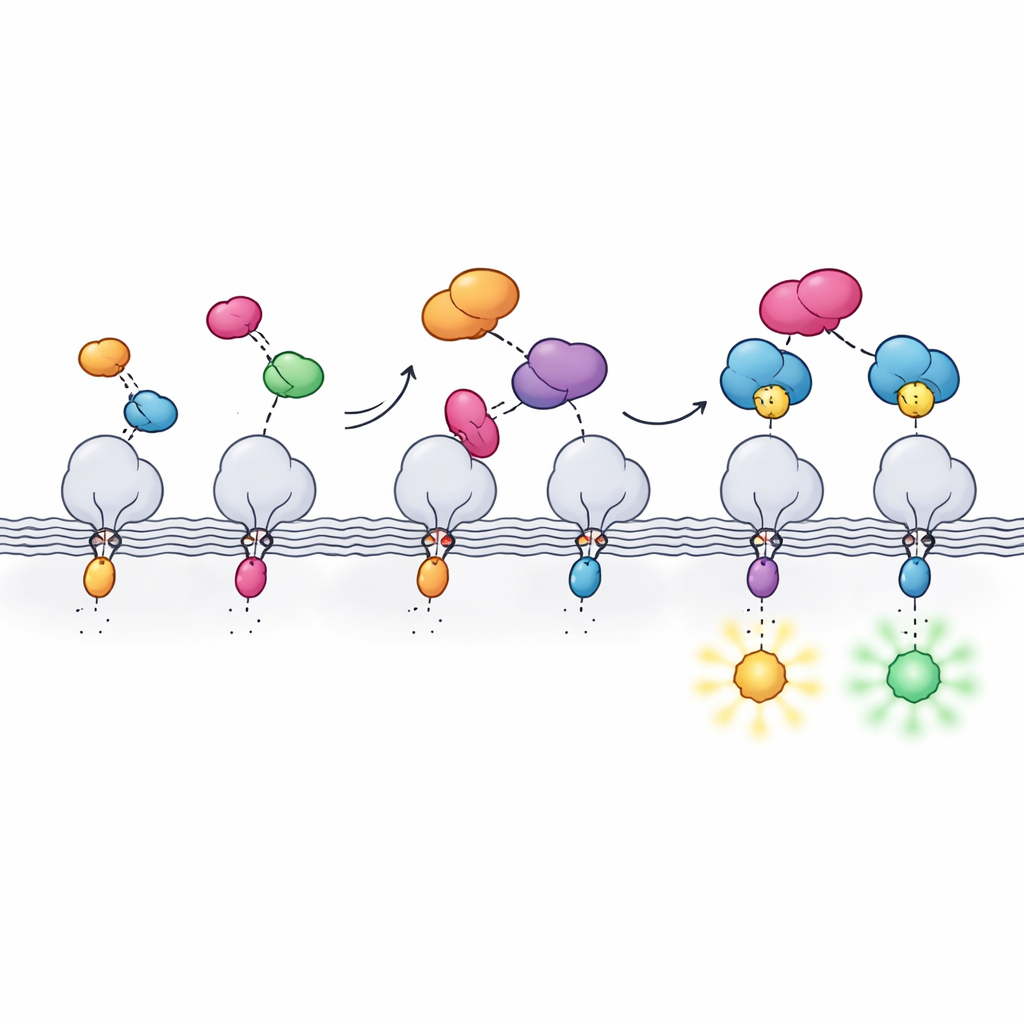
Il lavoro si basa su HaloTag, un marcatore proteico ampiamente usato che forma un legame permanente con specifici coloranti fluorescenti. HaloTag è brillante e versatile ma anche ingombrante, il che può interferire con il comportamento normale della proteina a cui è fuso. Gli autori risolvono questo problema dividendo HaloTag in due pezzi: un peptide molto piccolo chiamato Hpep, lungo solo 14 amminoacidi, e una proteina partner più grande chiamata cpHaloΔ3. Il piccolo Hpep può essere inserito direttamente nella proteina di interesse, mentre cpHaloΔ3 viene fornito separatamente. Quando si incontrano all’interno della cellula, i due pezzi si riuniscono con altissima affinità e ricreano un HaloTag attivo in grado di catturare coloranti brillanti.
Progettare un interruttore luminoso che si snap‑incastra
Per rendere pratico questo sistema split, il team ha dovuto bilanciare simultaneamente diverse proprietà. Hpep e cpHaloΔ3 dovevano riconoscersi estremamente saldamente in modo che anche una singola copia su una proteina presente in bassa abbondanza venisse etichettata, ma cpHaloΔ3 da solo doveva rimanere quasi inattivo per evitare un fastidioso bagliore di fondo. Usando l’espressione su lievito e il sorting cellulare ad alto rendimento, hanno screenato librerie di frammenti cpHalo leggermente modificati per varianti che fossero silenziose da sole ma veloci ed efficienti una volta legate a Hpep. La versione finale, cpHaloΔ3, ha combinato affinità nell’ordine dei nanomolari, bassa etichettatura non voluta e reazione rapida con i coloranti quando i due pezzi si ricomponevano. Anche le varianti di Hpep sono state ottimizzate in modo che, una volta legate, modificassero sottilmente il comportamento dei coloranti allegati, alterandone sia la luminosità sia il tempo di vita fluorescente.
Illuminare strutture cellulari reali
I ricercatori hanno quindi dimostrato che il loro split‑HaloTag funziona in un’ampia gamma di contesti cellulari. Hanno unito Hpep a proteine che marcano il nucleo, la superficie mitocondriale e l’involucro nucleare, ed espresso contemporaneamente cpHaloΔ3 in cellule umane. Dopo l’aggiunta di coloranti HaloTag permeabili alle cellule, il tag ricostituito ha prodotto immagini nitide delle strutture attese con pochissimo fondo dovuto a cpHaloΔ3 non legato. Fondamentale, poiché Hpep è così piccolo, può essere inserito direttamente nei geni endogeni della cellula usando CRISPR senza bisogno di clonare grandi costrutti di DNA. Il team ha dimostrato inserimenti “knock‑in” efficienti per molte proteine endogene diverse, da componenti strutturali come la vimentina a canali di membrana e clatrina, e ha mostrato che questi potevano essere arricchiti e analizzati mediante citometria a flusso e microscopia.
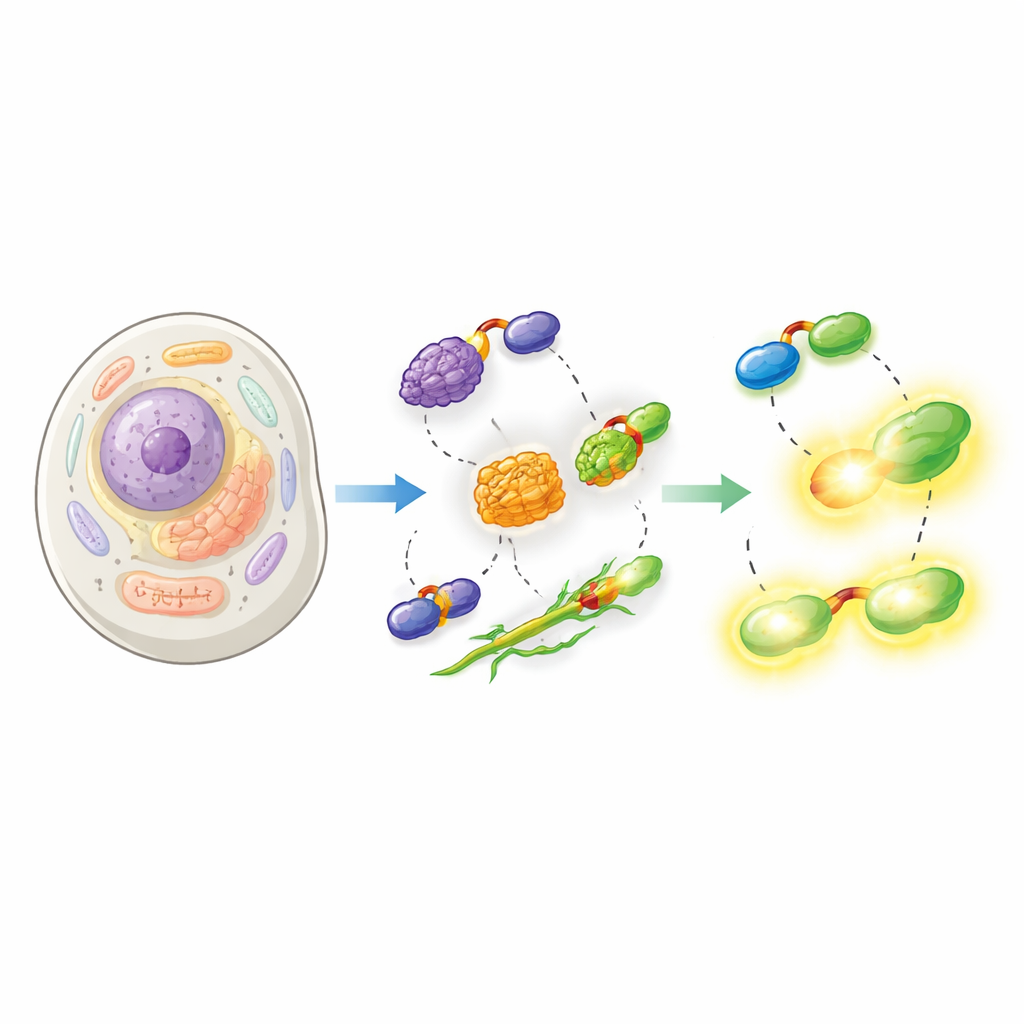
Spingere i limiti della microscopia moderna
Oltre all’imaging fluorescente standard, il nuovo tag è stato testato con alcune delle tecniche ottiche più esigenti. Usando coloranti speciali compatibili con la super-risoluzione e la microscopia a deplezione, gli autori hanno risolto membrane mitocondriali e microtubuli con dettagli molto al di sotto del limite di diffrazione convenzionale, in alcuni casi in cellule vive. Hanno inoltre combinato il sistema con la microscopia di espansione, gonfiando fisicamente cellule fissate per rivelare strutture fini, e con l’imaging del tempo di vita fluorescente. Diverse varianti di Hpep hanno modificato il tempo durante il quale il colorante resta nello stato eccitato, permettendo di distinguere due proteine etichettate con lo stesso colore soltanto in base ai loro tempi di vita e abilitando l’imaging multiplex con un singolo partner cpHaloΔ3.
Perché questo nuovo tag è importante
Nel complesso, questi progressi creano un sistema di etichettatura compatto e flessibile che fonde la comodità genetica di tag peptidici minuscoli con la potenza ottica dei coloranti sintetici. La piccola dimensione di Hpep ne facilita l’inserimento nei geni nativi ed è meno probabile che comprometta la funzione proteica, mentre cpHaloΔ3 fornisce colori brillanti e stabili quando e dove servono. Il risultato è un modo ad alto contrasto e basso rumore di fondo per osservare le proteine dentro cellule vive, compatibile con microscopi avanzati ed esperimenti multi‑bersaglio. Questo kit split‑HaloTag dovrebbe aiutare i ricercatori a mappare come i componenti cellulari sono organizzati e come cambiano nel tempo in salute e malattia.
Citazione: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Parole chiave: etichettatura delle proteine, imaging in cellule vive, HaloTag, tagging CRISPR, microscopia a super-risoluzione