Clear Sky Science · sv
Strukturell grund för cyklin Y/14-3-3-proteinernas medierade aktivering av CDK16
Varför detta proteinpussel är viktigt
Inuti våra celler samarbetar proteinteam som små maskiner för att kontrollera tillväxt, överlevnad och hur celler reagerar på stress. Ett sådant protein, CDK16, påverkar nervcellernas kopplingar, återvinning av cellinnehåll, fertilitet och cancercellsbeteende. Ändå är CDK16 märkligt passivt om inte två specifika hjälpproteiner, cyklin Y och 14-3-3, kommer samman på precis rätt sätt. I den här studien visas, atom för atom, hur den ovanliga tredelningen monteras och hur deras handslag förvandlar CDK16 från vilande till aktivt — vilket ger nya ledtrådar för framtida läkemedelsdesign som riktar in sig på detta kontrollsystem.
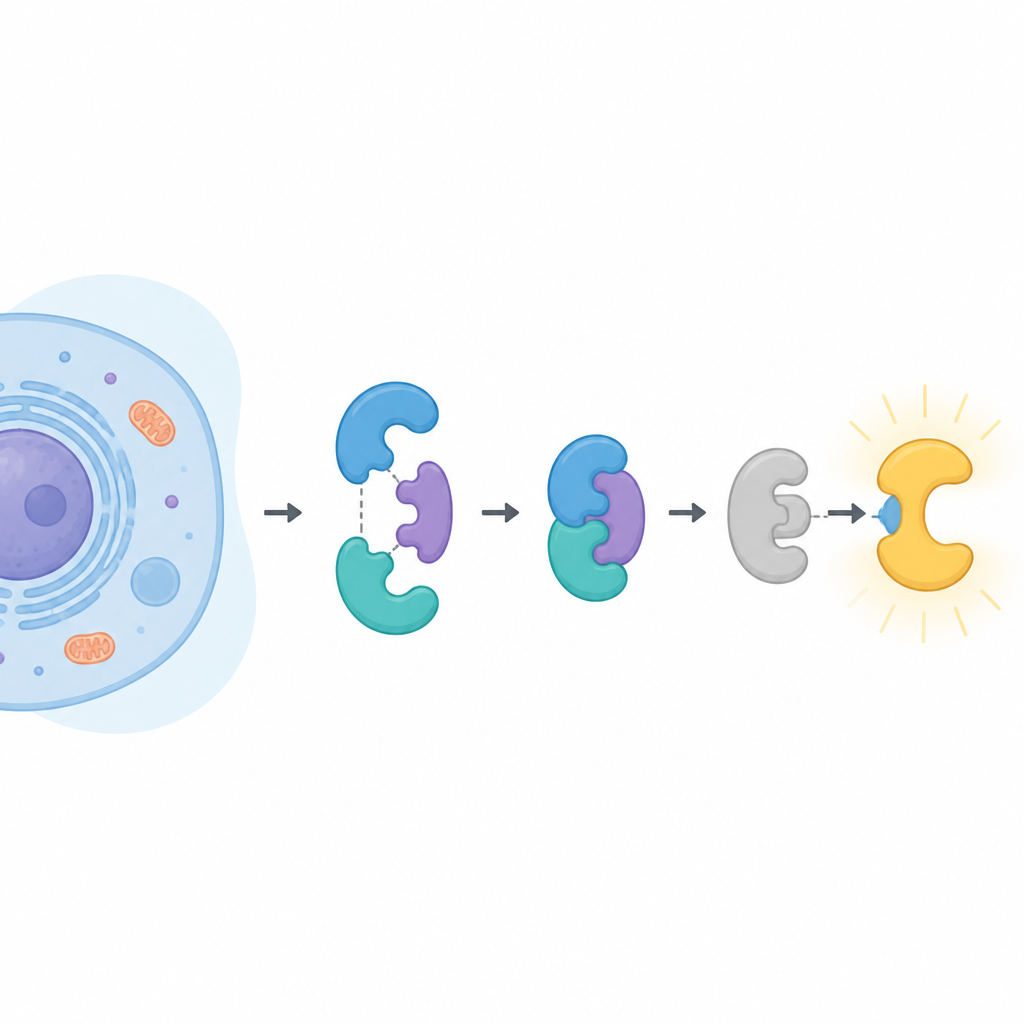
De viktigaste aktörerna i cellen
CDK16 tillhör en stor familj enzymer som fäster små fosfatmärken på andra proteiner och ändrar deras aktivitet. De flesta släktingar aktiveras enkelt genom bindning till en partner kallad cyklin. CDK16 är annorlunda. Det vaknar endast när det är bundet till cyklin Y, som i sig måste vara försett med fosfatmärken och hållas på plats av ett annat proteinpar känt som 14-3-3. CDK16 har kopplats till hjärnans utveckling, slutstadierna av spermieutveckling, hur celler återvinner sitt innehåll vid svält, samt till tillväxt och läkemedelsresistens i flera cancerformer. Att förstå exakt hur CDK16 styrs kan därför belysa både normal biologi och sjukdom.
Hur hjälpparet omformar cyklin Y
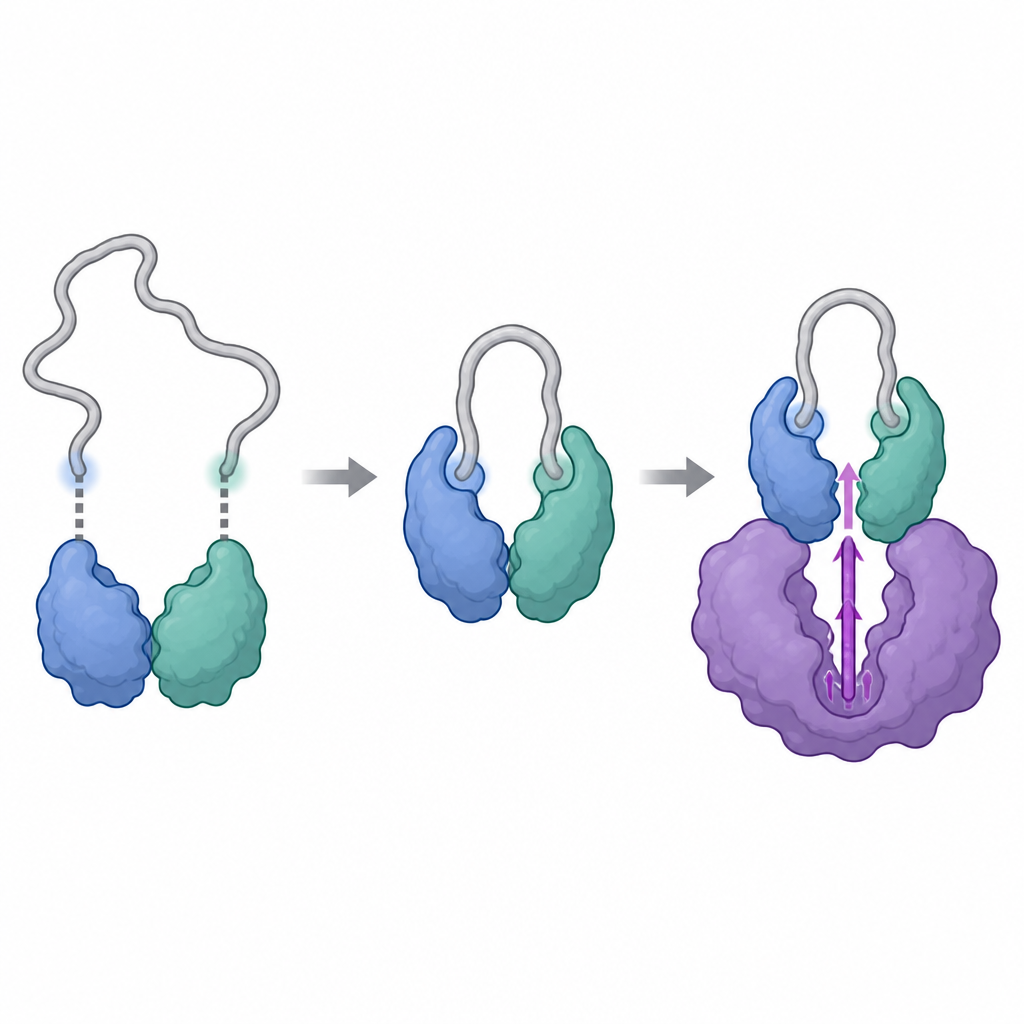
Forskarna använde kraftfulla strukturella verktyg, inklusive kryoelektronmikroskopi och en teknik som följer hur väteatomer i ett protein byts mot tungt vatten, för att visualisera komplexen som bildas av cyklin Y och 14-3-3, med och utan CDK16. De fann att cyklin Y bär två specifika platser som var och en kan haka i ena halvan av 14-3-3-paret, som två knappar i ett spänne. När båda platserna är fosforylerade och engagerade griper 14-3-3 tag i cyklin Y och omformar subtilt en viktig yta. Denna omformning blottlägger och styvar upp det område som senare kommer att interagera med CDK16, vilket gör cyklin Y till en mer lämplig dockningspartner än det skulle vara ensam.
Hur CDK16 slås på
När cyklin Y hålls korrekt av 14-3-3 kan CDK16 binda och slutföra monteringen. De strukturella ögonblicksbilderna visar att CDK16 omfamnar cyklin Y med två huvudkontaktzoner: en central region som liknar den typiska dockningsplatsen som ses i andra cyklinberoende enzymer, och en extra flexibel svans i CDK16:s framkant som är unik för denna underfamilj. När CDK16 binder veckar sig denna lösa svans och fäster mot cyklin Y, vilket hjälper till att låsa ihop komplexet. Samtidigt blir CDK16:s aktiveringsslinga, ett rörligt segment nära dess kemiska centrum, ordnad och hålls i ett "på"-läge genom direkta beröringar från både cyklin Y och änden av 14-3-3-paret. Mutationer i nyckelaminosyror vid dessa gränssnitt försvagar komplexet och minskar CDK16:s aktivitet kraftigt, vilket bekräftar att dessa strukturella kontakter är väsentliga för att slå på enzymet.
Finjustering av kontrollbrytaren
Studien visar också hur CDK16 självt kan ställas in av ytterligare fosfatmärken på sin egen framkantssvans. I tidigare arbete var vissa platser i denna svans kända för att påverka hur väl cyklin Y binder. De nya strukturella och dynamiska uppgifterna tyder på att tillägg eller borttagning av dessa märken kan ändra hur svansen veckar sig och om den kan engagera sig med cyklin Y–14-3-3-komplexet. I vissa fall kan märkena till och med rekrytera 14-3-3 direkt till CDK16, blockera åtkomst till cyklin Y eller skydda dessa regulatoriska platser från att återställas. På så sätt använder cellerna en flerskiktad kontroll där både cyklin Y och CDK16 måste bära rätt fosfatmärken innan ett fullt aktivt komplex kan bildas.
Vad detta betyder för hälsa och sjukdom
Genom att lägga fram den tredelade omfamningen mellan CDK16, cyklin Y och 14-3-3 i molekylär detalj förklarar detta arbete varför CDK16 vägrar att aktiveras utan sina hjälpare och hur deras interaktion skjuter enzymet i dess aktiva form. För icke-specialister är slutsatsen att CDK16 inte är en ensam strömbrytare utan en del av ett noggrant kopplat säkerhetssystem som är beroende av flera proteinkontakter och kemiska märken. Eftersom CDK16 bidrar till cancercellers överlevnad och resistens mot behandling, erbjuder de nyupptäckta kontaktytorna specifika mål där framtida läkemedel kan kilas in och störa komplexet, vilket selektivt dämpar CDK16:s aktivitet samtidigt som närliggande enzymer påverkas mindre.
Citering: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Nyckelord: CDK16, cyklin Y, 14-3-3-proteiner, proteinkomplex, cancersignalering