Clear Sky Science · de
Strukturelle Grundlage der Aktivierung von CDK16 durch Cyclin Y/14-3-3-Proteine
Warum dieses Proteinrätsel wichtig ist
In unseren Zellen arbeiten Proteinteams wie winzige Maschinen zusammen, um Wachstum, Überleben und die Reaktion auf Stress zu steuern. Ein solches Protein, CDK16, beeinflusst die Verschaltung von Nervenzellen, den Abbau und die Wiederverwertung von Zellbestandteilen, Fruchtbarkeit und das Verhalten von Krebszellen. Doch CDK16 bleibt ungewöhnlich inaktiv, sofern nicht zwei spezifische Helferproteine, Cyclin Y und 14-3-3, in genau der richtigen Weise zusammentreten. Diese Studie zeigt atomgenau, wie dieses ungewöhnliche Trio sich zusammenfügt und wie ihr Zusammenspiel CDK16 vom Ruhezustand in die aktive Form schaltet – ein Befund, der neue Hinweise für die Entwicklung künftiger Krebsmedikamente liefert, die dieses Kontrollsystem anvisieren.
Die Hauptakteure in der Zelle
CDK16 gehört zu einer großen Enzymfamilie, die anderen Proteinen kleine Phosphatmarken anhängt und damit deren Aktivität verändert. Die meisten Verwandten werden einfach durch Bindung an ein Cyclin aktiviert. CDK16 ist anders: Es erwacht nur, wenn es an Cyclin Y gebunden ist, das seinerseits mit Phosphatmarken versehen sein muss und von einem weiteres Proteinpaar, den 14-3-3-Proteinen, gehalten wird. CDK16 wurde mit Gehirnentwicklung, den letzten Stadien der Spermienreifung, der Autophagie bei Nährstoffmangel und dem Wachstum sowie der Medikamentenresistenz verschiedener Krebserkrankungen in Verbindung gebracht. Ein genaues Verständnis der Kontrolle von CDK16 kann daher sowohl normale biologische Prozesse als auch Krankheitsmechanismen beleuchten.
Wie das Helferpaar Cyclin Y umformt
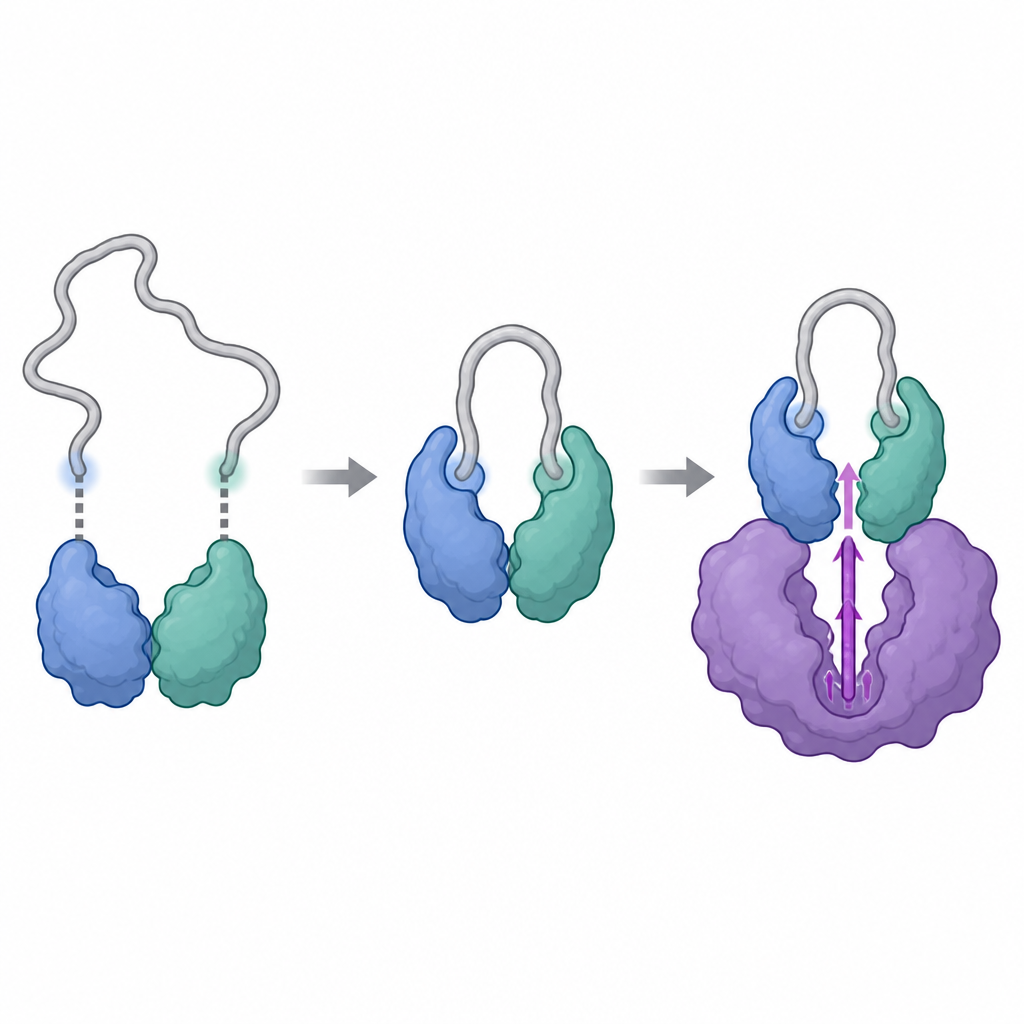
Die Forscher nutzten leistungsfähige Strukturmethoden, darunter Kryo-Elektronenmikroskopie und eine Technik, die verfolgt, wie Wasserstoffatome in einem Protein gegen schweres Wasser ausgetauscht werden, um die von Cyclin Y und 14-3-3 gebildeten Komplexe mit und ohne CDK16 zu visualisieren. Sie fanden heraus, dass Cyclin Y zwei spezifische Stellen trägt, die jeweils an eine Hälfte des 14-3-3-Paares andocken können, vergleichbar mit zwei Knöpfen, die in eine Klammer einrasten. Wenn beide Stellen phosphoryliert und gebunden sind, ergreift 14-3-3 Cyclin Y und formt eine wichtige Oberflächenregion dezent um. Diese Umformung legt einen Bereich frei und versteift ihn, der später mit CDK16 interagieren wird, wodurch Cyclin Y zu einem geeigneteren Andockpartner wird, als es alleine wäre.
Wie CDK16 eingeschaltet wird
Sobald Cyclin Y von 14-3-3 korrekt gehalten wird, kann CDK16 binden und den Komplex vervollständigen. Die strukturellen Momentaufnahmen zeigen, dass CDK16 Cyclin Y mit zwei Hauptkontaktzonen umschließt: einer zentralen Region, die dem typischen Andockplatz anderer cyclinabhängiger Enzyme ähnelt, und einem zusätzlichen, flexiblen Vorderende von CDK16, das für diese Unterfamilie einzigartig ist. Beim Andocken faltet sich dieser schlaffe Schwanz und legt sich an Cyclin Y, was hilft, den Komplex zu verriegeln. Gleichzeitig wird die Aktivierungsschleife von CDK16, ein bewegliches Segment nahe seinem katalytischen Zentrum, geordnet und in eine „ein“-Position gehalten durch direkte Kontakte sowohl von Cyclin Y als auch vom Ende des 14-3-3-Paares. Mutationen wichtiger Aminosäuren an diesen Schnittstellen schwächen den Komplex und reduzieren CDK16-Aktivität deutlich, was bestätigt, dass diese strukturellen Kontakte für die Aktivierung des Enzyms essentiell sind.
Feinabstimmung des Schalters
Die Studie zeigt außerdem, wie CDK16 selbst durch zusätzliche Phosphatmarken an seinem vorderen Schwanz feinjustiert werden kann. In früheren Arbeiten waren bestimmte Stellen in diesem Schwanz bereits dafür bekannt, die Bindung an Cyclin Y zu beeinflussen. Die neuen strukturellen und dynamischen Daten deuten darauf hin, dass das Anbringen oder Entfernen dieser Marken beeinflussen kann, wie sich der Schwanz faltet und ob er mit dem Cyclin Y/14-3-3-Komplex in Kontakt treten kann. In manchen Fällen könnten die Marken sogar 14-3-3 direkt an CDK16 anziehen, den Zugang zu Cyclin Y blockieren oder jene regulatorischen Stellen vor einer Rücksetzung schützen. Auf diese Weise nutzen Zellen offenbar ein geschichtetes Kontrollschema, bei dem sowohl Cyclin Y als auch CDK16 die richtigen Phosphatmarken tragen müssen, bevor ein vollständig aktiver Komplex entstehen kann.
Welche Bedeutung das für Gesundheit und Krankheit hat
Indem die Dreifachinteraktion zwischen CDK16, Cyclin Y und 14-3-3 auf molekularer Ebene beschrieben wird, erklärt diese Arbeit, warum CDK16 ohne seine Helfer nicht eingeschaltet wird und wie ihre Interaktion das Enzym in seine aktive Form schiebt. Für Nicht-Fachleute lautet die Kernaussage: CDK16 ist kein einzelner Schalter, sondern Teil eines sorgfältig verkabelten Sicherheitskreises, der von mehreren Protein-Kontakten und chemischen Markierungen abhängt. Da CDK16 zum Überleben von Krebszellen und zu deren Resistenz gegen Therapien beiträgt, bieten die neu entdeckten Kontaktflächen konkrete Angriffspunkte, an denen künftige Medikamente eingreifen könnten, um den Komplex gezielt zu stören und so die Aktivität von CDK16 selektiv zu dämpfen, während verwandte Enzyme weniger betroffen bleiben.
Zitation: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Schlüsselwörter: CDK16, cyclin Y, 14-3-3-Proteine, Protein-Komplexe, Krebs-Signalgebung