Clear Sky Science · ja
CDK16の活性化を仲介するサイクリンY/14-3-3タンパク質の構造基盤
なぜこのタンパク質の謎が重要なのか
細胞内ではタンパク質のチームが小さな機械のように協働し、成長、生存、ストレスへの応答を制御しています。CDK16と呼ばれるタンパク質は、神経の配線、細胞内成分のリサイクル、受精能、そしてがん細胞の挙動に影響します。しかしCDK16は、特定の二つの補助タンパク質、サイクリンYと14-3-3が適切に揃わないとほとんど活動しません。本研究は、その特殊な三者が原子レベルでどのように組み合わさり、握手によってCDK16を待機状態から活性状態へ切り替えるかを明らかにし、この制御系を標的とする将来のがん治療薬設計への手がかりを提供します。
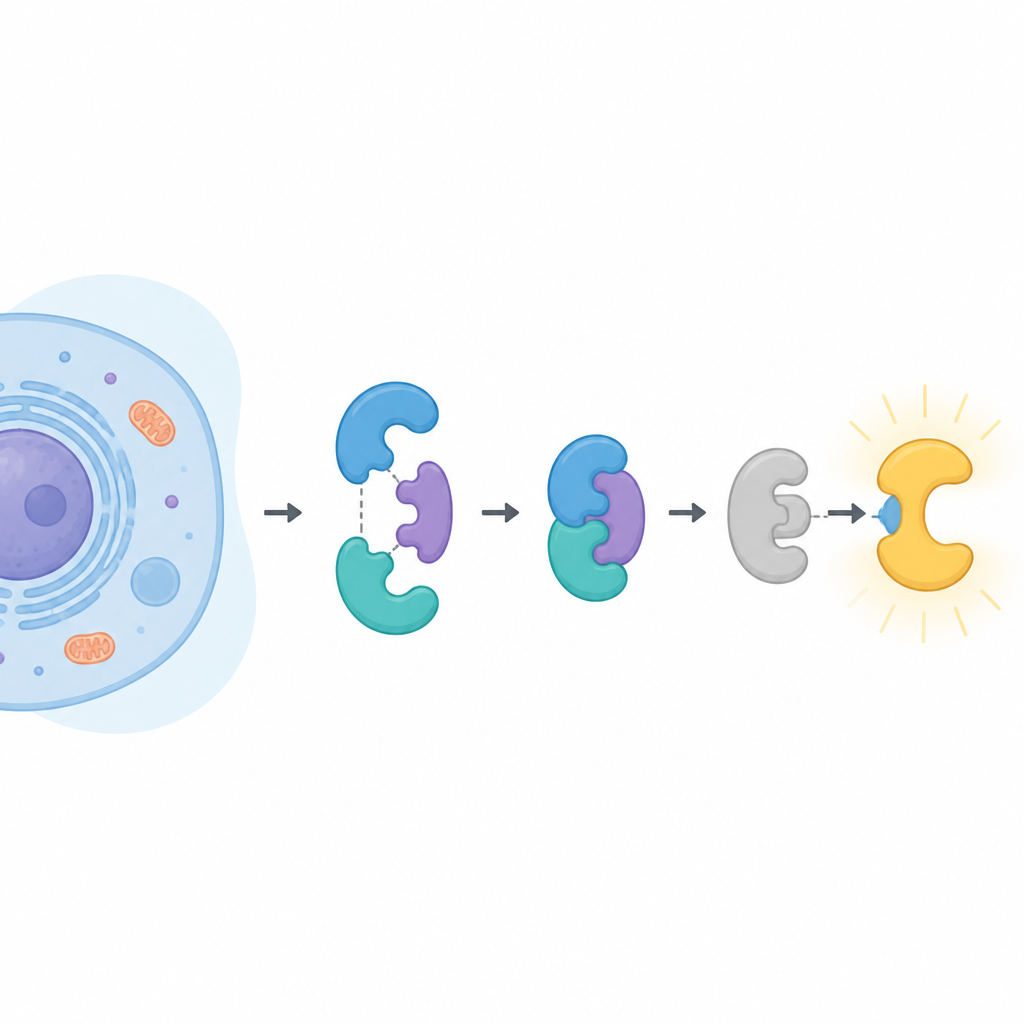
細胞内の主要な担い手
CDK16は他のタンパク質に小さなリン酸タグを付加してその活性を変える酵素ファミリーに属します。多くの同族は単にサイクリンというパートナーと結合するだけで活性化されますが、CDK16は異なります。CDK16はサイクリンYに結合したときにしか目覚めず、サイクリンY自体はリン酸化され、さらに14-3-3と呼ばれる別のタンパク質対によって保持される必要があります。CDK16は脳の発達、精子形成の最終段階、飢餓時の自己貪食(オートファジー)、およびいくつかのがんの増殖や薬剤耐性に関連してきました。CDK16がどのように制御されるかを正確に理解することは、正常な生理学と疾病の両方の解明につながります。
補助ペアがサイクリンYをどう変形させるか
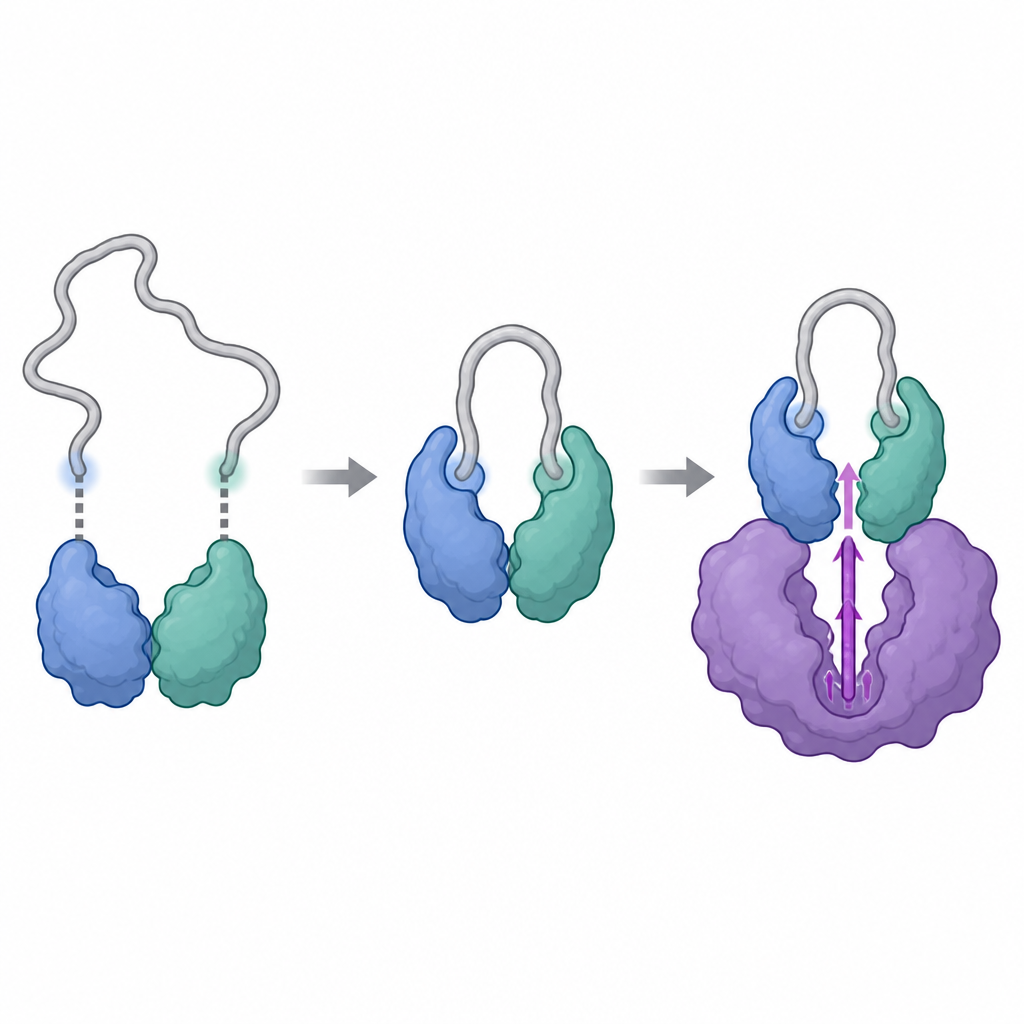
研究者たちはクライオ電子顕微鏡や、タンパク質中の水素原子が重水と交換する様子を追う手法などの強力な構造解析ツールを用いて、CDK16の有無でのサイクリンYと14-3-3による複合体を可視化しました。その結果、サイクリンYには14-3-3のそれぞれの半分に一つずつはまる二つの特異的部位があり、ちょうどボタンが留め具に掛かるように作用することが分かりました。両方の部位がリン酸化されて結合すると、14-3-3はサイクリンYをしっかり掴み、重要な表面領域を微妙に再形成します。この再形成により、後にCDK16と相互作用する領域が露出して硬くなり、サイクリンYは単独の場合よりもCDK16の受け入れ側として適した形になります。
CDK16はどうやってスイッチオンされるか
サイクリンYが14-3-3によって適切に保持されると、CDK16が結合して複合体が完成します。構造スナップショットは、CDK16がサイクリンYを抱き込むように二つの主要な接触領域を持つことを示しています:他のサイクリン依存性酵素で見られる典型的なドッキング部位に似た中央領域と、このサブファミリー特有の前方に伸びる柔軟な尾部です。CDK16が結合すると、この遊走する尾部が折り畳まれてサイクリンYに寄り添い、複合体をしっかり固定するのに寄与します。同時に、化学的中心付近にある可動セグメントである活性化ループが秩序化され、「オン」状態に保持されます。この保持はサイクリンYと14-3-3の末端の双方からの直接的な接触によって実現します。これらの界面の重要なアミノ酸を変異させると複合体が弱まり、CDK16の活性が著しく低下するため、これらの構造的接触が酵素をオンにするために不可欠であることが確認されました。
制御スイッチの微調整
研究はまた、CDK16自身がその前端の尾部に付く追加のリン酸タグによってどのように調節されうるかも示しています。以前の研究では、この尾部の特定部位がサイクリンYの結合に影響することが知られていました。新しい構造と動的データは、これらのタグの付加・除去が尾部の折り畳み方を変え、サイクリンYおよび14-3-3複合体と関与できるかどうかを左右することを示唆します。場合によっては、そのタグが14-3-3を直接CDK16に呼び寄せ、サイクリンYへのアクセスを遮るか、あるいは調節部位がリセットされるのを防ぐ可能性もあります。このように、細胞はサイクリンYとCDK16の双方が適切なリン酸化状態を持つことを必要とする多層的な制御スキームを用いて、完全に活性な複合体の形成を厳密に管理しているようです。
健康と疾患への示唆
CDK16、サイクリンY、14-3-3の三者による抱擁を分子レベルで示すことにより、本研究はなぜCDK16が補助因子なしでは活性化されないのか、そしてそれらの相互作用がどのように酵素を活性型へと押し込むのかを説明します。非専門家向けの要点は、CDK16が単独のスイッチではなく、複数のタンパク質接触と化学的タグに依存した精巧な安全回路の一部であるということです。CDK16ががん細胞の生存や治療抵抗性に寄与するため、今回明らかになった接触面は将来の薬剤が複合体を分断してCDK16の活性を選択的に抑える際の具体的な標的を提供する可能性があります。
引用: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
キーワード: CDK16, サイクリンY, 14-3-3タンパク質, タンパク質複合体, がんシグナル伝達