Clear Sky Science · pt
Base estrutural da ativação de CDK16 mediada por ciclina Y/proteína 14-3-3
Por que esse quebra-cabeça proteico importa
Dentro de nossas células, equipes de proteínas trabalham em conjunto como pequenas máquinas para controlar crescimento, sobrevivência e até a resposta ao estresse. Uma dessas proteínas, chamada CDK16, influencia o emaranhamento de neurônios, a reciclagem do conteúdo celular, a fertilidade e o comportamento de células cancerosas. Ainda assim, a CDK16 fica estranhamente inativa a menos que duas proteínas auxiliares específicas, ciclina Y e 14-3-3, se reúnam da maneira certa. Este estudo revela, átomo por átomo, como esse trio incomum se monta e como seu aperto de mãos transforma a CDK16 de ociosa em ativa, oferecendo novas pistas para o desenvolvimento de futuros fármacos contra o câncer que visem esse sistema de controle.
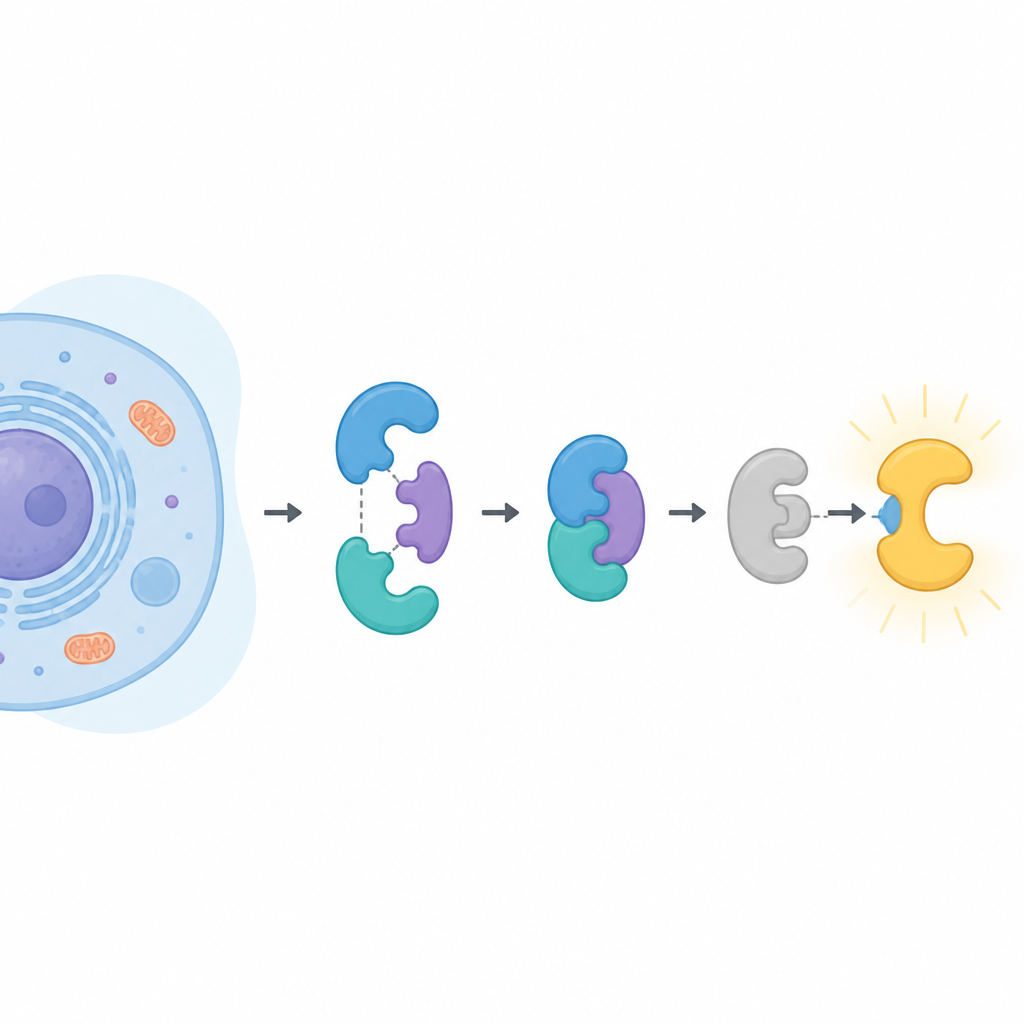
Os protagonistas dentro da célula
A CDK16 pertence a uma grande família de enzimas que adicionam pequenos rótulos de fosfato a outras proteínas, alterando sua atividade. A maioria de seus parentes é ativada simplesmente pela ligação a uma parceira chamada ciclina. A CDK16 é diferente. Ela só desperta quando ligada à ciclina Y, que por sua vez precisa ser decorada com marcas de fosfato e mantida no lugar por um par de proteínas conhecido como 14-3-3. A CDK16 tem sido associada ao desenvolvimento cerebral, às fases finais da formação do espermatozoide, à forma como as células recicl am seu conteúdo durante a privação de nutrientes e ao crescimento e resistência a medicamentos em vários cânceres. Compreender exatamente como a CDK16 é controlada pode, portanto, iluminar tanto a biologia normal quanto a doença.
Como o par auxiliar remodela a ciclina Y
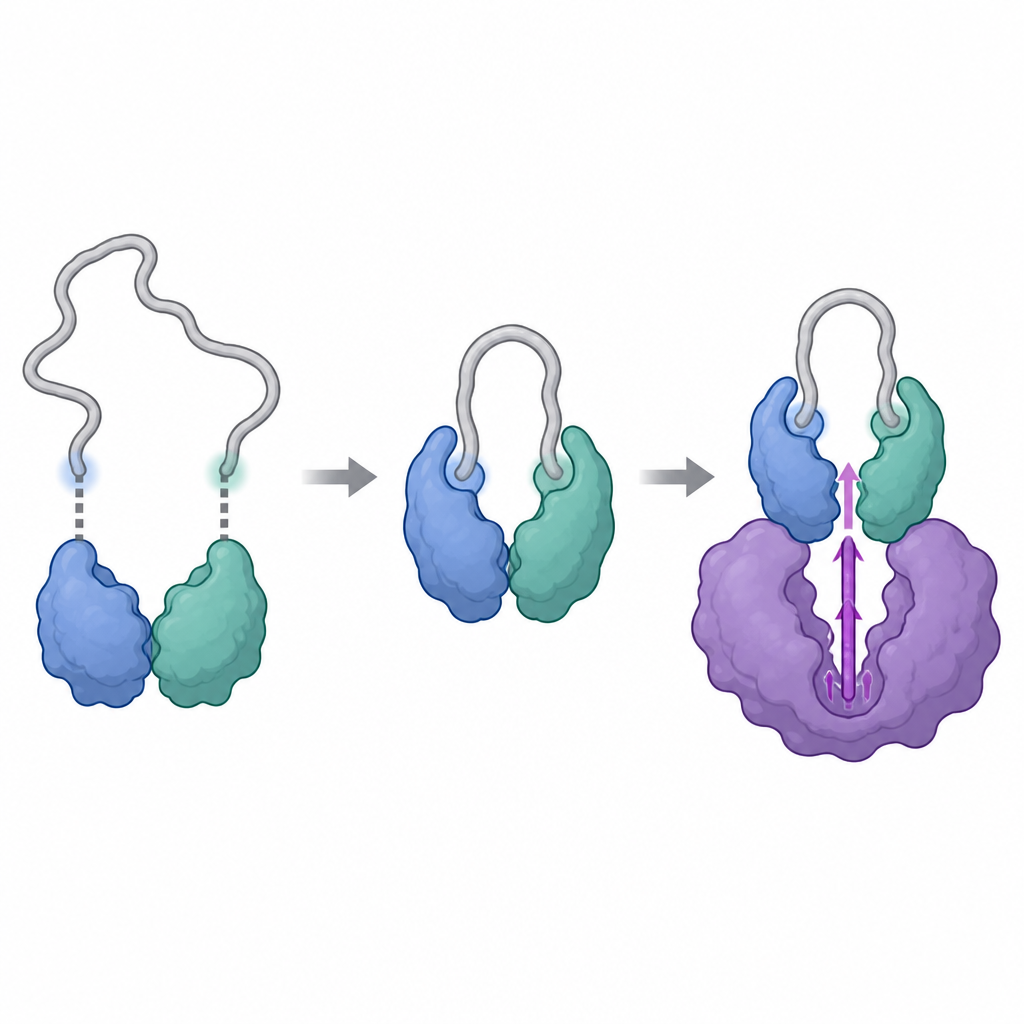
Os pesquisadores usaram poderosas ferramentas estruturais, incluindo criomicroscopia eletrônica e uma técnica que rastreia como átomos de hidrogênio em uma proteína trocam com água pesada, para visualizar os complexos formados pela ciclina Y e 14-3-3, com e sem CDK16. Eles descobriram que a ciclina Y carrega dois pontos específicos que podem se ligar cada um a uma metade do par 14-3-3, como dois botões encaixando em um fecho. Quando ambos os pontos são fosforilados e engajados, a 14-3-3 prende a ciclina Y e remodela sutilmente uma região superficial crucial. Essa remodelagem expõe e torna mais rígida a área que mais tarde interagirá com a CDK16, transformando a ciclina Y em um parceiro de ancoragem mais adequado do que seria por si só.
Como a CDK16 é ligada
Uma vez que a ciclina Y é mantida corretamente pela 14-3-3, a CDK16 pode se ligar e completar a montagem. As imagens estruturais mostram que a CDK16 abraça a ciclina Y com duas zonas principais de contato: uma região central que se assemelha ao sítio de ancoragem típico visto em outras quinases dependentes de ciclina, e uma cauda extra e flexível na frente da CDK16 que é única desta subfamília. Quando a CDK16 se liga, essa cauda flácida se dobra e se acolhe contra a ciclina Y, ajudando a travar o complexo. Ao mesmo tempo, o laço de ativação da CDK16, um segmento móvel próximo ao seu centro químico, torna-se ordenado e mantido em uma posição de "ligado" por contatos diretos tanto da ciclina Y quanto da extremidade do par 14-3-3. Mutar aminoácidos-chave nessas interfaces enfraquece o complexo e reduz drasticamente a atividade da CDK16, confirmando que esses contatos estruturais são essenciais para ativar a enzima.
Ajustando finamente o interruptor de controle
O estudo também revela como a própria CDK16 pode ser ajustada por marcas adicionais de fosfato em sua própria cauda dianteira. Em trabalhos anteriores, certos sítios nessa cauda eram conhecidos por afetar o quão bem a ciclina Y se liga. Os novos dados estruturais e dinâmicos sugerem que adicionar ou remover essas marcas pode alterar como a cauda se dobra e se ela consegue interagir com o complexo ciclina Y–14-3-3. Em alguns casos, as marcas podem até recrutar a 14-3-3 diretamente para a CDK16, bloqueando o acesso à ciclina Y ou protegendo esses sítios regulatórios de serem redefinidos. Dessa forma, as células parecem usar um esquema de controle em camadas no qual tanto a ciclina Y quanto a CDK16 devem carregar as marcas de fosfato corretas antes que um complexo totalmente ativo possa se formar.
O que isso significa para saúde e doença
Ao detalhar o abraço triplo entre CDK16, ciclina Y e 14-3-3 em nível molecular, este trabalho explica por que a CDK16 se recusa a ligar sem seus auxiliares e como essa interação empurra a enzima para sua forma ativa. Para não especialistas, a conclusão é que a CDK16 não é um interruptor solitário, mas parte de um circuito de segurança cuidadosamente ligado que depende de múltiplos contatos proteicos e marcas químicas. Como a CDK16 contribui para a sobrevivência de células cancerosas e resistência a tratamentos, as superfícies de contato agora reveladas oferecem alvos específicos onde futuros fármacos podem se inserir e interromper o complexo, diminuindo seletivamente a atividade da CDK16 enquanto deixam enzimas relacionadas menos afetadas.
Citação: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Palavras-chave: CDK16, ciclina Y, proteínas 14-3-3, complexos proteicos, sinalização do câncer