Clear Sky Science · ru
Структурная основа активации CDK16, опосредованной циклином Y и белком 14-3-3
Почему эта белковая головоломка важна
Внутри наших клеток команды белков работают как миниатюрные машины, контролируя рост, выживание и реакцию на стресс. Один из таких белков, CDK16, влияет на формирование нервных связей, процессы утилизации клеточного содержимого, фертильность и поведение раковых клеток. При этом CDK16 по‑настоящему «просыпается» только тогда, когда два определённых вспомогательных белка — циклин Y и 14-3-3 — собираются вместе в нужной конфигурации. В этом исследовании показано на атомном уровне, как собирается эта нетипичная тройка и как их «рукопожатие» переводит CDK16 из неактивного в активное состояние, что даёт новые подсказки для разработки противораковых препаратов, нацеленных на эту систему контроля.
Ключевые участники в клетке
CDK16 относится к большому семейству ферментов, которые присоединяют маленькие фосфатные метки к другим белкам, изменяя их активность. Большинство его родственников включаются просто при связывании с партнёром, называемым циклином. CDK16 отличается: он активируется только в комплексе с циклином Y, который сам должен быть фосфорилирован и зафиксирован другой парой белков — 14-3-3. CDK16 ассоциирован с развитием мозга, завершающей стадией образования сперматозоидов, аутофагией при голодании, а также с ростом и лекарственной устойчивостью ряда опухолей. Понимание точного механизма контроля CDK16 может пролить свет как на нормальную биологию, так и на заболевания.
Как пара помощников перестраивает циклин Y
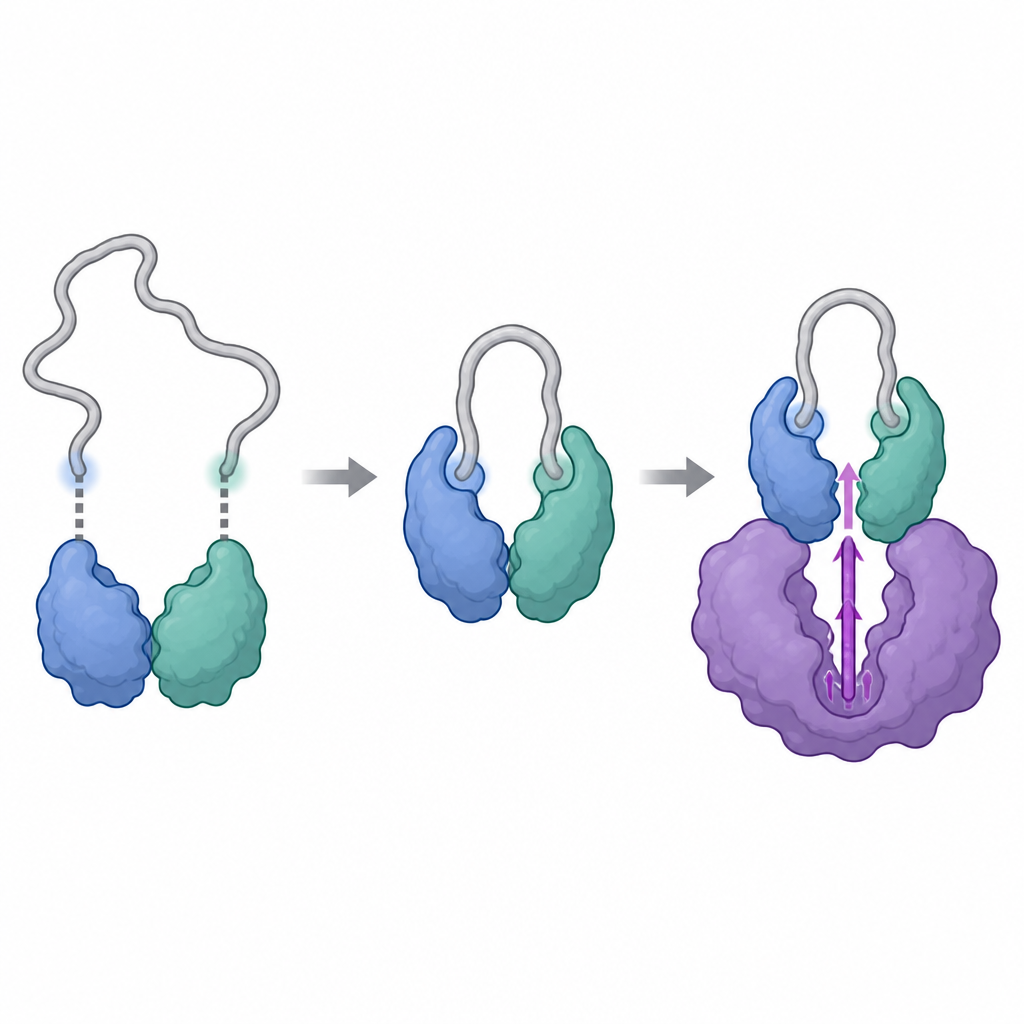
Исследователи использовали мощные структурные методы, включая крио‑электронную микроскопию и гидроген–дейтерий обмен для слежения за подвижностью участков белка, чтобы визуализировать комплексы циклина Y и 14-3-3 в присутствии и без CDK16. Они обнаружили, что циклин Y имеет две специфические позиции, каждая из которых может сцепляться с одной из половинок димера 14-3-3, как две пуговицы в застёжке. Когда обе позиции фосфорилированы и заняты, 14-3-3 захватывает циклин Y и тонко перестраивает критическую поверхностную область. Эта перестройка открывает и уплотняет участок, который впоследствии будет взаимодействовать с CDK16, делая циклин Y более подходящим докинг‑партнёром, чем он был бы сам по себе.
Как CDK16 включается
После того как циклин Y надёжно зафиксирован 14-3-3, CDK16 может присоединиться и завершить сборку комплекса. Структурные снимки показывают, что CDK16 контактирует с циклином Y через две основные зоны: центральную область, напоминающую типичную посадочную площадку, наблюдаемую у других циклин‑зависимых киназ, и дополнительный гибкий хвост спереди CDK16, уникальный для этого подсемейства. При связывании этот подвижный хвост складывается и прижимается к циклину Y, способствуя стабилизации комплекса. Одновременно активационная петля CDK16, подвижный сегмент около его каталитического центра, упорядочивается и фиксируется в «включённом» положении за счёт прямых контактов как с циклином Y, так и с концом димера 14-3-3. Мутации ключевых аминокислот в этих интерфейсах ослабляют комплекс и резко снижают активность CDK16, что подтверждает жизненно важную роль этих структурных контактов для активации фермента.
Тонкая настройка переключателя
Работа также показывает, как сам CDK16 может подвергаться дополнительной регулировке фосфатными метками на его переднем хвосте. В предыдущих исследованиях некоторые сайты в этом хвосте уже связывались с изменением афинности к циклину Y. Новые структурные и динамические данные указывают, что добавление или снятие этих меток может менять свёртывание хвоста и его способность взаимодействовать с комплексом циклин Y–14-3-3. В некоторых случаях эти метки могут даже напрямую привлекать 14-3-3 к CDK16, блокируя доступ циклина Y или защищая регуляторные сайты от перерафсъёма. Таким образом, клетки, по‑видимому, используют многоуровневую схему контроля, в которой и циклин Y, и CDK16 должны нести правильные фосфорные метки прежде, чем сформируется полностью активный комплекс.
Что это значит для здоровья и болезни
Показав трёхстороннее взаимодействие между CDK16, циклином Y и 14-3-3 в молекулярных деталях, эта работа объясняет, почему CDK16 отказывается включаться без своих помощников и как их взаимодействие подталкивает фермент в активную форму. Для неспециалистов вывод таков: CDK16 — не одиночный переключатель, а часть тщательно сработанной предохранительной схемы, зависящей от множества белковых контактов и химических меток. Поскольку CDK16 способствует выживанию раковых клеток и их устойчивости к терапии, недавно выявленные контактные поверхности предлагают конкретные мишени, куда будущие препараты могли бы вмешаться, разрушая комплекс и селективно подавляя активность CDK16, при этом в меньшей степени затрагивая родственные ферменты.
Цитирование: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Ключевые слова: CDK16, циклин Y, белки 14-3-3, белковые комплексы, онкосигналинг