Clear Sky Science · pl
Strukturalne podstawy aktywacji CDK16 pośredniczonej przez cyklinę Y i białko 14-3-3
Dlaczego ta zagadka białkowa ma znaczenie
W naszych komórkach zespoły białek współdziałają niczym maleńkie maszyny kontrolujące wzrost, przetrwanie i reakcje na stres. Jedno z tych białek, CDK16, wpływa na okablowanie komórek nerwowych, recykling zawartości komórkowej, płodność oraz zachowanie komórek nowotworowych. Jednak CDK16 pozostaje z reguły nieaktywny, dopóki dwie specyficzne białka pomocnicze — cyklina Y i 14-3-3 — nie połączą się w odpowiedni sposób. W niniejszym badaniu pokazano, atom po atomie, jak ten nietypowy tercet się składa i jak ich „uścisk dłoni” przełącza CDK16 ze stanu spoczynku na aktywny, dostarczając nowych wskazówek do projektowania leków przeciwnowotworowych celujących w ten system kontroli.
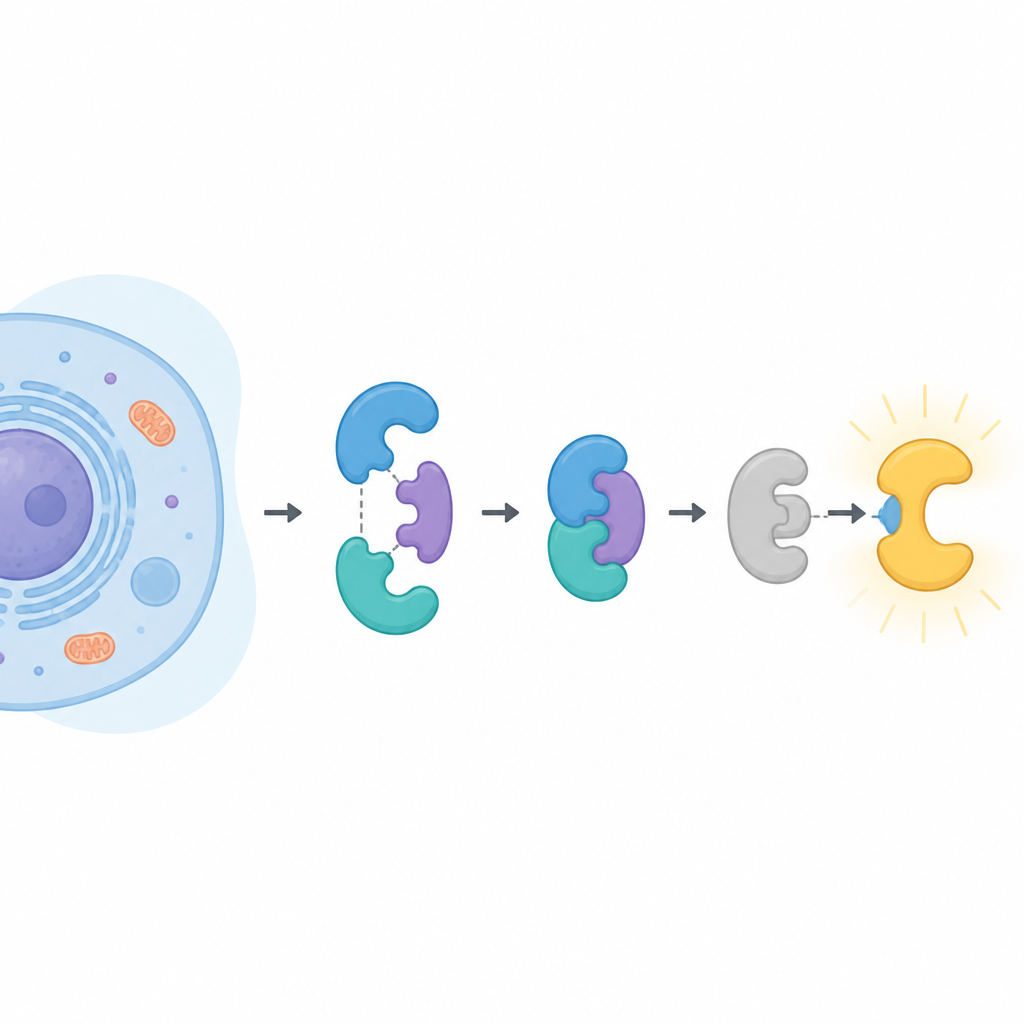
Główni gracze w komórce
CDK16 należy do dużej rodziny enzymów dokujących reszty fosforanowej do innych białek, zmieniając ich aktywność. Większość jego krewnych uruchamia się po prostu przez związanie z partnerem zwanym cykliną. CDK16 jest inny. Budzi się dopiero po związaniu z cykliną Y, która sama musi być oznaczona resztami fosforanowymi i utrzymywana przez parę białek 14-3-3. CDK16 powiązano z rozwojem mózgu, końcowymi etapami tworzenia plemników, sposobem recyklingu komórkowego podczas głodzenia oraz wzrostem i opornością na leki w kilku nowotworach. Dokładne zrozumienie kontroli CDK16 może więc rozjaśnić zarówno prawidłową biologię, jak i chorobę.
Jak para pomocnicza przeformowuje cyklinę Y
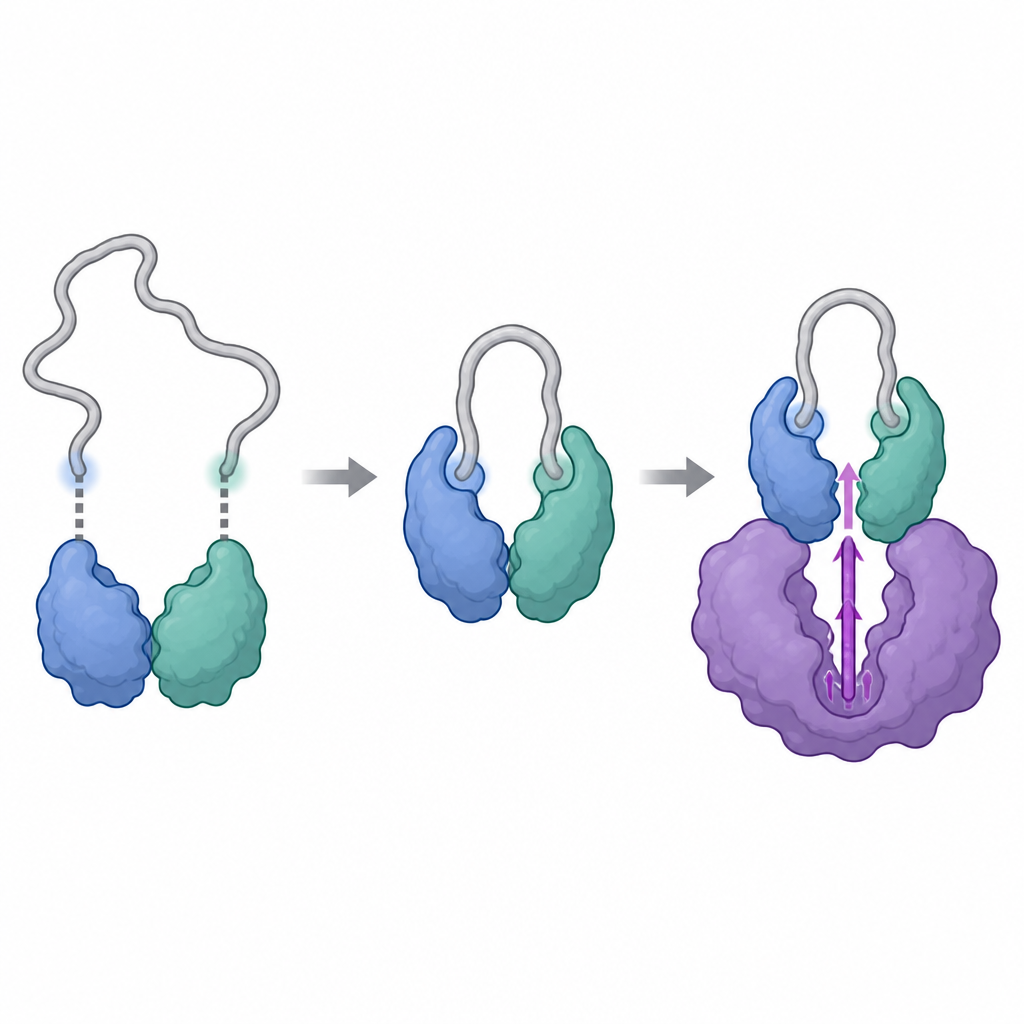
Naukowcy użyli zaawansowanych narzędzi strukturalnych, w tym krioelektronowego mikroskopu oraz techniki śledzącej wymianę atomów wodoru na ciężką wodę, aby zobrazować kompleksy tworzone przez cyklinę Y i 14-3-3, z CDK16 i bez niego. Stwierdzili, że cyklina Y ma dwa specyficzne miejsca, z których każde może zaczepić jedną połówkę pary 14-3-3, niczym dwa guziki wpadające w zapięcie. Gdy oba miejsca są ufosforylowane i zaangażowane, 14-3-3 chwytają cyklinę Y i subtelnie przekształcają kluczowy obszar powierzchniowy. To przeformowanie odsłania i usztywnia region, który później będzie współdziałał z CDK16, czyniąc cyklinę Y lepszym miejscem dokowania niż w stanie wolnym.
Jak CDK16 zostaje włączony
Gdy cyklina Y jest prawidłowo utrzymana przez 14-3-3, CDK16 może się związać i zakończyć składanie kompleksu. Migawki strukturalne pokazują, że CDK16 obejmuje cyklinę Y dwiema głównymi strefami kontaktu: centralnym obszarem przypominającym typowe miejsce dokowania obserwowane w innych kinazach zależnych od cyklin oraz dodatkowym, elastycznym ogonem z przodu CDK16, unikalnym dla tej podrodziny. Po związaniu ten wiotki ogon składa się i przytula do cykliny Y, pomagając zablokować kompleks. Równocześnie pętla aktywacyjna CDK16, ruchomy segment blisko centrum chemicznego, porządkuje się i jest utrzymywana w pozycji „włączonej” przez bezpośrednie kontakty zarówno z cykliną Y, jak i końcem pary 14-3-3. Mutacje kluczowych aminokwasów na tych interfejsach osłabiają kompleks i znacznie zmniejszają aktywność CDK16, potwierdzając, że te strukturalne kontakty są niezbędne do uruchomienia enzymu.
Dostrajanie przełącznika kontroli
Badanie ujawnia również, jak sam CDK16 może być regulowany przez dodatkowe reszty fosforanowe na jego własnym przednim ogonie. We wcześniejszych pracach pewne miejsca w tym ogonie wpływały na siłę wiązania cykliny Y. Nowe dane strukturalne i dynamiczne sugerują, że dodanie lub usunięcie tych znaczników może zmieniać sposób, w jaki ogon się składa i czy może nawiązać kontakt z kompleksem cyklina Y–14-3-3. W niektórych przypadkach znaczniki te mogą nawet rekrutować 14-3-3 bezpośrednio do CDK16, blokując dostęp do cykliny Y lub osłaniając te regulatoryczne miejsca przed zmianą. W ten sposób komórki wydają się stosować wielowarstwowy schemat kontroli, w którym zarówno cyklina Y, jak i CDK16 muszą nosić właściwe znaki fosforanowe, zanim utworzy się w pełni aktywny kompleks.
Co to znaczy dla zdrowia i chorób
Ukazując trójstronny uścisk między CDK16, cykliną Y i 14-3-3 w detalach molekularnych, praca ta wyjaśnia, dlaczego CDK16 nie włącza się bez swoich pomocników i jak ich interakcja popycha enzym do aktywnej formy. Dla czytelników niebędących specjalistami kluczowa konkluzja brzmi: CDK16 nie jest pojedynczym przełącznikiem, lecz częścią starannie zaprojektowanego obwodu zabezpieczającego, zależnego od wielu kontaktów białkowych i chemicznych znaczników. Ponieważ CDK16 przyczynia się do przetrwania komórek nowotworowych i oporności na leczenie, nowo ujawnione powierzchnie kontaktu stanowią konkretne cele, gdzie przyszłe leki mogłyby się wkleić i rozbić kompleks, selektywnie przygaszając aktywność CDK16, pozostawiając przy tym spokrewnione enzymy mniej dotknięte.
Cytowanie: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Słowa kluczowe: CDK16, cyklina Y, białka 14-3-3, kompleksy białkowe, sygnalizacja w nowotworach