Clear Sky Science · es
Base estructural de la activación de CDK16 mediada por ciclina Y/proteínas 14-3-3
Por qué importa este rompecabezas proteico
Dentro de nuestras células, equipos de proteínas actúan como pequeñas máquinas para controlar el crecimiento, la supervivencia e incluso la respuesta al estrés. Una de estas proteínas, llamada CDK16, influye en el cableado de las neuronas, el reciclado de contenidos celulares, la fertilidad y el comportamiento de las células cancerosas. Sin embargo, CDK16 permanece inactivo a menos que se junten de la manera precisa dos proteínas auxiliares específicas: la ciclina Y y las 14-3-3. Este estudio revela, átomo por átomo, cómo se ensambla ese trío inusual y cómo su interacción cambia a CDK16 de reposo a activo, ofreciendo nuevas pistas para diseñar futuros fármacos contra el cáncer que apunten a este sistema de control.
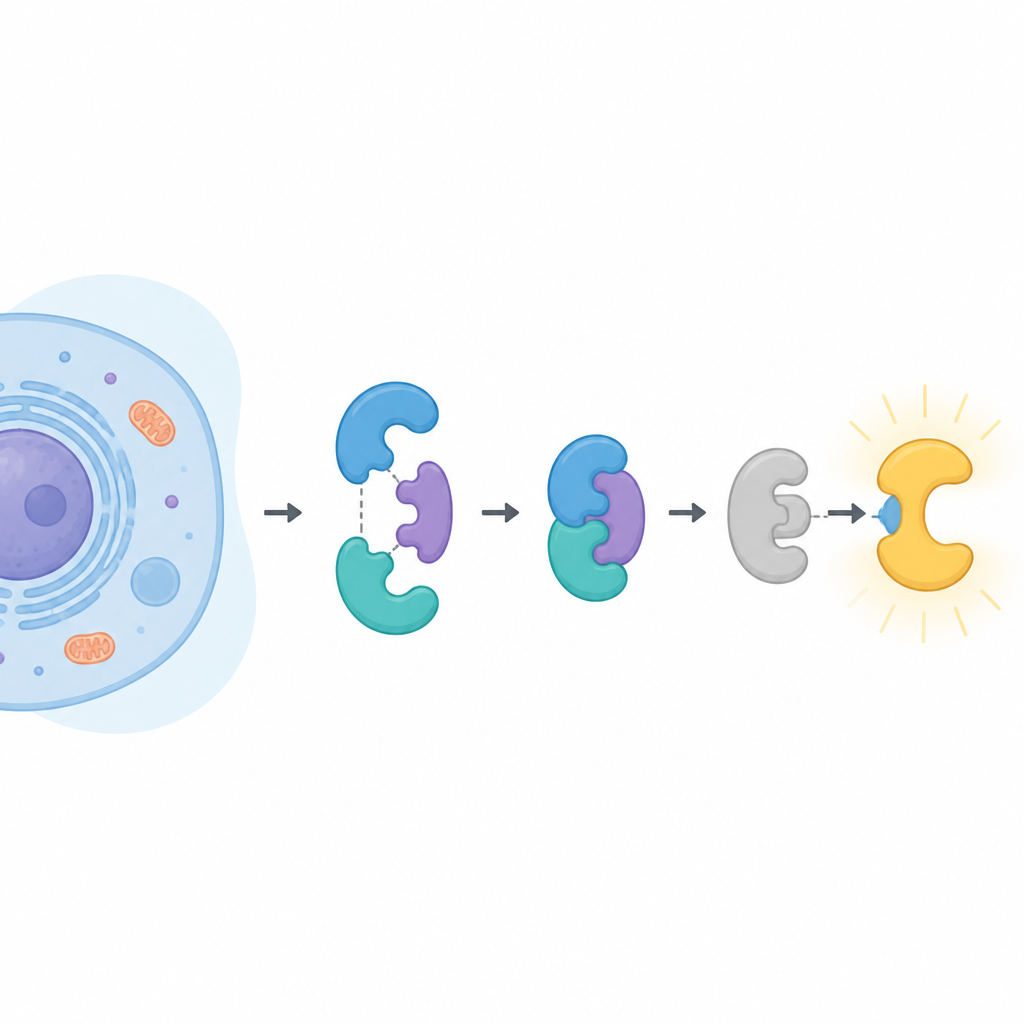
Los protagonistas en la célula
CDK16 pertenece a una amplia familia de enzimas que añaden pequeñas etiquetas de fosfato a otras proteínas, modificando su actividad. La mayoría de sus parientes se activan simplemente al unirse a una pareja llamada ciclina. CDK16 es distinto. Solo se despierta al unirse a la ciclina Y, que a su vez debe llevar marcas de fosfato y ser mantenida en su lugar por otra pareja proteica conocida como 14-3-3. CDK16 se ha vinculado al desarrollo cerebral, las etapas finales de la formación de espermatozoides, la forma en que las células reciclan sus propios contenidos durante la carencia de nutrientes, y al crecimiento y la resistencia a fármacos en varios cánceres. Comprender exactamente cómo se controla CDK16 puede iluminar tanto la biología normal como la enfermedad.
Cómo la pareja auxiliar remodela la ciclina Y
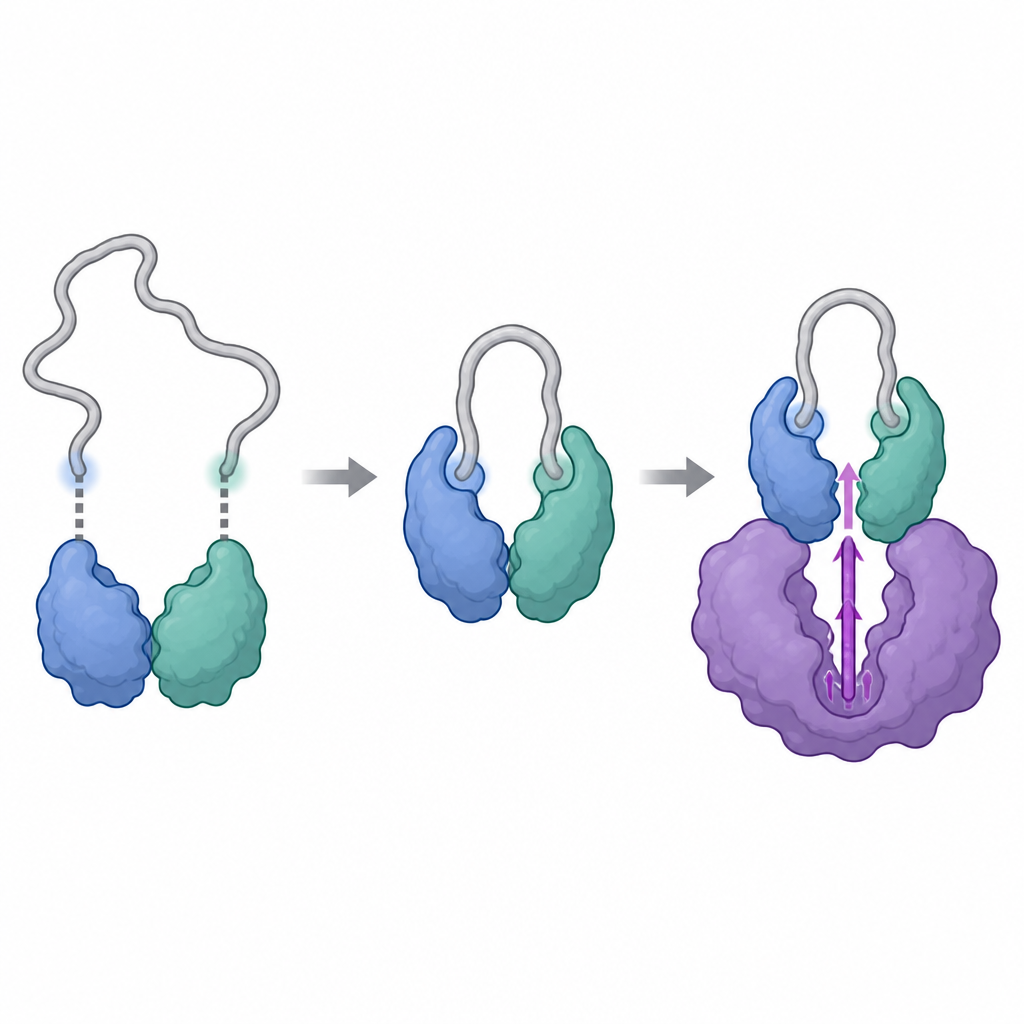
Los investigadores utilizaron potentes herramientas estructurales, incluyendo criomicroscopía electrónica y una técnica que sigue cómo los átomos de hidrógeno en una proteína intercambian con agua pesada, para visualizar los complejos formados por la ciclina Y y 14-3-3, con y sin CDK16. Encontraron que la ciclina Y tiene dos sitios específicos que pueden anclarse cada uno a una mitad del dímero 14-3-3, como dos botones que se enganchan en un broche. Cuando ambos sitios están fosforilados y comprometidos, 14-3-3 agarra la ciclina Y y remodela sutilmente una región superficial crucial. Esta remodelación expone y rigidiza la zona que más tarde interactuará con CDK16, convirtiendo a la ciclina Y en un receptor de acoplamiento más adecuado que cuando está sola.
Cómo se enciende CDK16
Una vez que la ciclina Y está correctamente retenida por 14-3-3, CDK16 puede unirse y completar el ensamblaje. Las instantáneas estructurales muestran que CDK16 abraza a la ciclina Y con dos zonas de contacto principales: una región central que se parece al sitio de acoplamiento típico observado en otras quinasas dependientes de ciclina, y una cola adicional y flexible en el frente de CDK16 que es única en esta subfamilia. Cuando CDK16 se une, esta cola flexible se pliega y se aposenta contra la ciclina Y, ayudando a fijar el complejo. Al mismo tiempo, el lazo de activación de CDK16, un segmento móvil cerca de su centro químico, se ordena y queda mantenido en una posición de "encendido" mediante contactos directos tanto de la ciclina Y como del extremo del dímero 14-3-3. Mutar aminoácidos clave en estas interfaces debilita el complejo y reduce drásticamente la actividad de CDK16, confirmando que estos contactos estructurales son esenciales para activar la enzima.
Ajustar con precisión el interruptor de control
El estudio también revela cómo el propio CDK16 puede ajustarse mediante marcas de fosfato adicionales en su propia cola frontal. En trabajos anteriores, se sabía que ciertos sitios en esa cola afectan la afinidad de unión por la ciclina Y. Los nuevos datos estructurales y dinámicos sugieren que añadir o eliminar estas marcas puede alterar cómo se pliega la cola y si puede interactuar con el complejo ciclina Y/14-3-3. En algunos casos, las marcas podrían incluso reclutar directamente a 14-3-3 hacia CDK16, bloqueando el acceso a la ciclina Y o protegiendo esos sitios reguladores de ser reiniciados. De este modo, las células parecen emplear un esquema de control por capas en el que tanto la ciclina Y como CDK16 deben portar las marcas de fosfato adecuadas antes de que pueda formarse un complejo totalmente activo.
Qué significa esto para la salud y la enfermedad
Al describir el abrazo a tres entre CDK16, ciclina Y y 14-3-3 en detalle molecular, este trabajo explica por qué CDK16 se niega a activarse sin sus auxiliares y cómo su interacción empuja a la enzima hacia su forma activa. Para el público general, la conclusión es que CDK16 no es un interruptor solitario sino parte de un circuito de seguridad cuidadosamente cableado que depende de múltiples contactos proteicos y etiquetas químicas. Dado que CDK16 contribuye a la supervivencia de células cancerosas y a la resistencia a tratamientos, las superficies de contacto recién reveladas ofrecen objetivos concretos donde futuros fármacos podrían encajar y perturbar el complejo, atenuando selectivamente la actividad de CDK16 mientras dejan menos afectadas a enzimas relacionadas.
Cita: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Palabras clave: CDK16, ciclina Y, proteínas 14-3-3, complejos proteicos, señalización en el cáncer