Clear Sky Science · it
Basi strutturali dell’attivazione di CDK16 mediata da ciclina Y e dalla proteina 14-3-3
Perché questo rompicapo proteico è importante
All’interno delle nostre cellule, squadre di proteine collaborano come piccole macchine per controllare crescita, sopravvivenza e persino la risposta allo stress. Una di queste proteine, chiamata CDK16, influenza l’assetto dei neuroni, il riciclo del materiale cellulare, la fertilità e il comportamento delle cellule tumorali. Tuttavia CDK16 rimane stranamente inattiva a meno che due proteine ausiliarie specifiche, ciclina Y e 14-3-3, non si associno nel modo giusto. Questo studio rivela, atomo per atomo, come si assembla quella singolare terna e come la loro stretta trasforma CDK16 da inattivo ad attivo, offrendo nuovi indizi per progettare in futuro farmaci contro il cancro che prendano di mira questo sistema di controllo.
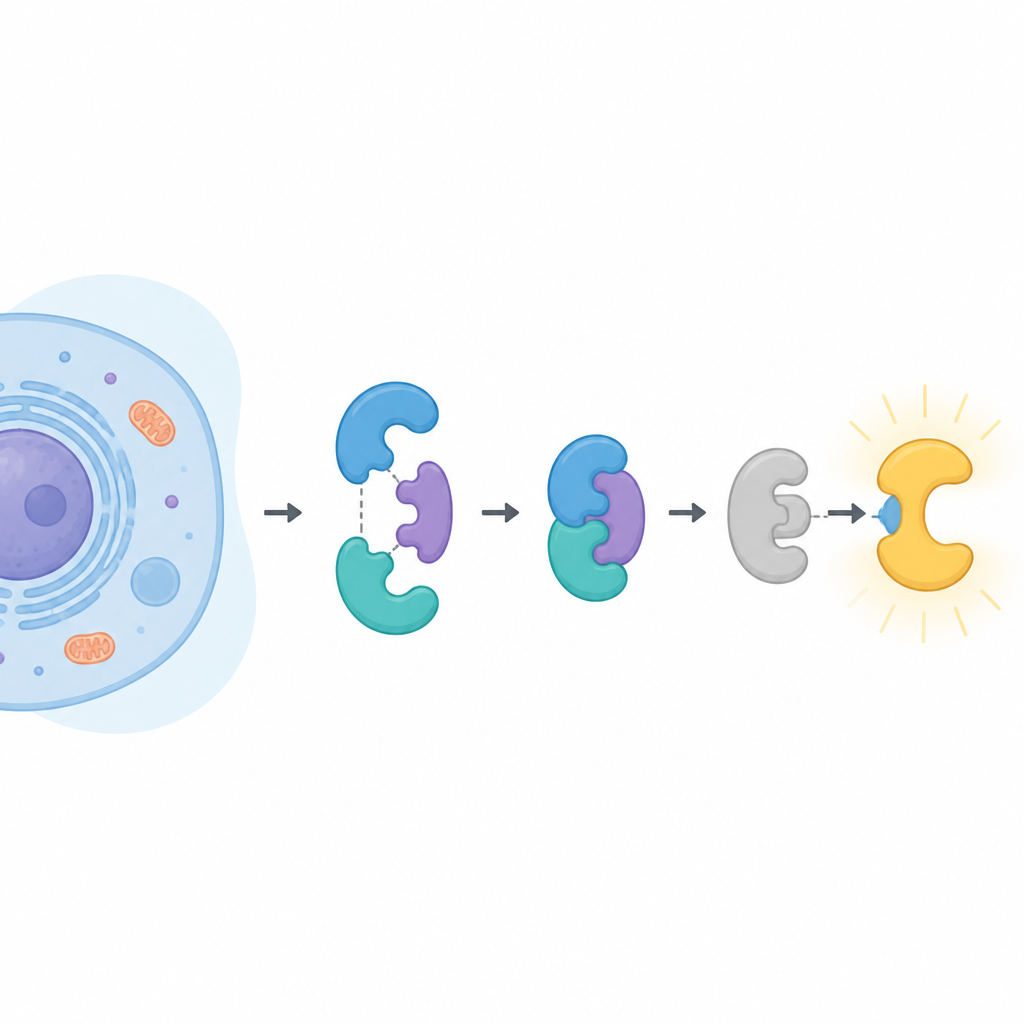
I protagonisti nella cellula
CDK16 appartiene a una grande famiglia di enzimi che aggiungono piccoli tag fosfato ad altre proteine, modificandone l’attività. La maggior parte dei suoi parenti si attiva semplicemente legandosi a un partner chiamato ciclina. CDK16 è diverso. Si risveglia solo quando è legato alla ciclina Y, che a sua volta deve essere decorata con gruppi fosfato e stabilizzata da una coppia proteica nota come 14-3-3. CDK16 è stato collegato allo sviluppo cerebrale, alle fasi finali della formazione degli spermatozoi, al modo in cui le cellule riciclano i propri componenti durante la fame e alla crescita e resistenza ai farmaci in diversi tumori. Capire esattamente come CDK16 sia regolato potrebbe quindi illuminare sia la biologia normale sia la malattia.
Come la coppia ausiliaria rimodella la ciclina Y
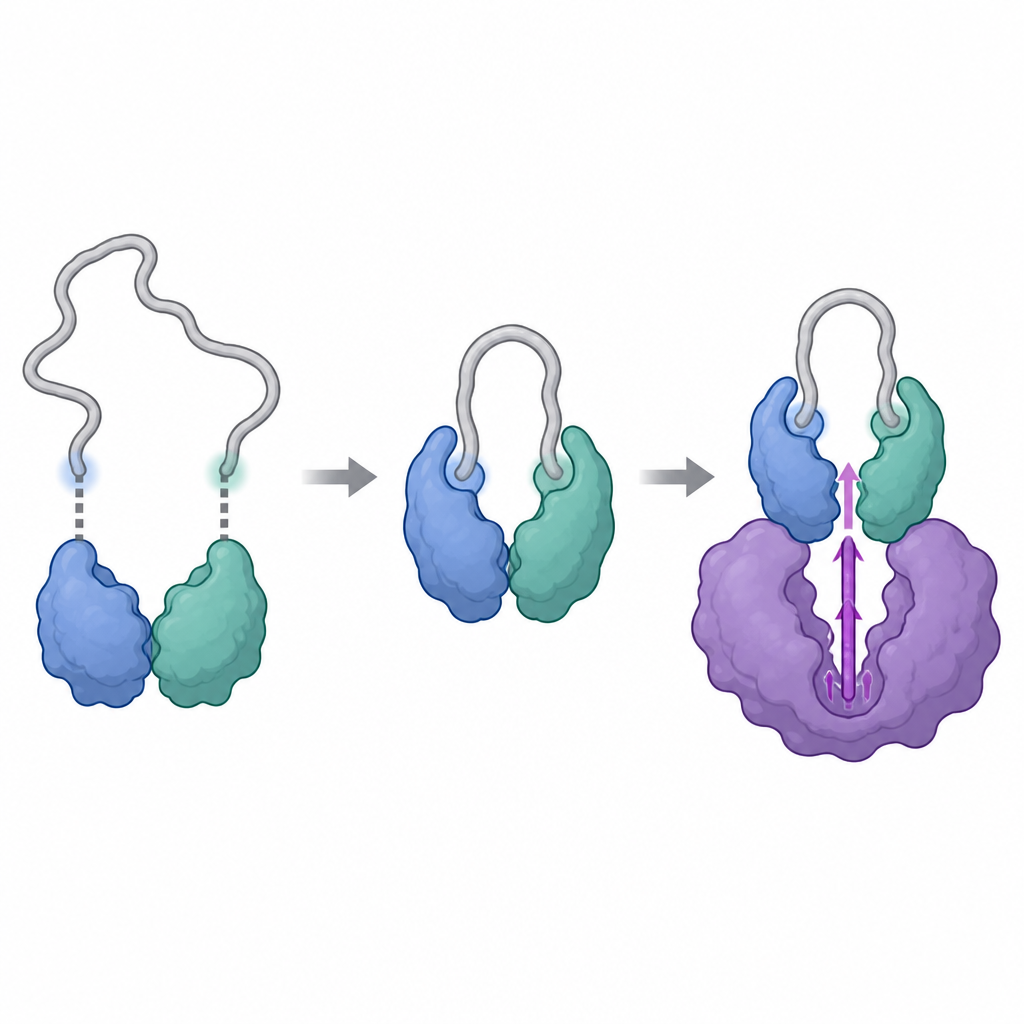
I ricercatori hanno usato potenti strumenti strutturali, tra cui la criomicroscopia elettronica e una tecnica che traccia come gli atomi di idrogeno in una proteina scambiano con acqua pesante, per visualizzare i complessi formati dalla ciclina Y e 14-3-3, con e senza CDK16. Hanno scoperto che la ciclina Y porta due siti specifici che possono ciascuno agganciarsi a una metà della coppia 14-3-3, come due bottoni che si inseriscono in una fibbia. Quando entrambi i siti sono fosforilati e impegnati, 14-3-3 afferra la ciclina Y e rimodella sottilmente una regione superficiale cruciale. Questo rimodellamento espone e irrigidisce l’area che in seguito interagirà con CDK16, trasformando la ciclina Y in un partner di aggancio più adatto rispetto a quando è da sola.
Come CDK16 viene acceso
Una volta che la ciclina Y è tenuta correttamente da 14-3-3, CDK16 può legarsi e completare l’assemblaggio. Gli istantanee strutturali mostrano che CDK16 abbraccia la ciclina Y con due zone di contatto principali: una regione centrale che somiglia al sito di aggancio tipico visto in altri enzimi dipendenti da ciclina, e una coda anteriore extra e flessibile di CDK16 che è unica per questa sottoclasse. Quando CDK16 si lega, questa coda floscia si ripiega e si appoggia contro la ciclina Y, aiutando a bloccare il complesso. Allo stesso tempo, il loop di attivazione di CDK16, un segmento mobile vicino al suo centro chimico, diventa ordinato e mantenuto in una posizione "on" tramite contatti diretti sia dalla ciclina Y sia dall’estremità della coppia 14-3-3. Mutazioni di aminoacidi chiave in queste interfacce indeboliscono il complesso e riducono drasticamente l’attività di CDK16, confermando che questi contatti strutturali sono essenziali per attivare l’enzima.
Regolazione fine dell’interruttore
Lo studio rivela anche come lo stesso CDK16 possa essere modulato da ulteriori gruppi fosfato sulla sua coda anteriore. In lavori precedenti, alcuni siti in questa coda erano noti per influenzare quanto bene la ciclina Y si lega. I nuovi dati strutturali e dinamici suggeriscono che aggiungere o rimuovere questi tag può modificare il modo in cui la coda si ripiega e se riesce a interagire con il complesso ciclina Y–14-3-3. In alcuni casi, i tag possono persino reclutare direttamente 14-3-3 su CDK16, bloccando l’accesso alla ciclina Y o proteggendo quei siti regolatori dal venire resettati. In questo modo, le cellule sembrano usare uno schema di controllo a strati in cui sia la ciclina Y sia CDK16 devono portare i corretti segni fosfato prima che un complesso pienamente attivo possa formarsi.
Cosa significa per salute e malattia
Stendendo la mappa dell’abbraccio a tre vie tra CDK16, ciclina Y e 14-3-3 in dettaglio molecolare, questo lavoro spiega perché CDK16 rifiuta di attivarsi senza i suoi aiutanti e come la loro interazione induca l’enzima nella sua forma attiva. Per i non specialisti, la conclusione è che CDK16 non è un interruttore solitario ma parte di un circuito di sicurezza attentamente cablato che dipende da molteplici contatti proteici e marcature chimiche. Poiché CDK16 contribuisce alla sopravvivenza delle cellule tumorali e alla resistenza ai trattamenti, le superfici di contatto appena rivelate offrono bersagli specifici dove futuri farmaci potrebbero insinuarsi e interrompere il complesso, attenuando selettivamente l’attività di CDK16 lasciando meno coinvolti gli enzimi correlati.
Citazione: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Parole chiave: CDK16, ciclina Y, proteine 14-3-3, complessi proteici, segnalazione nel cancro