Clear Sky Science · nl
Structurele basis van de activatie van CDK16 door cycline Y/14-3-3-eiwitten
Waarom deze eiwitpuzzel ertoe doet
Binnen onze cellen werken eiwitteams samen als kleine machines die groei, overleving en zelfs de reactie van cellen op stress regelen. Eén van die eiwitten, CDK16, beïnvloedt het leggen van neurale verbindingen, het recyclen van celmateriaal, vruchtbaarheid en het gedrag van kankercellen. Toch blijft CDK16 opmerkelijk stil tenzij twee specifieke helper-eiwitten, cycline Y en 14-3-3, op precies de juiste manier samenkomen. Deze studie onthult, atoom voor atoom, hoe dat ongewone trio zich assembleert en hoe hun handdruk CDK16 van stil naar actief schakelt, wat nieuwe aanwijzingen biedt voor het ontwerpen van toekomstige kankertherapieën die dit regelsysteem targeten.
De hoofdrolspelers in de cel
CDK16 behoort tot een grote familie van enzymen die kleine fosfaatlabels aan andere eiwitten toevoegen en daarmee hun activiteit veranderen. De meeste familieleden worden eenvoudigweg geactiveerd door te binden aan een partner die een cycline heet. CDK16 is anders. Het wordt alleen wakker wanneer het gebonden is aan cycline Y, die zelf gefosforyleerd moet zijn en op zijn plaats gehouden wordt door een ander eiwitpaar, de 14-3-3-eiwitten. CDK16 is in verband gebracht met hersenontwikkeling, de eindfasen van spermaproductie, de manier waarop cellen hun eigen materiaal recyclen tijdens uithongering, en de groei en medicijnresistentie van verschillende kankers. Precies begrijpen hoe CDK16 wordt gecontroleerd kan dus zowel normale biologie als ziekte verhelderen.
Hoe het helper-paar cycline Y hervormt
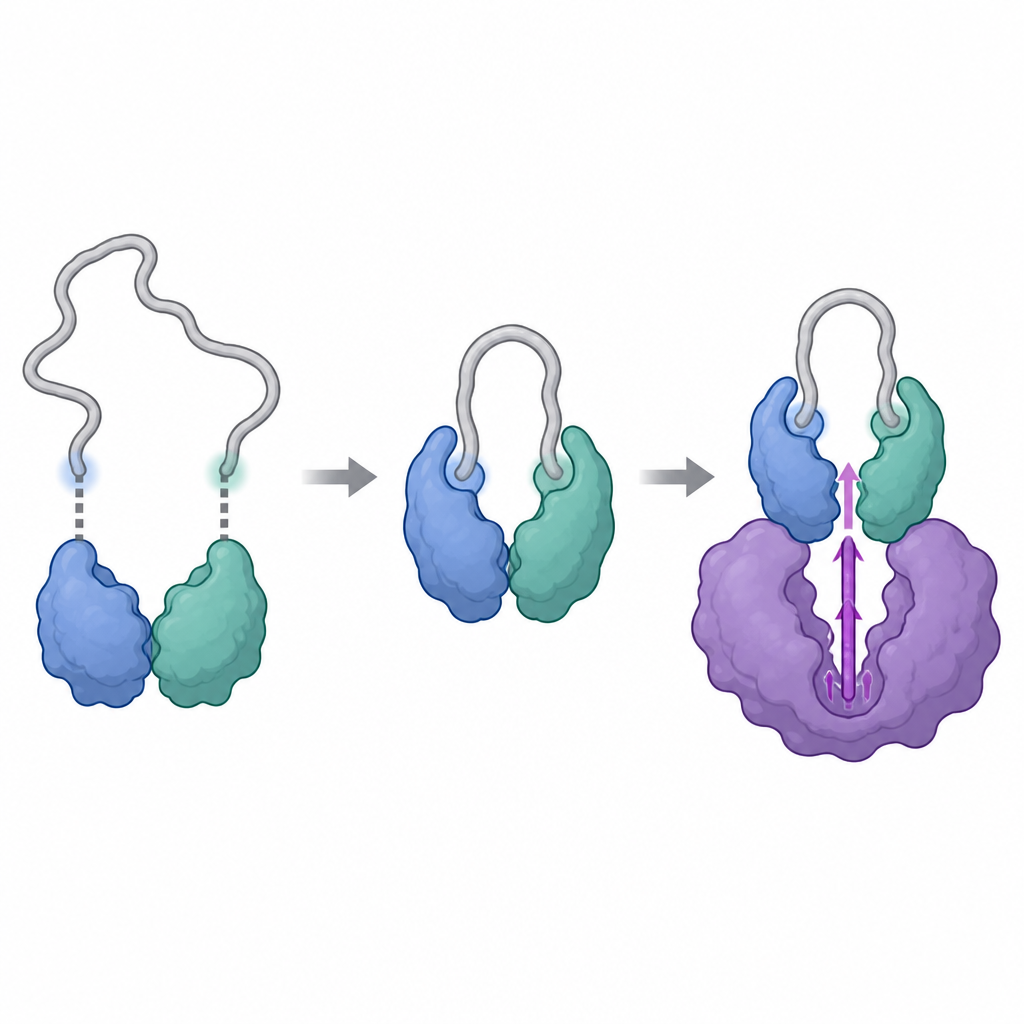
De onderzoekers gebruikten krachtige structurele technieken, waaronder cryo-elektronenmicroscopie en een methode die volgt hoe waterstofatomen in een eiwit uitgewisseld worden met zwaar water, om de complexen van cycline Y en 14-3-3 te visualiseren, met en zonder CDK16. Ze vonden dat cycline Y twee specifieke plekken draagt die elk aan één helft van het 14-3-3-paar kunnen vastklikken, als twee knopen in een sluiting. Wanneer beide plekken gefosforyleerd en betrokken zijn, grijpt 14-3-3 cycline Y vast en vormt subtiel een cruciaal oppervlak om. Deze herschikking onthult en verstevigt het gebied dat later met CDK16 zal interageren, waardoor cycline Y een beter aanmeerplatform wordt dan wanneer het op zichzelf staat.
Hoe CDK16 wordt ingeschakeld
Zodra cycline Y op de juiste manier door 14-3-3 wordt vastgehouden, kan CDK16 binden en de assemblage voltooien. De structurele snapshots tonen dat CDK16 cycline Y omarmt via twee hoofdcontactzones: een centraal gebied dat lijkt op de typische aanhechtingsplaats die bij andere cycline-afhankelijke enzymen wordt gezien, en een extra, flexibele flank aan de voorkant van CDK16 die uniek is voor deze subfamilie. Wanneer CDK16 bindt, vouwt deze losse flank zich en nestelt tegen cycline Y, wat helpt het complex vast te zetten. Tegelijkertijd wordt de activatielus van CDK16, een beweeglijk segment nabij het chemische centrum, geordend en in een "aan"-positie gehouden door directe aanrakingen van zowel cycline Y als het einde van het 14-3-3-paar. Mutaties in sleutelaminozuren op deze interfaces verzwakken het complex en verminderen CDK16’s activiteit scherp, wat bevestigt dat deze structurele contacten essentieel zijn om het enzym te activeren.
Het fijn afstellen van de schakelaar
De studie laat ook zien hoe CDK16 zelf bijgesteld kan worden door extra fosfaatlabels op zijn eigen voorste flank. In eerder werk was bekend dat bepaalde plaatsen in deze flank de bindingssterkte van cycline Y beïnvloeden. De nieuwe structurele en dynamische gegevens suggereren dat het toevoegen of verwijderen van deze labels kan veranderen hoe de flank vouwt en of die kan meedoen met het cycline Y/14-3-3-complex. In sommige gevallen kunnen de labels zelfs 14-3-3 direct naar CDK16 rekruteren, waardoor de toegang tot cycline Y wordt geblokkeerd of die regulerende sites worden afgeschermd tegen resetten. Op die manier lijken cellen een gelaagd controleschema te gebruiken waarin zowel cycline Y als CDK16 de juiste fosfaatmerken moeten dragen voordat een volledig actief complex kan vormen.
Wat dit betekent voor gezondheid en ziekte
Door de drie-eenheid tussen CDK16, cycline Y en 14-3-3 in moleculaire details uiteen te zetten, verklaart dit werk waarom CDK16 zich weigert te activeren zonder zijn helpers en hoe hun interactie het enzym in zijn actieve vorm duwt. Voor niet-specialisten is de kernboodschap dat CDK16 geen eenzame schakelaar is maar deel van een zorgvuldig bekabeld veiligheidscircuit dat afhankelijk is van meerdere eiwitcontacten en chemische labels. Omdat CDK16 bijdraagt aan het overleven van kankercellen en resistentie tegen behandeling, bieden de nieuw onthulde contactvlakken concrete doelwitten waar toekomstige geneesmiddelen zich tussen kunnen klemmen om het complex te verstoren en zo specifiek de activiteit van CDK16 te dempen terwijl verwante enzymen minder worden beïnvloed.
Bronvermelding: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Trefwoorden: CDK16, cycline Y, 14-3-3-eiwitten, proteïnecomplexen, kankersignalering