Clear Sky Science · fr
Base structurelle de l’activation de CDK16 médiée par la cycline Y et la protéine 14‑3‑3
Pourquoi ce casse‑tête protéique est important
À l’intérieur de nos cellules, des équipes de protéines coopèrent comme de petites machines pour contrôler la croissance, la survie et la réponse au stress. Une de ces protéines, appelée CDK16, influence le câblage des neurones, le recyclage du contenu cellulaire, la fertilité et le comportement des cellules cancéreuses. Pour autant, CDK16 reste curieusement inactif à moins que deux protéines auxiliaires spécifiques, la cycline Y et 14‑3‑3, ne se rassemblent de façon précise. Cette étude révèle, atome par atome, comment ce trio inhabituel s’assemble et comment leur interaction passe CDK16 de l’état inerte à l’état actif, offrant de nouveaux indices pour concevoir à l’avenir des médicaments anticancéreux ciblant ce système de contrôle.
Les acteurs clés dans la cellule
CDK16 appartient à une grande famille d’enzymes qui ajoutent de petits groupes phosphate à d’autres protéines, modifiant leur activité. La plupart de ses homologues s’activent simplement en se liant à une cycline. CDK16 fait exception. Il ne s’éveille que lorsqu’il est associé à la cycline Y, qui elle‑même doit être marquée par des phosphates et maintenue en place par une paire protéique connue sous le nom de 14‑3‑3. CDK16 a été lié au développement cérébral, aux étapes finales de la spermatogenèse, au recyclage cellulaire en période de privation et à la croissance ainsi qu’à la résistance aux traitements dans plusieurs cancers. Comprendre précisément comment CDK16 est contrôlé peut donc éclairer à la fois la biologie normale et la maladie.
Comment la paire auxiliaire remodele la cycline Y
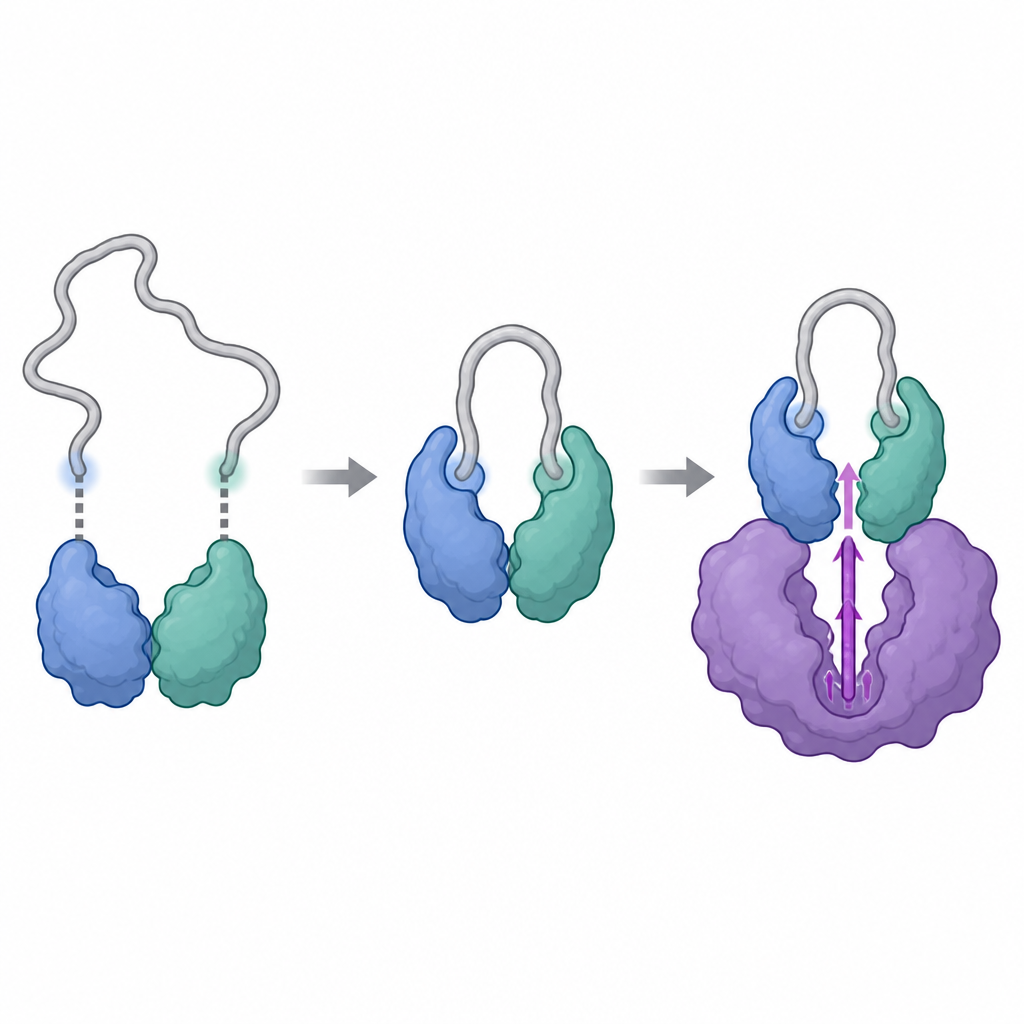
Les chercheurs ont utilisé des outils structuraux puissants, dont la cryo‑microscopie électronique et une technique suivant l’échange des hydrogènes d’une protéine avec de l’eau lourde, pour visualiser les complexes formés par la cycline Y et 14‑3‑3, avec ou sans CDK16. Ils ont trouvé que la cycline Y porte deux sites spécifiques qui peuvent chacun s’attacher à une moitié du dimère 14‑3‑3, comme deux boutons venant se fixer sur un fermoir. Lorsque les deux sites sont phosphorylés et engagés, 14‑3‑3 saisit la cycline Y et reconfigure subtilement une région de surface cruciale. Cette reconfiguration expose et rigidifie la zone qui interagira ensuite avec CDK16, faisant de la cycline Y un partenaire d’accueil mieux adapté que lorsqu’elle est isolée.
Comment CDK16 s’enclenche
Une fois que la cycline Y est correctement maintenue par 14‑3‑3, CDK16 peut se lier et compléter l’assemblage. Les clichés structuraux montrent que CDK16 embrasse la cycline Y par deux zones de contact principales : une région centrale rappelant le site d’accueil typique observé chez d’autres kinases dépendantes des cyclines, et une queue flexible à l’avant de CDK16 qui est spécifique à cette sous‑famille. Quand CDK16 se lie, cette queue mobile se replie et vient s’appuyer contre la cycline Y, contribuant au verrouillage du complexe. Parallèlement, la boucle d’activation de CDK16, un segment mobile proche de son centre catalytique, se stabilise et est maintenue dans une position « activée » grâce à des contacts directs à la fois de la cycline Y et de l’extrémité du dimère 14‑3‑3. La mutation d’acides aminés clés à ces interfaces affaiblit le complexe et réduit fortement l’activité de CDK16, confirmant que ces contacts structuraux sont essentiels pour l’activation de l’enzyme.
Ajuster finement l’interrupteur de contrôle
L’étude révèle aussi comment CDK16 lui‑même peut être modulé par des marques phosphate additionnelles sur sa propre queue avant. Dans des travaux antérieurs, certains sites de cette queue étaient connus pour influencer l’affinité de liaison à la cycline Y. Les nouvelles données structurales et dynamiques suggèrent que l’ajout ou la suppression de ces marques peut modifier le repliement de la queue et sa capacité à s’engager avec le complexe cycline Y–14‑3‑3. Dans certains cas, ces phosphates pourraient même recruter directement 14‑3‑3 sur CDK16, bloquant l’accès à la cycline Y ou protégeant ces sites régulateurs d’un réarrangement. Ainsi, la cellule semble utiliser un schéma de contrôle à plusieurs niveaux où la cycline Y et CDK16 doivent porter les bonnes marques phosphates avant qu’un complexe pleinement actif puisse se former.
Conséquences pour la santé et la maladie
En décrivant en détail l’étreinte à trois entre CDK16, la cycline Y et 14‑3‑3, ce travail explique pourquoi CDK16 refuse de s’activer sans ses auxiliaires et comment leur interaction pousse l’enzyme vers sa conformation active. Pour un public non spécialiste, l’idée principale est que CDK16 n’est pas un interrupteur isolé mais fait partie d’un circuit de sécurité finement câblé dépendant de multiples contacts protéiques et de marques chimiques. Étant donné que CDK16 contribue à la survie des cellules cancéreuses et à leur résistance aux traitements, les surfaces de contact nouvellement révélées offrent des cibles spécifiques où de futurs médicaments pourraient s’immiscer pour perturber le complexe, atténuant sélectivement l’activité de CDK16 tout en épargnant dans une large mesure les kinases apparentées.
Citation: Kohoutova, K., Kosek, D., Brzezina, A. et al. Structural basis of the cyclin Y/14-3-3 protein-mediated activation of CDK16. Nat Commun 17, 4262 (2026). https://doi.org/10.1038/s41467-026-70778-5
Mots-clés: CDK16, cycline Y, protéines 14‑3‑3, complexes protéiques, signalisation du cancer