Clear Sky Science · sv
Energi-sensorisk molekyl RORγ reglerar kolesterolmetabolism och immunsignalering vid diabetisk njursjukdom och åldrande
Varför denna forskning är viktig för personer med diabetes och åldrande njurar
Diabetisk njursjukdom och de naturliga åldersförändringarna i njurarna är två av huvudorsakerna till att människor till slut behöver dialys eller transplantation. Denna studie avslöjar en tidigare oupptäckt ”energi-sensorisk omkopplare” i njurtubuliceller som hjälper till att hålla kolesterol och inflammation i schack. När denna omkopplare, ett molekylärt nav kallat RORγ, slås av byggs fett- och inflammatorisk skada upp i njurarna. När den slås på igen skyddas njurarna. Förståelsen av detta kontrollsystem pekar mot nya sätt att bromsa njurskador både vid diabetes och åldrande.
Den dolda kopplingen mellan energianvändning, fett och njurskada
Njurtubuli ansvarar för mycket av kroppens städarbete och använder stor mängd energi för detta. Vid både diabetes och åldrande ackumulerar dessa celler överskott av lipider, särskilt kolesterol, och blir inflammerade och ärrbildade. Författarna undersökte njurvävnad från diabetiska möss, åldrade möss och människor med diabetes. I samtliga tre fann de att RORγ — ett nukleärt protein som hjälper celler att uppfatta energi och reglera gener — konsekvent var reducerat, särskilt i tubuliceller. Lägre nivåer av RORγ var associerade med sämre njurfunktion, mer ärrbildning och högre markörer för cellulärt åldrande, vilket tyder på att RORγ normalt fungerar som en väktare för tubulär hälsa. 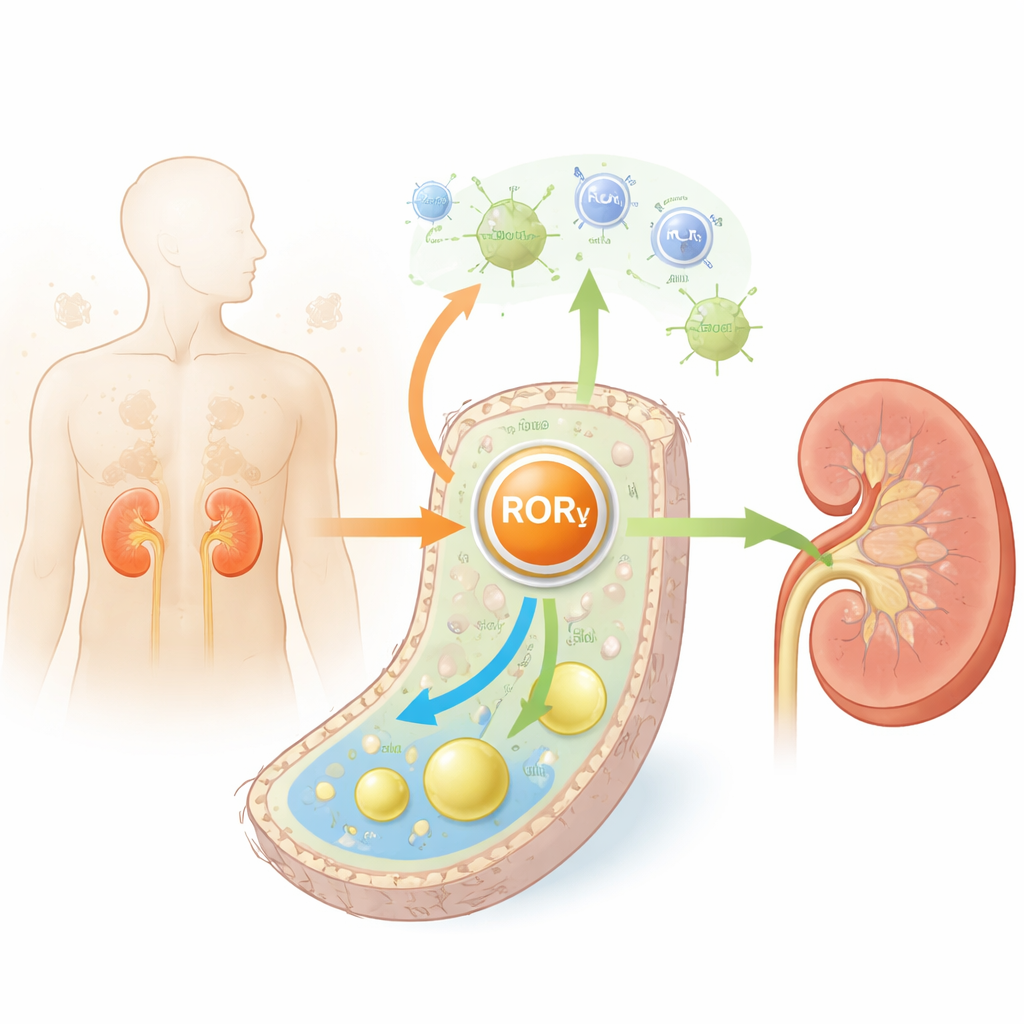
Hur RORγ håller kolesterolproduktion och immunsignaler under kontroll
Teamet upptäckte att RORγ skyddar tubuliceller genom att stabilisera ett annat protein, INSIG1, som sitter i membranet hos ett inre organell kallat endoplasmatiskt retikulum. INSIG1 fungerar normalt som en grindvakt som hindrar en kolesterolfrämjande faktor (SREBP2) och en inflammationsutlösande sensor (STING) från att förflytta sig till cellens transportcentrum, Golgi-apparaten, där de blir fullt aktiva. Vid diabetes eller åldrande, när RORγ är lågt, märks INSIG1 snabbt för nedbrytning och bryts ner, grinden fallerar och både kolesterolproduktion och inflammatorisk signalering ökar kraftigt.
De två hjälprutterna som RORγ använder för att stabilisera INSIG1
RORγ stärker INSIG1 genom två kompletterande hjälpsystem. För det första aktiverar det ett protein kallat YOD1 som tar bort ubiquitin-taggar — molekylära ”släng bort mig”-signaler — från INSIG1 och bromsar dess nedbrytning. För det andra ökar RORγ aktiviteten hos ett energisensorenzym, AMPK, genom att höja nivåerna av ett stöttande protein kallat CAB39 som monterar AMPK:s uppströmsaktivator. Aktivt AMPK tillsätter sedan en fosfatgrupp på INSIG1 vid en specifik plats, vilket försvagar dess interaktion med ett enzym som annars skulle rikta det för nedbrytning. Tillsammans får YOD1 och AMPK INSIG1 att bestå längre, vilket håller kolestersyntes och STING-driven immunaktivitet hårt begränsade. 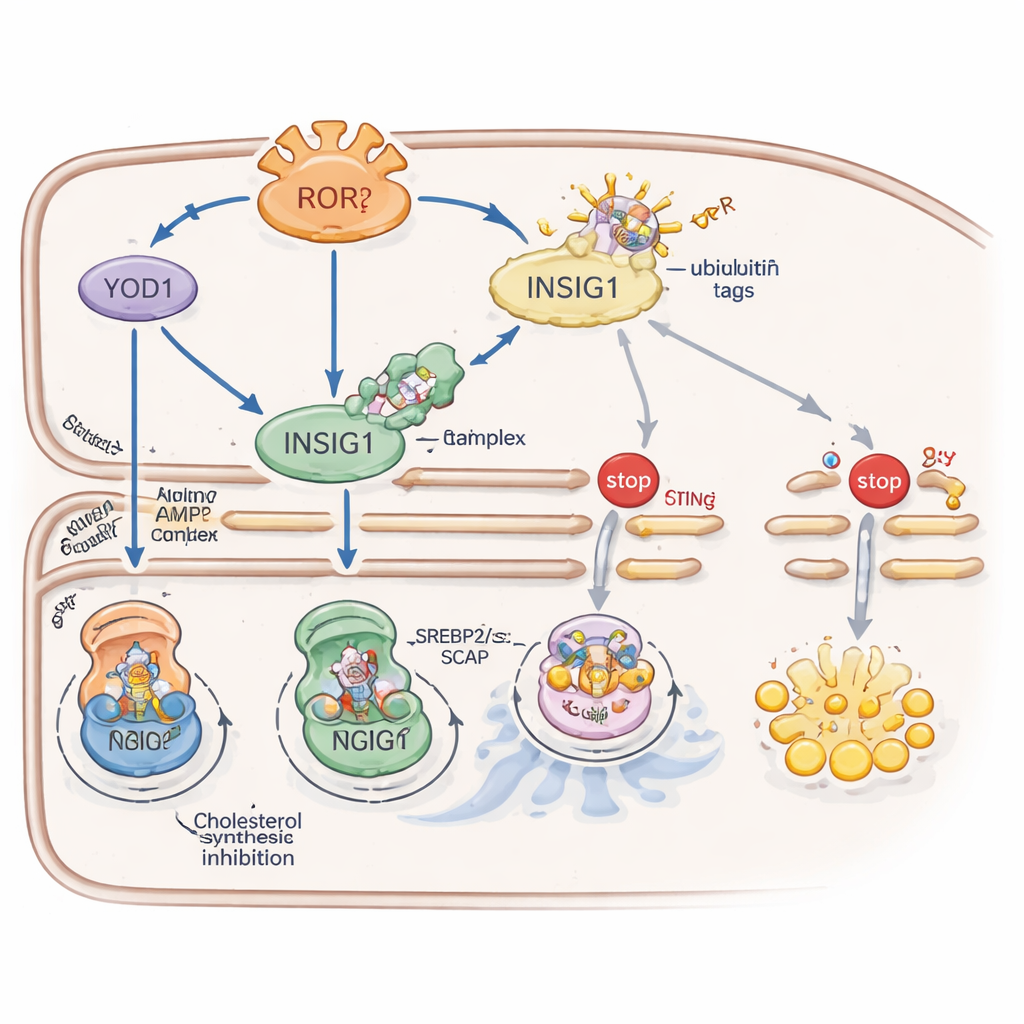
När den skyddande omkopplaren fallerar vid diabetes och åldrande
I en diabetisk miljö — högt socker och fett, oxidativ stress och DNA-skador — samverkar flera mekanismer för att stänga av RORγ. Ett DNA-bindande protein kallat CTCF blir mer aktivt och trycker ner RORγ-genen, vilket minskar dess produktion. Samtidigt försvagad AMPK-signalering och minskad aktivitet hos en annan regulator, SIRT1, reducerar RORγ:s förmåga att röra sig in i kärnan och försvagar dess grepp om målgener. I möss som konstruerats att sakna RORγ endast i tubuliceller orsakade diabetes och åldrande mycket grövre kolesteroluppbyggnad, inflammation, fibros och markörer för cellulär senescens, vilket bekräftar att förlust av denna omkopplare direkt påskyndar njurskada.
Att slå på RORγ igen som potentiell terapi
Eftersom RORγ är försvagat men inte helt frånvarande vid sjukdom testade författarna om återställande av dess aktivitet kunde skydda njurarna. Att tillföra extra RORγ specifikt till tubuliceller, eller att ge exosomer lastade med RORγ-protein, förbättrade njurstruktur och funktion hos diabetiska och åldrade möss: albuminutträde minskade, ärrbildning avtog och kolesterol- samt inflammatoriska geners aktivitet sjönk. De identifierade även en naturlig förening från Ganoderma lucidum (en medicinsk svamp), kallad ganodermanontriol, som binder till RORγ och förstärker dess aktivitet. Hos diabetiska möss stärkte denna förening RORγ:s nedströmsvägar, dämpade kolesterolproduktion och STING-signalering och lindrade njurskadan.
Vad detta betyder för framtida njurbehandlingar
Detta arbete avslöjar RORγ som en central koordinator som länkar njurcellens energitillstånd till fettomsättning och medfödda immunsvar. När den är aktiv stabiliserar den INSIG1 och förhindrar att både kolestersyntes och inflammatoriska larm löper amok. När den undertrycks, som vid diabetes och åldrande, blir njurarna sårbara för lipidöverbelastning, kronisk inflammation och ärrbildning. Genom att visa att RORγ kan reaktiveras med genleverans, exosom-baserade strategier eller småmolekylära agonister belyser studien en lovande ny strategi för att sakta ner eller förhindra diabetisk njursjukdom och åldersrelaterad njurförsämring.
Citering: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Nyckelord: diabetisk njursjukdom, kolesterolmetabolism, medfödd immunitet, åldrande njure, nukleära receptorer