Clear Sky Science · ar
الجزيء المستشعر للطاقة RORγ ينظّم أيض الكوليسترول والإشارات المناعية في مرض الكلى السكري والتقدّم بالعمر
لماذا تهم هذه الدراسة الأشخاص المصابين بالسكري أو الذين تتقدّم أعمار كليتهم
مرض الكلى السكري والشيخوخة الطبيعية للكلى هما من الأسباب الرئيسية التي تجعل الأشخاص يحتاجون في النهاية إلى غسيل الكلى أو زرع الكلى. تكشف هذه الدراسة عن «مفتاح استشعار الطاقة» داخل خلايا النبيبات الكلوية لم يكن معروفًا من قبل، يساعد على ضبط مستويات الكوليسترول والالتهاب. عندما يغلق هذا المفتاح، وهو جزيء يسمى RORγ، يتراكم الدّهون وتزداد الأضرار الالتهابية في الكلى. وعند إعادة تشغيله، تحمي الكلى من التلف. فهم هذا النظام الضابط يشير إلى سبل جديدة لإبطاء تلف الكلى في كلٍ من السكري والشيخوخة.
الرابط المخفي بين استهلاك الطاقة والدهون وإصابة الكلى
تتحمّل أنابيب الكلى كثيرًا من أعمال التنظيف في الجسم وتستهلك طاقة كبيرة للقيام بذلك. في كلٍ من السكري والشيخوخة، تتكدّس في هذه الخلايا دهون زائدة، خصوصًا الكوليسترول، وتصبح ملتهبة ومتندبة. فحص الباحثون أنسجة كلوية من فئران مصابة بالسكري، وفئران مسنة، وبشر مصابين بالسكري. عبر العينات الثلاثة، وجدوا أن مستوى RORγ — وهو بروتين نووي يساعد الخلايا على استشعار الطاقة وتنظيم التعبير الجيني — كان منخفضًا باستمرار، خاصة في خلايا الأنابيب. ارتبطت مستويات RORγ المنخفضة بوظيفة كلوية أسوأ ومزيد من التليف وزيادة مؤشرات شيخوخة الخلايا، مما يوحي بأن RORγ يعمل عادة كحارس على صحة الأنابيب. 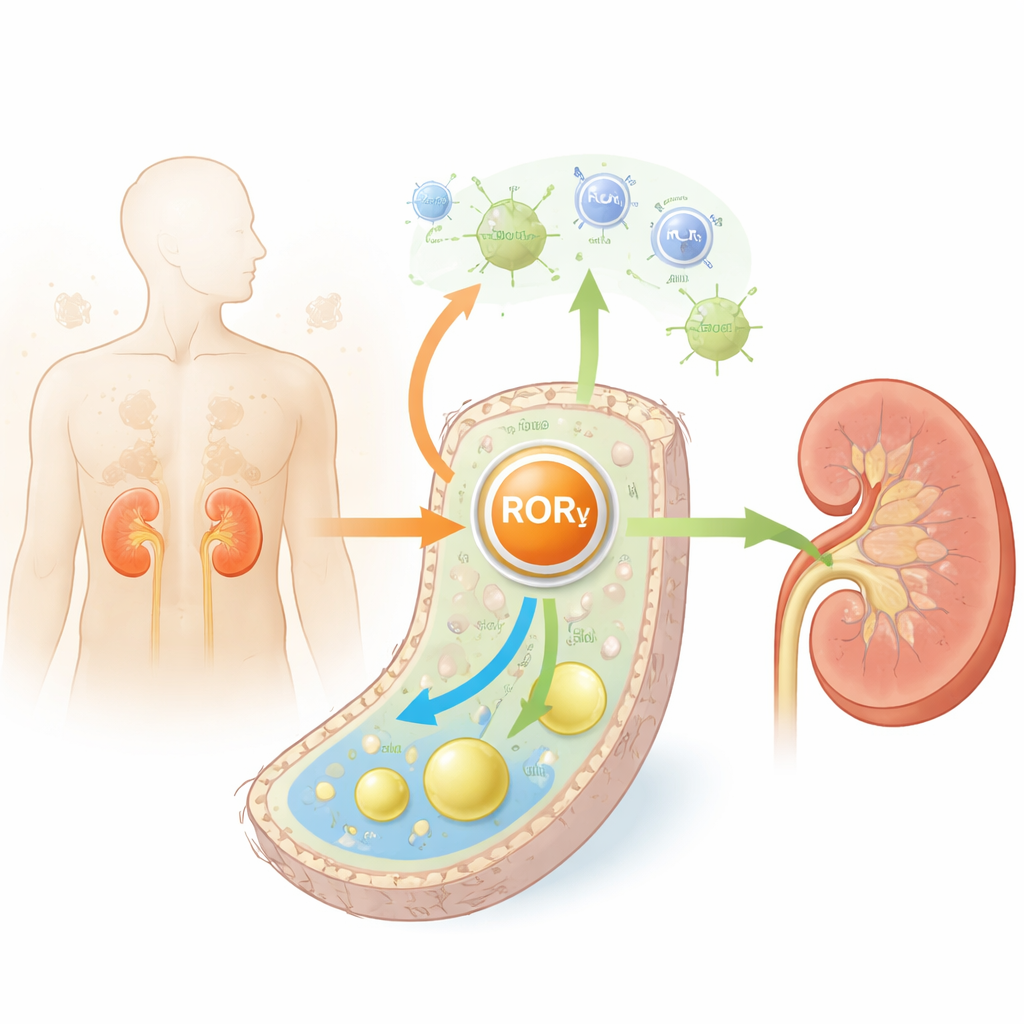
كيف يحافظ RORγ على ضبط إنتاج الكوليسترول وإشارات الإنذار المناعي
اكتشف الفريق أن RORγ يحمي خلايا الأنابيب عن طريق تثبيت بروتين آخر، INSIG1، الموجود في غشاء بنية داخلية تسمى الشبكة الإندوبلازمية. يعمل INSIG1 عادة كحارس بوابة، يمنع عاملًا محرضًا لإنتاج الكوليسترول (SREBP2) ومستشعرًا يطلق الالتهاب (STING) من الانتقال إلى جهاز غولجي داخل الخلية حيث يصبحان نشطين تمامًا. في حالة السكري أو التقدّم بالعمر، عندما يكون RORγ منخفضًا، يتم وضع علامة على INSIG1 بسرعة للتدمير وتحلّل، وتفشل البوابة، فيرتفع كل من إنتاج الكوليسترول والإشارات الالتهابية.
الطرِقان المساعدتان اللتان يستخدمهما RORγ لتثبيت INSIG1
يعزّز RORγ ثبات INSIG1 من خلال نظامين مساعدين متكاملين. أولًا، يُشغّل بروتينًا يدعى YOD1 الذي يزيل وسوم اليوبيكويتين — إشارات جزيئية تعني «تخلص مني» — عن INSIG1، مما يبطئ من تحلّله. ثانيًا، يعزز RORγ نشاط إنزيم حساس للطاقة، AMPK، بزيادة مستويات بروتين هيكلي يُدعى CAB39 الذي يجمع منشّط AMPK الأعلى رتبة. يقوم AMPK النشط بعدها بإضافة مجموعة فوسفات إلى INSIG1 في موقع محدد، ما يضعف تفاعله مع إنزيم كان سيستهدفه للتدمير. معًا، يجعل YOD1 وAMPK عمر INSIG1 أطول، محافظين على تخليق الكوليسترول ونشاط STING المناعي تحت كبح محكم. 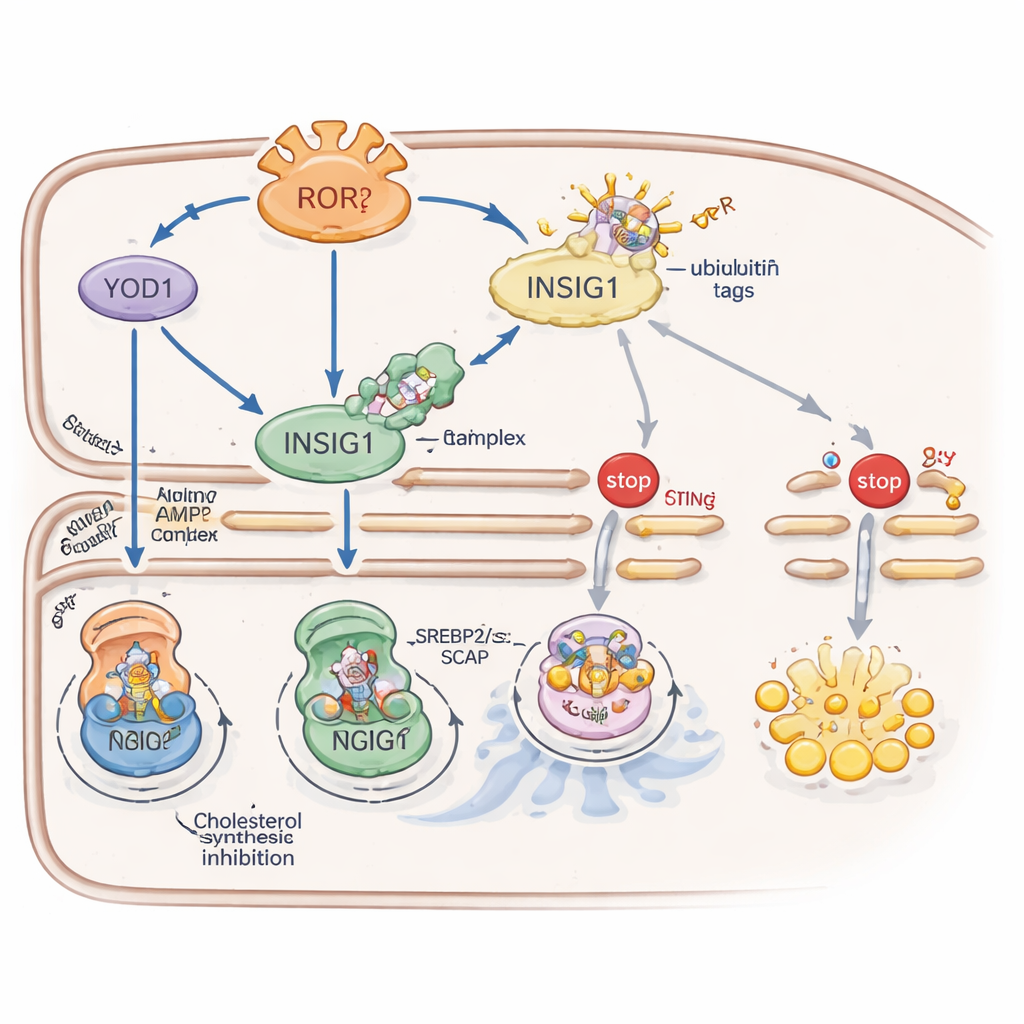
عندما يفشل المفتاح الوقائي في السكري والشيخوخة
في بيئة سكرية — ارتفاع السكر والدهون، والإجهاد التأكسدي، وتلف الحمض النووي — تتآمر عدة آليات لإيقاف RORγ. يصبح بروتين رابط للحمض النووي يُدعى CTCF أكثر نشاطًا ويكبّت جين RORγ، خافضًا من إنتاجه. في الوقت نفسه، يؤدي اضطراب إشارة AMPK وانخفاض نشاط منظم آخر، SIRT1، إلى تقليل دخول RORγ إلى النواة وإضعاف سيطرته على الجينات المستهدفة. في فئران مُهندسة نقصت فيها RORγ فقط في خلايا الأنابيب، أدى السكري والشيخوخة إلى تراكم كوليسترول أسوأ بكثير وارتفاع الالتهاب والتليف ومؤشرات شيخوخة الخلايا، مؤكدة أن فقدان هذا المفتاح يسرّع مباشرة إصابة الكلى.
إعادة تنشيط RORγ كعلاج محتمل
بما أن RORγ يكون مُضعّفًا ولكن ليس مفقودًا تمامًا في المرض، اختبر المؤلفون ما إذا كان استعادة نشاطه يمكن أن تحمي الكلى. توصيل RORγ إضافيًا بشكل خاص إلى خلايا الأنابيب، أو توفير حويصلات خارجية (إكسوسومات) محمّلة ببروتين RORγ، حسّن بنية ووظيفة الكلى في الفئران المصابة بالسكري والمسنة: انخفض تسرب الألبومين، قلّ التليف، وتراجعت نشاطات جينات الكوليسترول والالتهاب. كما عرّفوا مركبًا طبيعيًا من الفطر الطبي Ganoderma lucidum (ريشي)، يدعى ganodermanontriol، يرتبط بـRORγ ويعزّز نشاطه. في الفئران المصابة بالسكري، عزز هذا المركب مسارات RORγ اللاحقة، وكبح إنتاج الكوليسترول وإشارة STING، وخفّف من تلف الكلى.
ماذا يعني هذا لعلاجات الكلى المستقبلية
تكشف هذه الدراسة أن RORγ منسق مركزي يربط حالة طاقة خلية الكلى بمعالجة الدهون والاستجابات المناعية الفطرية. عندما يكون نشطًا، يثبّت INSIG1 ويمنع كلًا من تخليق الكوليسترول وإنذارات الالتهاب من الخروج عن السيطرة. وعند قمعه، كما في السكري والشيخوخة، تصبح الكلى عرضة لحمولة دهنية مفرطة والتهاب مزمن وتليف. بإظهار أن RORγ يمكن إعادة تنشيطه عبر توصيل جيني، منهجيات قائمة على الإكسوسومات، أو منشطات جزيئية صغيرة، تبرز الدراسة استراتيجية واعدة لإبطاء أو منع مرض الكلى السكري وتدهور الكلى المرتبط بالعمر.
الاستشهاد: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
الكلمات المفتاحية: مرض الكلى السكري, أيض الكوليسترول, المناعة الفطرية, الكلى المتقدمة في العمر, المستقبلات النووية