Clear Sky Science · de
Der energiesensierende Molekül RORγ reguliert Cholesterinstoffwechsel und Immunsignalgebung bei diabetischer Nierenerkrankung und Alterung
Warum diese Forschung für Menschen mit Diabetes und alternden Nieren wichtig ist
Diabetische Nierenerkrankung und die natürliche Alterung der Nieren gehören zu den Hauptgründen, warum Menschen schließlich eine Dialyse oder Transplantation benötigen. Diese Studie enthüllt einen bisher wenig beachteten „energiesensierenden Schalter“ in Tubuluszellen der Niere, der dabei hilft, Cholesterin und Entzündungen in Schach zu halten. Fällt dieser Schalter — ein Molekül namens RORγ — aus, sammeln sich Fett und entzündliche Schäden in der Niere an. Wird er wieder aktiviert, sind die Nieren geschützt. Das Verständnis dieses Regulationssystems weist auf neue Wege hin, um die Nierenschädigung bei Diabetes und Alterung zu verlangsamen.
Die verborgene Verbindung zwischen Energieverbrauch, Fett und Nierenschädigung
Die Nierentubuli übernehmen einen Großteil der Reinigungsarbeit des Körpers und benötigen dafür viel Energie. Sowohl bei Diabetes als auch beim Altern sammeln diese Zellen überschüssige Lipide, vor allem Cholesterin, an und werden entzündet und vernarbt. Die Autoren untersuchten Nierengewebe aus diabetischen Mäusen, gealterten Mäusen und Menschen mit Diabetes. In allen drei Gruppen fanden sie, dass RORγ — ein nukleäres Protein, das Zellen hilft, Energie zu erkennen und Gene zu regulieren — insbesondere in Tubuluszellen durchgängig vermindert war. Niedrigere RORγ-Werte korrelierten mit schlechterer Nierenfunktion, stärkerer Vernarbung und höheren Markern zellulären Alterns, was darauf hindeutet, dass RORγ normalerweise als Wächter der tubulären Gesundheit fungiert. 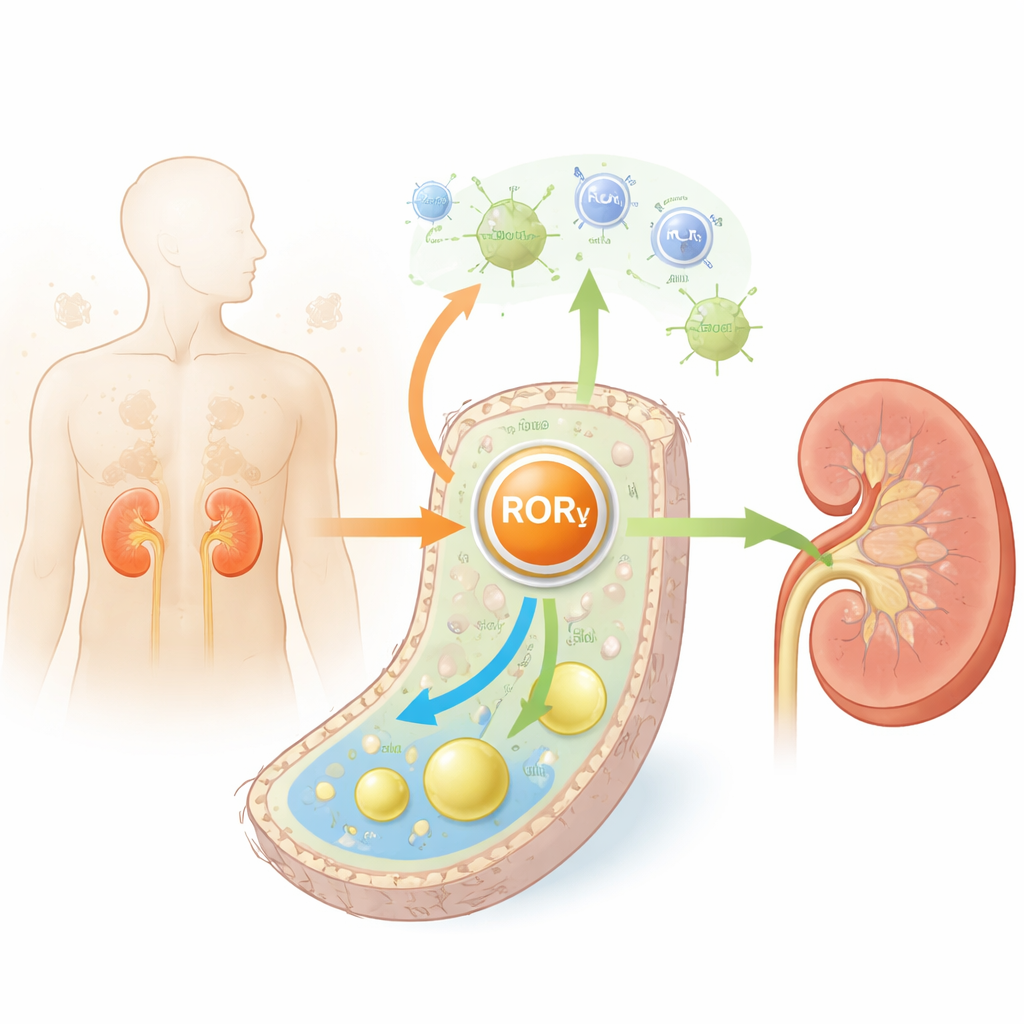
Wie RORγ die Cholesterinproduktion und Immunalarme unter Kontrolle hält
Das Team entdeckte, dass RORγ Tubuluszellen schützt, indem es ein anderes Protein, INSIG1, stabilisiert, das in der Membran eines inneren Zellkompartiments, des endoplasmatischen Retikulums, sitzt. INSIG1 fungiert normalerweise als Torwächter und verhindert, dass ein cholesterinfördernder Faktor (SREBP2) und ein entzündungsaktivierender Sensor (STING) zum Golgi-Apparat — dem Versandzentrum der Zelle — gelangen, wo sie voll aktiv werden. Bei Diabetes oder Alterung, wenn RORγ gering ist, wird INSIG1 schnell mit Abbausignalen versehen und degradiert, das Tor versagt, und sowohl die Cholesterinproduktion als auch die entzündlichen Signalwege nehmen stark zu.
Die zwei Hilfswege, über die RORγ INSIG1 stabilisiert
RORγ stärkt INSIG1 über zwei komplementäre Hilfssysteme. Erstens schaltet es ein Protein namens YOD1 ein, das Ubiquitin-Anhänge — molekulare „werf mich weg“-Signale — von INSIG1 entfernt und so dessen Abbau verlangsamt. Zweitens fördert RORγ die Aktivität einer Energiesensor-Kinase, AMPK, indem es die Menge eines Gerüstproteins namens CAB39 erhöht, das den Aktivator von AMPK zusammenfügt. Aktives AMPK fügt dann an einer spezifischen Stelle ein Phosphat an INSIG1 an, wodurch dessen Interaktion mit einem Enzym geschwächt wird, das sonst INSIG1 für den Abbau markieren würde. Zusammen sorgen YOD1 und AMPK dafür, dass INSIG1 länger erhalten bleibt und sowohl die Cholesterinsynthese als auch STING-vermittelte Immunaktivität streng gebremst bleiben. 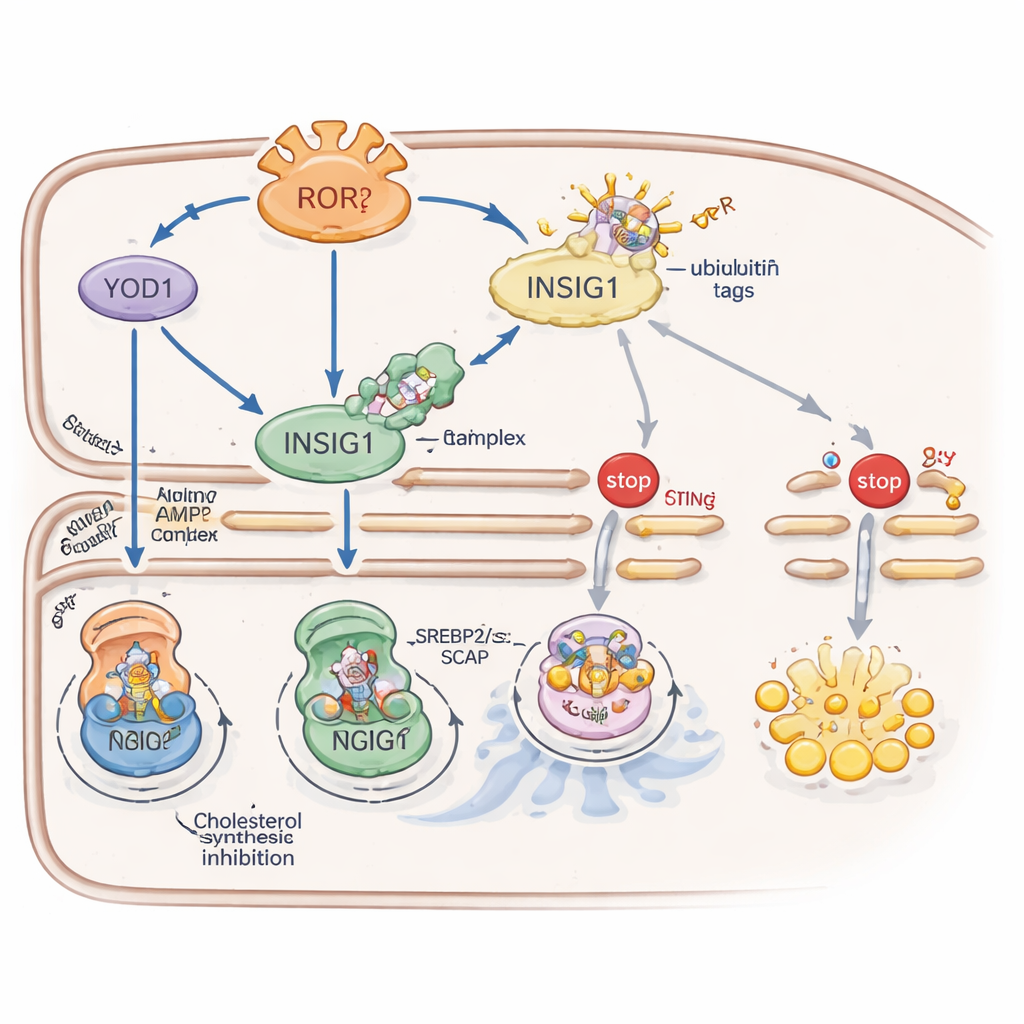
Wenn der Schutzschalter bei Diabetes und Alterung versagt
In einem diabetischen Umfeld — hoher Zucker- und Fettwerte, oxidativer Stress und DNA-Schäden — wirken mehrere Mechanismen zusammen, um RORγ abzuschalten. Ein DNA-bindendes Protein namens CTCF wird aktiver und dämpft das RORγ-Gen, wodurch dessen Produktion sinkt. Gleichzeitig verringern gestörte AMPK-Signale und reduzierte Aktivität eines weiteren Regulators, SIRT1, die Bewegung von RORγ in den Zellkern und schwächen seine Bindung an Zielgene. In Mäusen, denen RORγ gezielt nur in Tubuluszellen fehlte, führten Diabetes und Alterung zu deutlich stärkerer Cholesterinansammlung, Entzündung, Fibrose und Markern zellulärer Seneszenz, was bestätigt, dass der Verlust dieses Schalters die Nierenschädigung direkt beschleunigt.
RORγ wieder einschalten als potenzielle Therapie
Da RORγ in der Krankheit abgeschwächt, aber nicht vollständig verschwunden ist, prüften die Autoren, ob die Wiederherstellung seiner Aktivität die Nieren schützen kann. Die gezielte Zufuhr von zusätzlichem RORγ in Tubuluszellen oder die Verabreichung von Exosomen, die RORγ-Protein enthalten, verbesserte Struktur und Funktion der Nieren in diabetischen und gealterten Mäusen: Albuminaustritt nahm ab, Vernarbung verringerte sich und die Aktivität cholesterin- sowie entzündungsbezogener Gene sank. Sie identifizierten außerdem eine natürliche Verbindung aus Ganoderma lucidum (einem Heilpilz), genannt Ganodermanontriol, die an RORγ bindet und seine Aktivität verstärkt. Bei diabetischen Mäusen stärkte diese Verbindung RORγ-abhängige Signalwege, bremste Cholesterinproduktion und STING-Signalisierung und milderte die Nierenschädigung.
Was das für künftige Nierenbehandlungen bedeutet
Diese Arbeit zeigt RORγ als zentralen Koordinator, der den Energiestatus der Nierenzelle mit Fettstoffwechsel und angeborenen Immunantworten verknüpft. Wenn es aktiv ist, stabilisiert es INSIG1 und verhindert, dass sowohl die Cholesterinsynthese als auch entzündliche Alarme außer Kontrolle geraten. Ist es unterdrückt, wie bei Diabetes und Alterung, werden die Nieren anfällig für Lipidüberladung, chronische Entzündung und Vernarbung. Die Demonstration, dass RORγ durch Genlieferung, exosomenbasierte Ansätze oder kleine Molekül-Agonisten reaktiviert werden kann, hebt eine vielversprechende neue Strategie hervor, um diabetische Nierenerkrankung und altersbedingten Nierenverfall zu verlangsamen oder zu verhindern.
Zitation: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Schlüsselwörter: diabetische Nierenerkrankung, Cholesterinstoffwechsel, angeborene Immunität, alternde Niere, nukleäre Rezeptoren