Clear Sky Science · pl
Cząsteczka wykrywająca energię RORγ reguluje metabolizm cholesterolu i sygnalizację immunologiczną w cukrzycowej chorobie nerek oraz podczas starzenia
Dlaczego te badania mają znaczenie dla osób z cukrzycą i starzejącymi się nerkami
Cukrzycowa choroba nerek oraz naturalne starzenie się nerek to dwa główne powody, dla których pacjenci ostatecznie potrzebują dializ lub przeszczepu. To badanie ujawnia wcześniej niepoznany „przełącznik wykrywający energię” w komórkach kanalików nerkowych, który pomaga utrzymywać cholesterol i zapalenie pod kontrolą. Gdy ten przełącznik, cząsteczka o nazwie RORγ, wyłącza się, w nerkach gromadzą się tłuszcze i uszkodzenia zapalne. Gdy zostaje ponownie uaktywniony, nerki są chronione. Zrozumienie tego systemu regulacji wskazuje nowe drogi spowalniania uszkodzeń nerek zarówno w cukrzycy, jak i podczas starzenia.
Ukryte powiązanie między wykorzystaniem energii, tłuszczem i uszkodzeniem nerek
Kanaliki nerkowe wykonują dużą część pracy oczyszczającej organizm i zużywają przy tym dużo energii. Zarówno w cukrzycy, jak i podczas starzenia te komórki gromadzą nadmiar lipidów, zwłaszcza cholesterolu, i stają się zapalne oraz włóknieją. Autorzy przeanalizowali tkankę nerkową od myszy cukrzyczych, starszych myszy oraz osób z cukrzycą. We wszystkich trzech przypadkach zaobserwowali spadek poziomu RORγ — białka jądrowego, które pozwala komórkom wyczuwać stan energetyczny i regulować ekspresję genów — szczególnie w komórkach kanalików. Niższe poziomy RORγ wiązały się z gorszą funkcją nerek, większym włóknieniem i wyższymi markerami starzenia komórkowego, co sugeruje, że RORγ zwykle działa jako strażnik zdrowia kanalików. 
Jak RORγ kontroluje produkcję cholesterolu i alarmy immunologiczne
Zespół odkrył, że RORγ chroni komórki kanalików, stabilizując inne białko, INSIG1, które znajduje się w błonie organelli wewnątrzkomórkowej zwanej retikulum endoplazmatycznym. INSIG1 pełni zwykle rolę strażnika, uniemożliwiając czynnikowi promującemu cholesterol (SREBP2) oraz czujnikowi wywołującemu zapalenie (STING) przemieszczanie się do centrum wysyłkowego komórki, aparatu Golgiego, gdzie stają się w pełni aktywne. W cukrzycy lub podczas starzenia, gdy RORγ jest niskie, INSIG1 szybko oznaczane jest do zniszczenia i degradowane, brama zawodzi, a zarówno produkcja cholesterolu, jak i sygnalizacja zapalna gwałtownie rosną.
Dwie pomocnicze ścieżki, którymi RORγ stabilizuje INSIG1
RORγ wzmacnia INSIG1 poprzez dwa uzupełniające się systemy pomocnicze. Po pierwsze, włącza białko o nazwie YOD1, które usuwa znaczniki ubikwityny — molekularne sygnały „usuń mnie” — z INSIG1, spowalniając jego degradację. Po drugie, RORγ zwiększa aktywność enzymu wykrywającego stan energetyczny, AMPK, podnosząc poziomy białka rusztowaniowego CAB39, które składa aktywator AMPK znajdujący się wyżej w kaskadzie. Aktywny AMPK dodaje następnie grupę fosforanową do INSIG1 w określonym miejscu, co osłabia jego interakcję z enzymem, który w przeciwnym razie skierowałby je do zniszczenia. Razem YOD1 i AMPK wydłużają żywotność INSIG1, utrzymując syntezę cholesterolu i aktywność zależną od STING w rygorystycznych granicach. 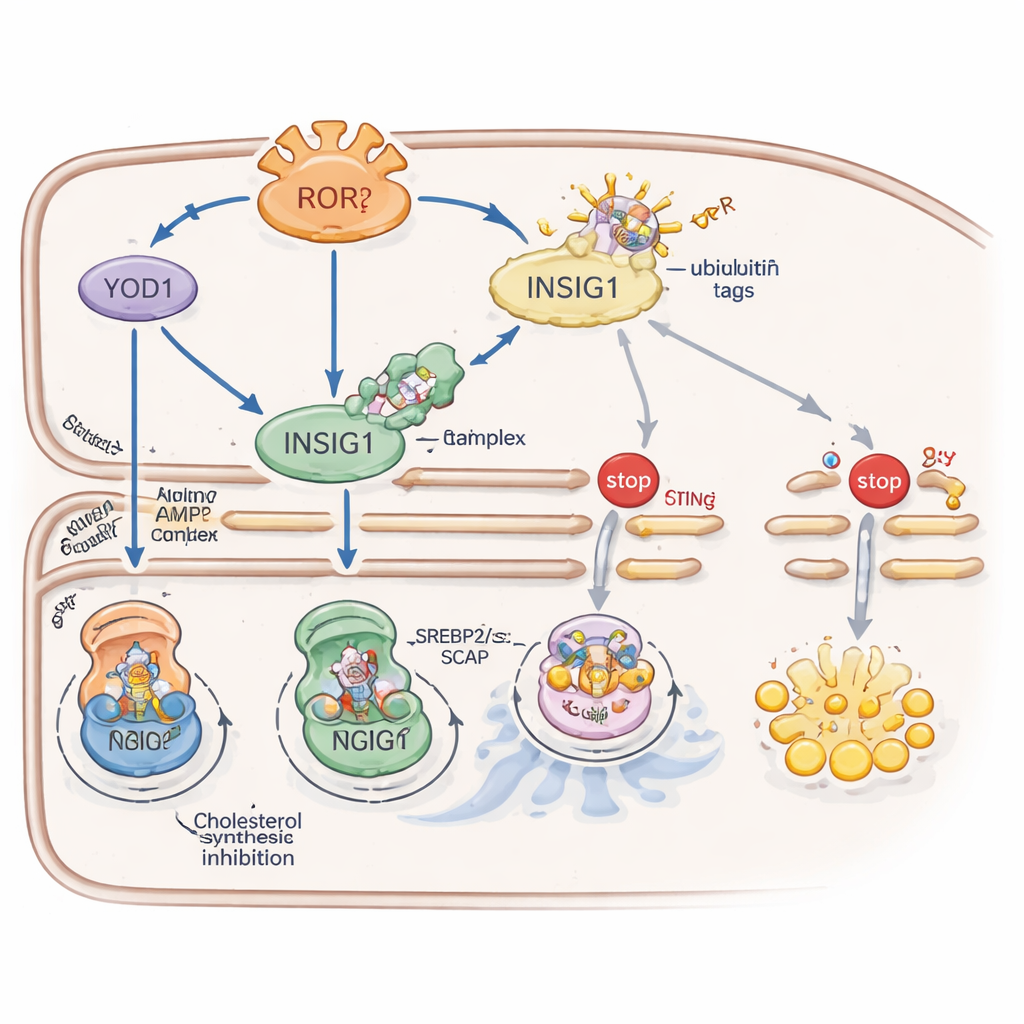
Kiedy ochronny przełącznik zawodzi w cukrzycy i starzeniu
W środowisku cukrzycowym — wysokie poziomy cukru i tłuszczu, stres oksydacyjny oraz uszkodzenia DNA — kilka mechanizmów sprzyja wyłączeniu RORγ. Białko wiążące DNA o nazwie CTCF staje się bardziej aktywne i hamuje gen RORγ, obniżając jego produkcję. Jednocześnie upośledzona sygnalizacja AMPK i zmniejszona aktywność innego regulatora, SIRT1, ograniczają przemieszczanie się RORγ do jądra i osłabiają jego wiązanie z genami docelowymi. U myszy zmodyfikowanych tak, by brakowało RORγ jedynie w komórkach kanalików, cukrzyca i starzenie wywołały znacznie większe nagromadzenie cholesterolu, zapalenie, włóknienie i markery starzenia komórkowego, potwierdzając, że utrata tego przełącznika bezpośrednio przyspiesza uszkodzenie nerek.
Przywrócenie aktywności RORγ jako potencjalna terapia
Ponieważ RORγ w chorobie jest osłabione, ale nie całkowicie nieobecne, autorzy sprawdzili, czy przywrócenie jego aktywności może chronić nerki. Dostarczenie dodatkowego RORγ specyficznie do komórek kanalików lub podanie egzosomów naładowanych białkiem RORγ poprawiło strukturę i funkcję nerek u myszy cukrzyczych i starszych: zmniejszyło przeciek albuminy, ograniczyło włóknienie oraz obniżyło aktywność genów związanych z cholesterolem i stanem zapalnym. Zidentyfikowali też związek naturalny z Ganoderma lucidum (grzyb leczniczy), zwany ganodermanontriolem, który wiąże się z RORγ i wzmacnia jego aktywność. U myszy cukrzyczych związek ten pobudził szlaki zależne od RORγ, ograniczył produkcję cholesterolu i sygnalizację STING oraz złagodził uszkodzenia nerek.
Co to oznacza dla przyszłych terapii nerek
Praca ta ukazuje RORγ jako centralnego koordynatora łączącego stan energetyczny komórki kanalikowej z gospodarką lipidową i odpowiedziami wrodzonego układu odpornościowego. Gdy jest aktywny, stabilizuje INSIG1 i zapobiega niekontrolowanemu wzrostowi zarówno syntezy cholesterolu, jak i alarmów zapalnych. Gdy jest stłumiony, jak w cukrzycy i starzeniu, nerki stają się podatne na przeciążenie lipidami, przewlekłe zapalenie i włóknienie. Pokazując, że RORγ można ponownie uaktywnić za pomocą terapii genowej, podejść opartych na egzosomach lub małocząsteczkowych agonistów, badanie wskazuje obiecującą strategię spowalniania lub zapobiegania cukrzycowej chorobie nerek i związanym ze starzeniem spadkom funkcji nerek.
Cytowanie: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Słowa kluczowe: cukrzycowa choroba nerek, metabolizm cholesterolu, odporność wrodzona, starość nerek, receptory jądrowe