Clear Sky Science · it
La molecola sensibile all’energia RORγ regola il metabolismo del colesterolo e la segnalazione immunitaria nella nefropatia diabetica e nell’invecchiamento
Perché questa ricerca è importante per le persone con diabete e reni che invecchiano
La nefropatia diabetica e l’invecchiamento naturale dei reni sono tra le principali cause per cui le persone arrivano alla dialisi o al trapianto. Questo studio mette in luce un “interruttore sensibile all’energia” finora non riconosciuto nelle cellule dei tubuli renali che contribuisce a tenere sotto controllo colesterolo e infiammazione. Quando questo interruttore, una molecola chiamata RORγ, si spegne, nei reni si accumulano lipidi e danno infiammatorio. Quando viene riattivato, i reni vengono protetti. Comprendere questo sistema di controllo apre la strada a nuovi modi per rallentare il danno renale sia nel diabete sia nell’invecchiamento.
Il legame nascosto tra consumo energetico, grasso e danno renale
I tubuli renali si occupano di gran parte del lavoro di pulizia del corpo e richiedono molta energia per farlo. Sia nel diabete sia nell’invecchiamento queste cellule accumulano lipidi in eccesso, in particolare colesterolo, e vanno incontro a infiammazione e fibrosi. Gli autori hanno analizzato tessuto renale di topi diabetici, topi anziani e persone con diabete. In tutti e tre i casi hanno riscontrato una riduzione costante di RORγ—una proteina nucleare che aiuta le cellule a percepire l’energia e a regolare i geni—in particolare nelle cellule tubulari. Livelli più bassi di RORγ erano associati a peggior funzione renale, maggiore fibrosi e marker di invecchiamento cellulare, suggerendo che RORγ funge normalmente da guardiano della salute tubulare. 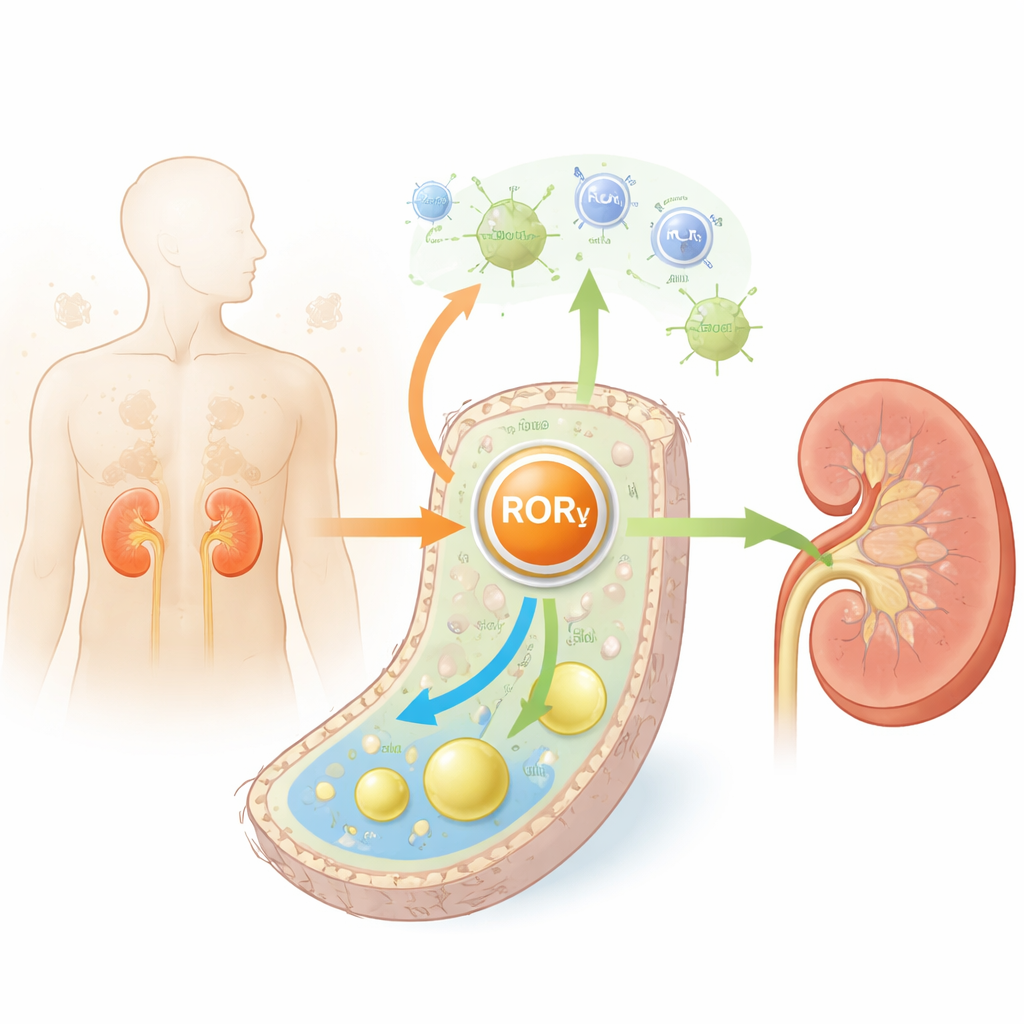
Come RORγ mantiene sotto controllo la produzione di colesterolo e gli allarmi immunitari
Il gruppo ha scoperto che RORγ protegge le cellule tubulari stabilizzando un’altra proteina, INSIG1, che si trova nella membrana di una struttura interna chiamata reticolo endoplasmatico. INSIG1 agisce normalmente come guardiano, impedendo a un fattore che promuove il colesterolo (SREBP2) e a un sensore che innesca l’infiammazione (STING) di spostarsi al centro di smistamento cellulare, il Golgi, dove diventano pienamente attivi. Nel diabete o con l’avanzare dell’età, quando RORγ è basso, INSIG1 viene rapidamente taggato per la distruzione e degradato, il cancello fallisce e sia la sintesi del colesterolo sia la segnalazione infiammatoria aumentano notevolmente.
Le due vie di supporto che RORγ usa per stabilizzare INSIG1
RORγ rinforza INSIG1 attraverso due sistemi complementari. Primo, attiva una proteina chiamata YOD1 che rimuove i tag di ubiquitina—segnali molecolari di “eliminami”—da INSIG1, rallentandone la degradazione. Secondo, RORγ potenzia l’attività di un enzima sensore dell’energia, AMPK, aumentando i livelli di una proteina impalcatura chiamata CAB39 che mette insieme l’attivatore a monte di AMPK. AMPK attiva quindi aggiunge un gruppo fosfato a INSIG1 in un sito specifico, indebolendone l’interazione con un enzima che altrimenti lo destinerebbe alla distruzione. Insieme, YOD1 e AMPK prolungano la vita di INSIG1, mantenendo la sintesi del colesterolo e l’attività immunitaria guidata da STING saldamente sotto controllo. 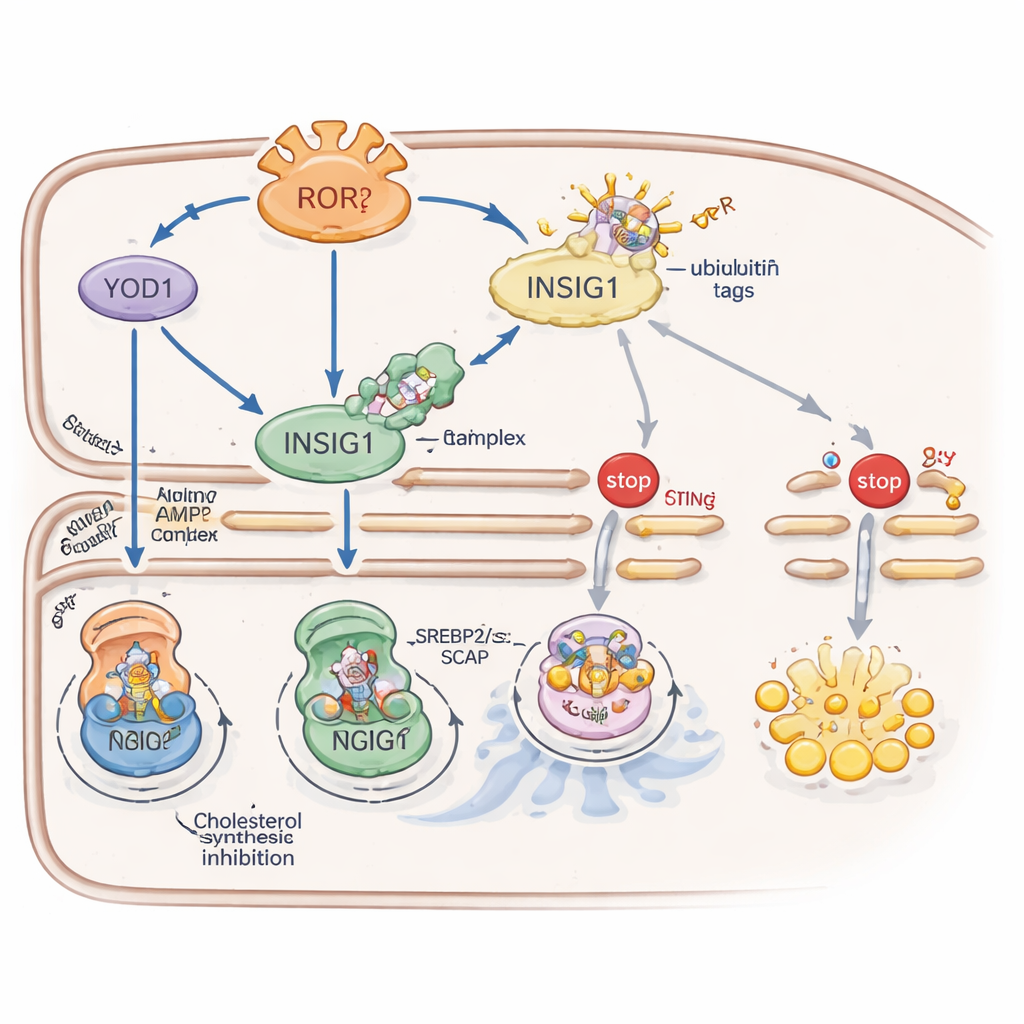
Quando l’interruttore protettivo fallisce nel diabete e nell’invecchiamento
In un ambiente diabetico—alto glucosio e grassi, stress ossidativo e danno al DNA—diversi meccanismi concorrono a spegnere RORγ. Una proteina legante il DNA chiamata CTCF diventa più attiva e reprime il gene RORγ, riducendone la produzione. Allo stesso tempo, un segnale AMPK compromesso e la ridotta attività di un altro regolatore, SIRT1, diminuiscono l’ingresso di RORγ nel nucleo e indeboliscono il suo controllo sui geni target. In topi ingegnerizzati per essere privi di RORγ solo nelle cellule tubulari, il diabete e l’invecchiamento hanno causato un accumulo di colesterolo molto più marcato, maggiore infiammazione, fibrosi e marker di senescenza cellulare, confermando che la perdita di questo interruttore accelera direttamente il danno renale.
Riaccendere RORγ come potenziale terapia
Poiché RORγ è indebolito ma non completamente assente nelle malattie, gli autori hanno testato se ripristinarne l’attività potesse proteggere i reni. Consegna di RORγ supplementare specificamente alle cellule tubulari, o l’uso di esosomi caricati con proteina RORγ, ha migliorato la struttura e la funzione renale in topi diabetici e anziani: la perdita di albumina è diminuita, la fibrosi si è ridotta e l’attività dei geni legati a colesterolo e infiammazione è calata. Hanno anche identificato un composto naturale da Ganoderma lucidum (un fungo medicinale), chiamato ganodermanontriol, che si lega a RORγ e ne potenzia l’attività. Nei topi diabetici questo composto ha aumentato le vie a valle di RORγ, ridotto la produzione di colesterolo e la segnalazione STING, attenuando il danno renale.
Cosa significa per i futuri trattamenti renali
Questo lavoro identifica RORγ come un coordinatore centrale che collega lo stato energetico della cellula renale alla gestione dei lipidi e alle risposte immunitarie innate. Quando è attivo, stabilizza INSIG1 e impedisce che sia la sintesi del colesterolo sia gli allarmi infiammatori escano dal controllo. Quando è soppresso, come nel diabete e nell’invecchiamento, i reni diventano vulnerabili a sovraccarico lipidico, infiammazione cronica e fibrosi. Dimostrando che RORγ può essere riattivato con la consegna genica, approcci basati su esosomi o agonisti di piccole molecole, lo studio mette in evidenza una strategia promettente per rallentare o prevenire la nefropatia diabetica e il declino renale legato all’età.
Citazione: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Parole chiave: nefropatia diabetica, metabolismo del colesterolo, immunità innata, rene invecchiato, recettori nucleari