Clear Sky Science · es
La molécula sensora de energía RORγ regula el metabolismo del colesterol y la señalización inmunitaria en la enfermedad renal diabética y el envejecimiento
Por qué esta investigación importa para personas con diabetes y riñones envejecidos
La enfermedad renal diabética y el envejecimiento natural de los riñones son dos de las principales causas por las que las personas acaban necesitando diálisis o un trasplante. Este estudio descubre un «interruptor sensor de energía» previamente no reconocido dentro de las células del túbulo renal que ayuda a mantener bajo control el colesterol y la inflamación. Cuando este interruptor, una molécula llamada RORγ, se apaga, se acumulan grasas y daños inflamatorios en los riñones. Cuando se reactiva, los riñones quedan protegidos. Comprender este sistema de control apunta a nuevas formas de frenar el daño renal tanto en la diabetes como en el envejecimiento.
El vínculo oculto entre el uso de energía, la grasa y la lesión renal
Los túbulos renales se encargan de gran parte del trabajo de limpieza del organismo y consumen mucha energía para hacerlo. En la diabetes y en el envejecimiento, estas células acumulan lípidos en exceso, especialmente colesterol, y se inflaman y cicatrizan. Los autores examinaron tejido renal de ratones diabéticos, ratones envejecidos y personas con diabetes. En los tres casos, observaron que RORγ—una proteína nuclear que ayuda a las células a detectar la energía y regular genes—estaba consistentemente reducida, sobre todo en las células del túbulo. Niveles bajos de RORγ se asociaron con peor función renal, más fibrosis y marcadores mayores de envejecimiento celular, lo que sugiere que RORγ actúa normalmente como un guardián de la salud tubular. 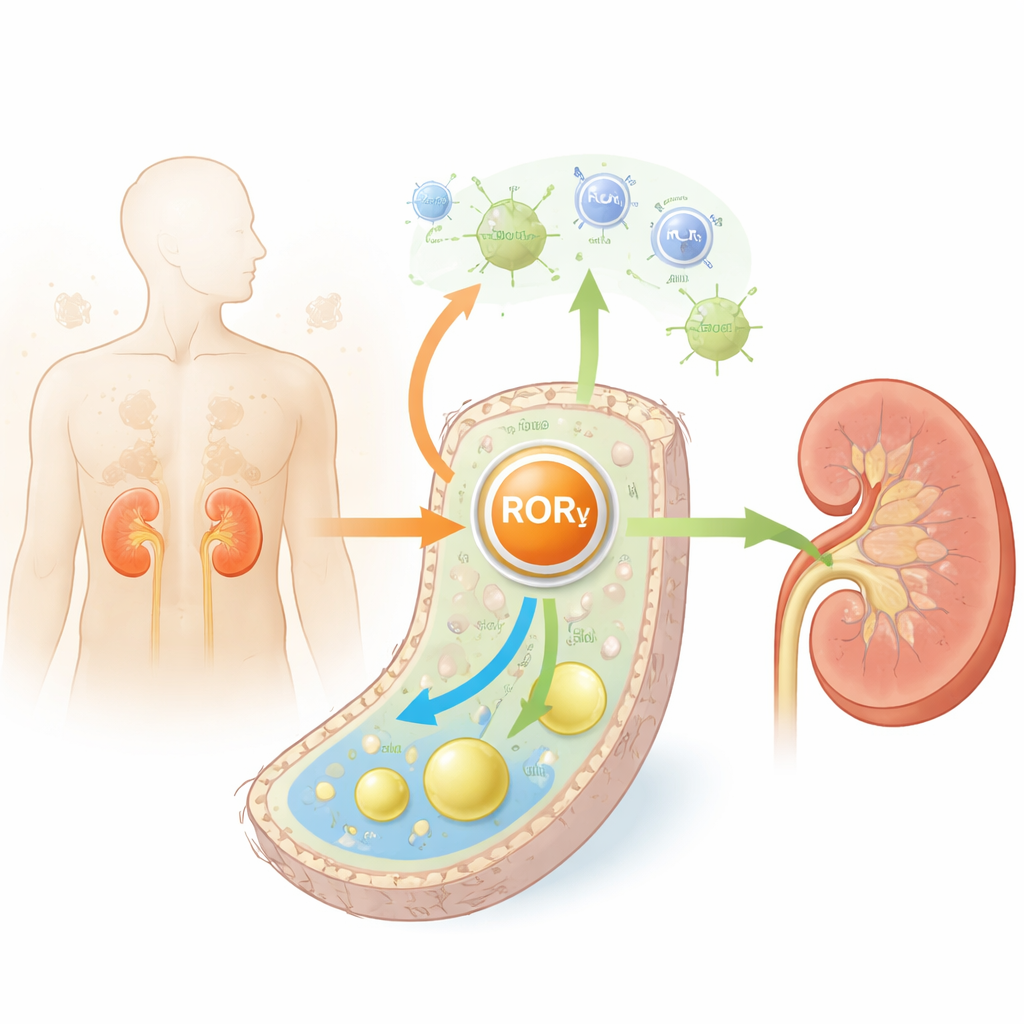
Cómo RORγ mantiene bajo control la producción de colesterol y las alarmas inmunitarias
El equipo descubrió que RORγ protege a las células tubulares estabilizando otra proteína, INSIG1, que se sitúa en la membrana de una estructura interna llamada retículo endoplásmico. INSIG1 actúa normalmente como portero, evitando que un factor que promueve el colesterol (SREBP2) y un sensor que desencadena inflamación (STING) viajen al centro de envío de la célula, el aparato de Golgi, donde se vuelven plenamente activos. En la diabetes o el envejecimiento, cuando RORγ está bajo, INSIG1 es etiquetado rápidamente para su destrucción y se degrada; la puerta falla y tanto la producción de colesterol como la señalización inflamatoria aumentan de forma descontrolada.
Las dos rutas auxiliares que RORγ emplea para estabilizar INSIG1
RORγ refuerza a INSIG1 mediante dos sistemas auxiliares complementarios. Primero, activa una proteína llamada YOD1 que elimina etiquetas de ubiquitina—señales moleculares de “desecharme”—de INSIG1, ralentizando su degradación. Segundo, RORγ potencia la actividad de una enzima sensora de energía, AMPK, al aumentar los niveles de una proteína andamiaje llamada CAB39 que reúne el activador upstream de AMPK. AMPK activo añade entonces un grupo fosfato a INSIG1 en un sitio específico, lo que debilita su interacción con una enzima que, de otro modo, lo dirigiría a la destrucción. Juntas, YOD1 y AMPK prolongan la vida de INSIG1, manteniendo la síntesis de colesterol y la actividad inmune mediada por STING bajo estricto control. 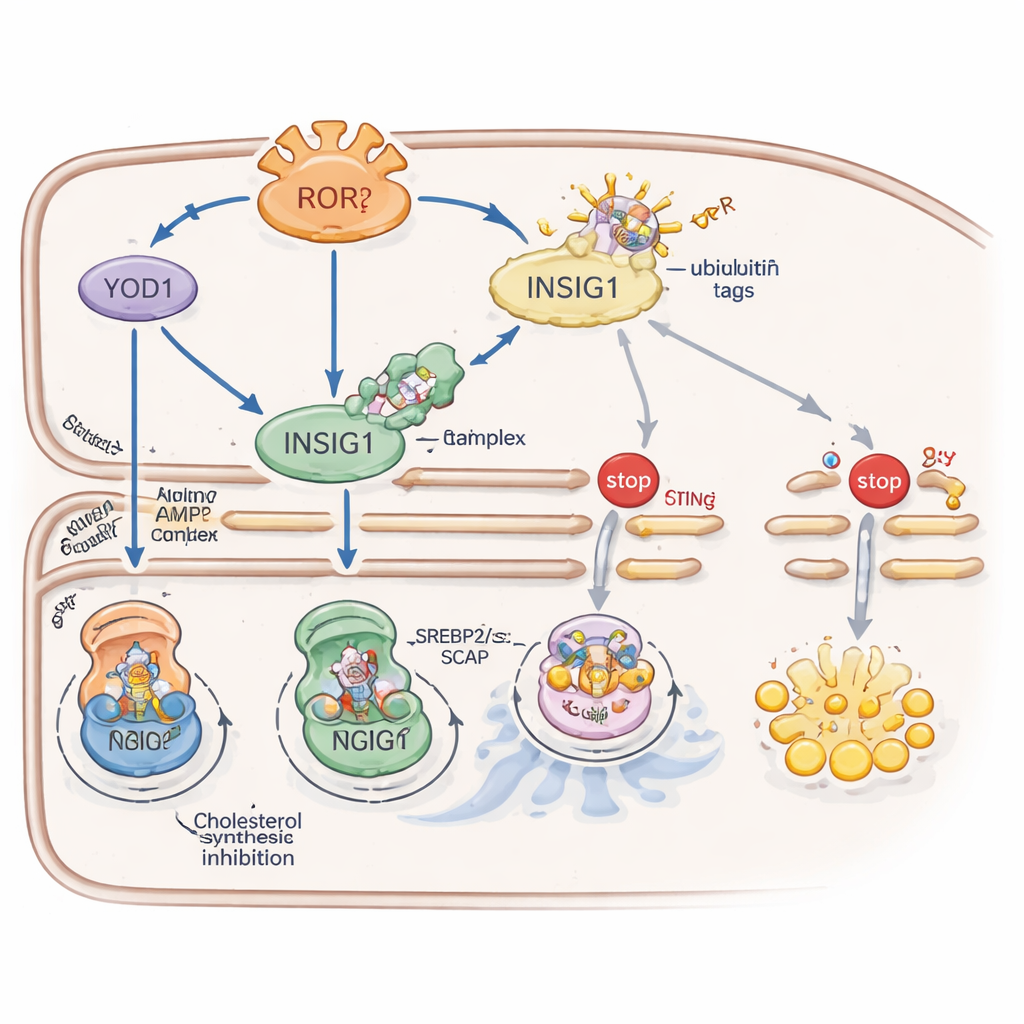
Cuando el interruptor protector falla en la diabetes y el envejecimiento
En un entorno diabético—alto en azúcar y grasa, con estrés oxidativo y daño en el ADN—varios mecanismos conspiran para apagar RORγ. Una proteína que se une al ADN llamada CTCF se vuelve más activa y reprime el gen RORγ, reduciendo su producción. Al mismo tiempo, la señalización de AMPK deteriorada y la actividad reducida de otro regulador, SIRT1, disminuyen el movimiento de RORγ hacia el núcleo y debilitan su control sobre los genes diana. En ratones diseñados para carecer de RORγ solo en las células tubulares, la diabetes y el envejecimiento causaron una acumulación de colesterol, inflamación, fibrosis y marcadores de senescencia celular mucho mayores, confirmando que la pérdida de este interruptor acelera directamente la lesión renal.
Reactivar RORγ como posible terapia
Dado que RORγ está debilitado pero no completamente ausente en la enfermedad, los autores probaron si restaurar su actividad podría proteger los riñones. La administración de RORγ adicional específicamente a las células tubulares, o el suministro de exosomas cargados con proteína RORγ, mejoró la estructura y la función renal en ratones diabéticos y envejecidos: la pérdida de albúmina disminuyó, la fibrosis se redujo y la actividad de genes relacionados con el colesterol y la inflamación cayó. También identificaron un compuesto natural de Ganoderma lucidum (un hongo medicinal), llamado ganodermanontriol, que se une a RORγ y potencia su actividad. En ratones diabéticos, este compuesto reforzó las vías downstream de RORγ, contuvo la producción de colesterol y la señalización de STING, y alivió el daño renal.
Qué significa esto para futuros tratamientos renales
Este trabajo revela a RORγ como un coordinador central que conecta el estado energético de la célula renal con el manejo de las grasas y las respuestas inmunitarias innatas. Cuando está activo, estabiliza INSIG1 y evita que tanto la síntesis de colesterol como las alarmas inflamatorias se descontrolen. Cuando se suprime, como en la diabetes y el envejecimiento, los riñones se vuelven vulnerables a la sobrecarga lipídica, la inflamación crónica y la fibrosis. Al demostrar que RORγ puede reactivarse mediante entrega génica, enfoques basados en exosomas o agonistas de pequeña molécula, el estudio subraya una estrategia prometedora para ralentizar o prevenir la enfermedad renal diabética y el deterioro renal relacionado con la edad.
Cita: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Palabras clave: enfermedad renal diabética, metabolismo del colesterol, inmunidad innata, riñón envejecido, receptores nucleares