Clear Sky Science · pt
Molécula sensora de energia RORγ regula o metabolismo do colesterol e o sinalizador imunológico na doença renal diabética e no envelhecimento
Por que esta pesquisa importa para pessoas com diabetes e rins envelhecidos
A doença renal diabética e o envelhecimento natural dos rins são duas das principais causas pelas quais as pessoas acabam precisando de diálise ou transplante. Este estudo revela um “interruptor sensorial de energia” até então não reconhecido dentro das células dos túbulos renais que ajuda a controlar o colesterol e a inflamação. Quando esse interruptor, uma molécula chamada RORγ, se desliga, gordura e danos inflamatórios se acumulam nos rins. Quando é religado, os rins ficam protegidos. Entender esse sistema de controle aponta para novas maneiras de retardar o dano renal tanto no diabetes quanto no envelhecimento.
O elo oculto entre uso de energia, gordura e lesão renal
Os túbulos renais realizam grande parte da limpeza do corpo e consomem muita energia para isso. Tanto no diabetes quanto no envelhecimento, essas células acumulam lipídios em excesso, especialmente colesterol, e ficam inflamadas e com fibrose. Os autores examinaram tecido renal de camundongos diabéticos, camundongos envelhecidos e pessoas com diabetes. Em todos os três, observaram que a RORγ — uma proteína nuclear que ajuda as células a perceberem energia e regular genes — estava consistentemente reduzida, especialmente nas células tubulares. Níveis mais baixos de RORγ associaram-se a pior função renal, mais fibrose e marcadores aumentados de envelhecimento celular, sugerindo que a RORγ normalmente atua como guardiã da saúde tubular. 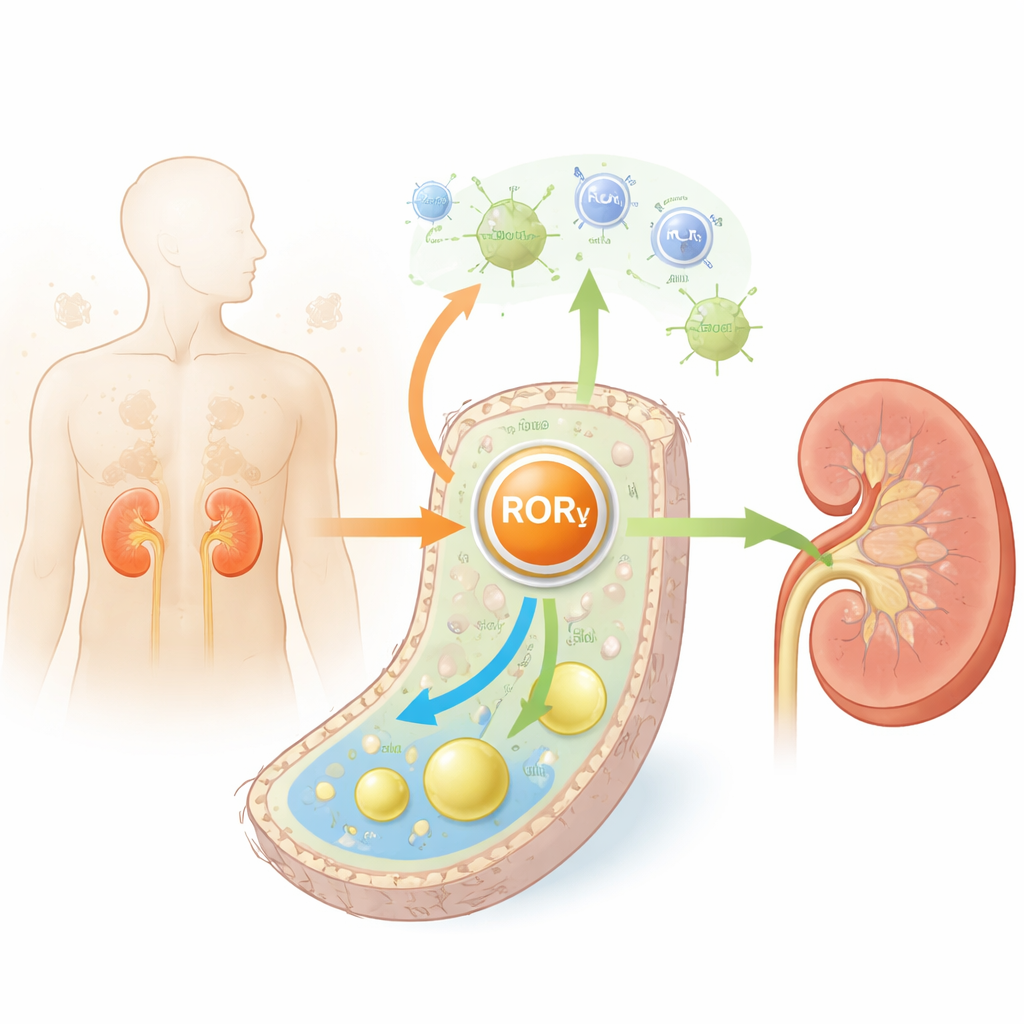
Como a RORγ mantém a produção de colesterol e os alarmes imunes sob controle
A equipe descobriu que a RORγ protege as células tubulares ao estabilizar outra proteína, INSIG1, que fica na membrana de uma estrutura interna chamada retículo endoplasmático. A INSIG1 normalmente age como porteira, impedindo que um fator promotor de colesterol (SREBP2) e um sensor que desencadeia inflamação (STING) viagem até o centro de empacotamento da célula, o aparelho de Golgi, onde se tornam totalmente ativos. No diabetes ou no envelhecimento, quando a RORγ está baixa, a INSIG1 é rapidamente marcada para destruição e degradada, a porteira falha e tanto a produção de colesterol quanto a sinalização inflamatória disparam.
As duas rotas auxiliares que a RORγ usa para estabilizar a INSIG1
A RORγ reforça a INSIG1 por meio de dois sistemas auxiliares complementares. Primeiro, ela ativa uma proteína chamada YOD1 que remove as marcas de ubiquitina — sinais moleculares de “descartar” — da INSIG1, retardando sua degradação. Segundo, a RORγ aumenta a atividade de uma enzima sensora de energia, AMPK, elevando os níveis de uma proteína andaime chamada CAB39, que monta o ativador a montante da AMPK. A AMPK ativa então adiciona um grupo fosfato à INSIG1 em um sítio específico, o que enfraquece sua interação com uma enzima que, de outra forma, a direcionaria para destruição. Juntas, YOD1 e AMPK fazem a INSIG1 durar mais, mantendo a síntese de colesterol e a atividade imune dirigida por STING sob forte restrição. 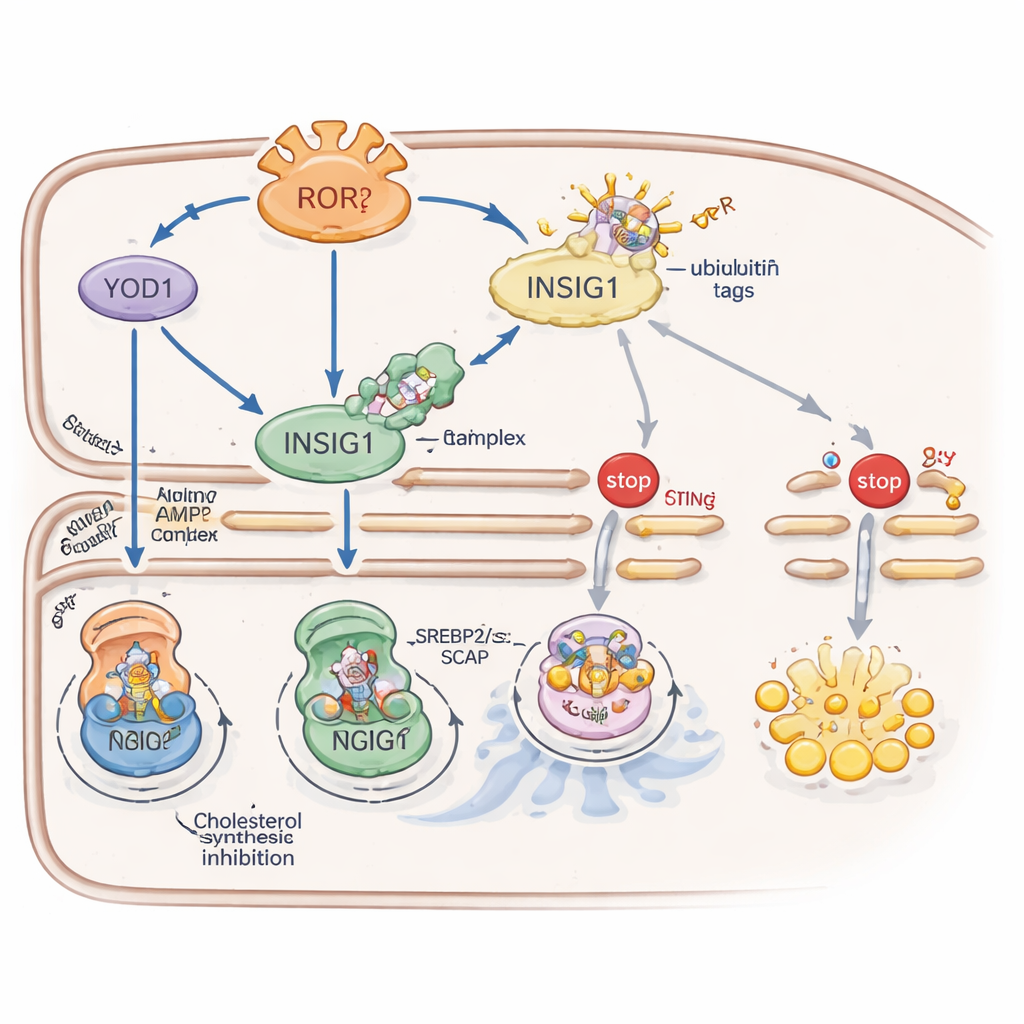
Quando o interruptor protetor falha no diabetes e no envelhecimento
Em um ambiente diabético — alto teor de açúcar e gordura, estresse oxidativo e danos ao DNA — vários mecanismos conspiram para desligar a RORγ. Uma proteína de ligação ao DNA chamada CTCF torna-se mais ativa e reprime o gene da RORγ, reduzindo sua produção. Ao mesmo tempo, a sinalização prejudicada da AMPK e a atividade reduzida de outro regulador, SIRT1, diminuem a translocação da RORγ para o núcleo e enfraquecem seu controle sobre genes-alvo. Em camundongos geneticamente modificados para não expressar RORγ apenas nas células tubulares, o diabetes e o envelhecimento provocaram acúmulo de colesterol muito mais grave, inflamação, fibrose e marcadores de senescência celular, confirmando que a perda desse interruptor acelera diretamente a lesão renal.
Reativar a RORγ como terapia em potencial
Como a RORγ fica enfraquecida, mas não totalmente ausente na doença, os autores testaram se restaurar sua atividade poderia proteger os rins. A entrega de RORγ extra especificamente às células tubulares, ou o fornecimento de exossomos carregados com a proteína RORγ, melhorou a estrutura e função renal em camundongos diabéticos e envelhecidos: a perda de albumina diminuiu, a fibrose reduziu-se e a atividade de genes de colesterol e inflamação caiu. Eles também identificaram um composto natural do Ganoderma lucidum (um cogumelo medicinal), chamado ganodermanontriol, que se liga à RORγ e potencializa sua atividade. Em camundongos diabéticos, esse composto estimulou as vias a montante da RORγ, conteve a produção de colesterol e a sinalização STING, e aliviou o dano renal.
O que isso significa para futuros tratamentos renais
Este trabalho revela a RORγ como uma coordenadora central que conecta o estado energético da célula renal ao manejo de lipídios e às respostas imunes inatas. Quando ativa, ela estabiliza a INSIG1 e impede que tanto a síntese de colesterol quanto os alarmes inflamatórios saiam do controle. Quando suprimida, como no diabetes e no envelhecimento, os rins ficam vulneráveis ao excesso de lipídios, à inflamação crônica e à fibrose. Ao demonstrar que a RORγ pode ser reativada com entrega gênica, abordagens baseadas em exossomos ou agonistas de pequenas moléculas, o estudo destaca uma estratégia promissora para retardar ou prevenir a doença renal diabética e o declínio renal relacionado à idade.
Citação: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Palavras-chave: doença renal diabética, metabolismo do colesterol, imunidade inata, rim envelhecido, receptores nucleares