Clear Sky Science · fr
La molécule détectrice d’énergie RORγ régule le métabolisme du cholestérol et la signalisation immunitaire dans la néphropathie diabétique et le vieillissement
Pourquoi cette recherche importe pour les personnes atteintes de diabète et pour les reins vieillissants
La néphropathie diabétique et le vieillissement naturel des reins sont deux des principales raisons pour lesquelles des patients finissent par nécessiter une dialyse ou une greffe. Cette étude met au jour un « interrupteur détecteur d’énergie » jusque-là méconnu au sein des cellules du tubule rénal qui aide à contrôler le cholestérol et l’inflammation. Lorsque cet interrupteur, une molécule appelée RORγ, s’éteint, des dépôts lipidiques et des lésions inflammatoires s’accumulent dans les reins. Lorsqu’on le réactive, les reins sont protégés. Comprendre ce système de contrôle ouvre des pistes pour ralentir les lésions rénales liées au diabète et au vieillissement.
Le lien caché entre utilisation d’énergie, lipides et lésions rénales
Les tubules rénaux assurent une grande partie du travail d’épuration de l’organisme et consomment beaucoup d’énergie pour le faire. Dans le diabète comme dans le vieillissement, ces cellules accumulent des lipides en excès, notamment du cholestérol, et deviennent enflammées et fibreuses. Les auteurs ont examiné des tissus rénaux de souris diabétiques, de souris âgées et de personnes atteintes de diabète. Dans les trois cas, ils ont constaté que RORγ — une protéine nucléaire qui aide les cellules à détecter l’état énergétique et à réguler l’expression génique — était systématiquement réduite, notamment dans les cellules tubulaires. Des niveaux plus faibles de RORγ étaient associés à une fonction rénale plus altérée, à davantage de fibrose et à des marqueurs accrus de sénescence cellulaire, suggérant que RORγ agit normalement comme un gardien de la santé tubulaire. 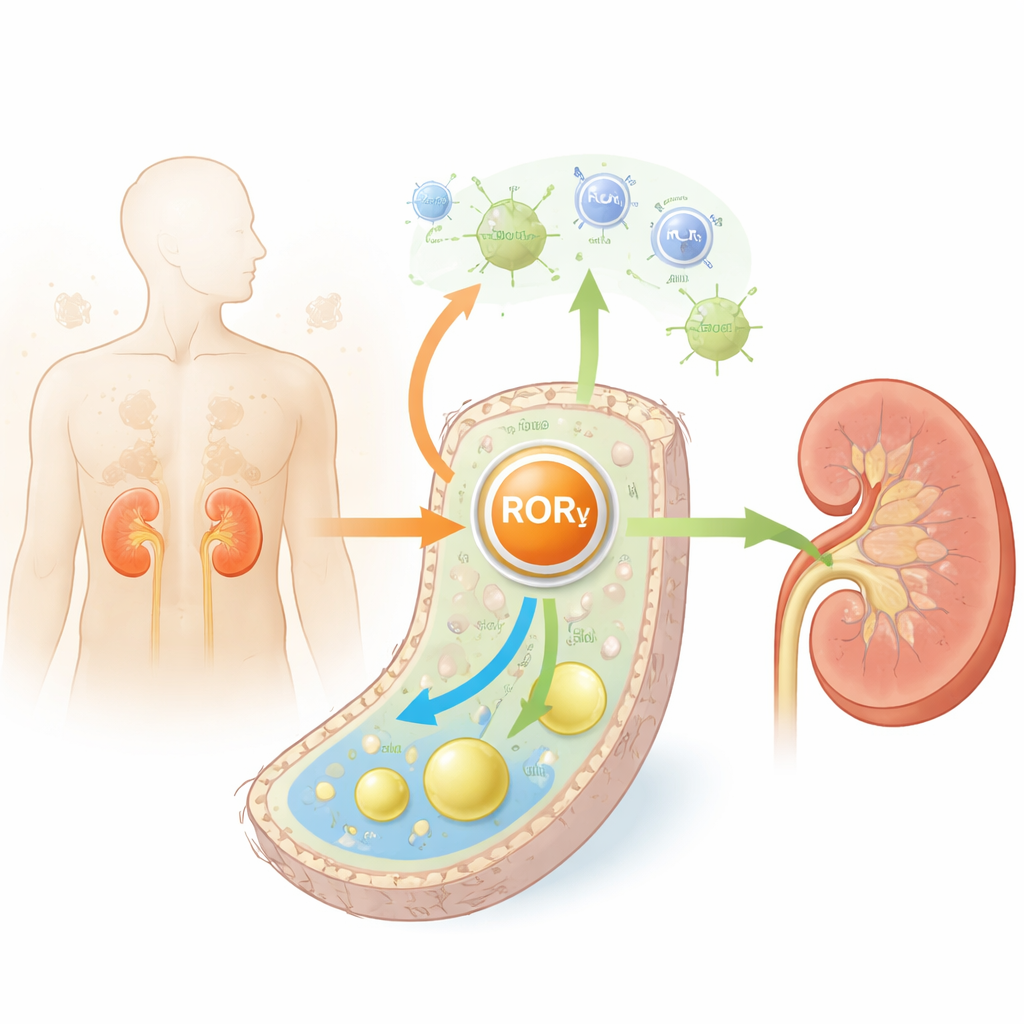
Comment RORγ maintient la production de cholestérol et les alertes immunitaires sous contrôle
L’équipe a découvert que RORγ protège les cellules tubulaires en stabilisant une autre protéine, INSIG1, qui se trouve dans la membrane d’un compartiment interne appelé réticulum endoplasmique. INSIG1 joue normalement le rôle de gardien, empêchant un facteur promoteur du cholestérol (SREBP2) et un détecteur déclencheur d’inflammation (STING) de migrer vers le centre d’expédition de la cellule, l’appareil de Golgi, où ils deviennent pleinement actifs. Dans le diabète ou le vieillissement, quand RORγ est faible, INSIG1 est rapidement marqué pour destruction et dégradé, la barrière cède, et la synthèse du cholestérol ainsi que la signalisation inflammatoire augmentent fortement.
Les deux voies auxiliaires par lesquelles RORγ stabilise INSIG1
RORγ renforce INSIG1 via deux systèmes auxiliaires complémentaires. Premièrement, il active une protéine appelée YOD1 qui enlève les étiquettes ubiquitine — signaux moléculaires de « jetez-moi » — d’INSIG1, ralentissant sa dégradation. Deuxièmement, RORγ stimule l’activité d’une enzyme détectrice d’énergie, AMPK, en augmentant les niveaux d’une protéine échafaudage nommée CAB39 qui assemble l’activateur en amont d’AMPK. L’AMPK active ajoute alors un groupe phosphate sur INSIG1 à un site spécifique, ce qui affaiblit son interaction avec une enzyme qui la viserait autrement pour destruction. Ensemble, YOD1 et AMPK prolongent la durée de vie d’INSIG1, maintenant la synthèse du cholestérol et l’activité immunitaire pilotée par STING sous un contrôle strict. 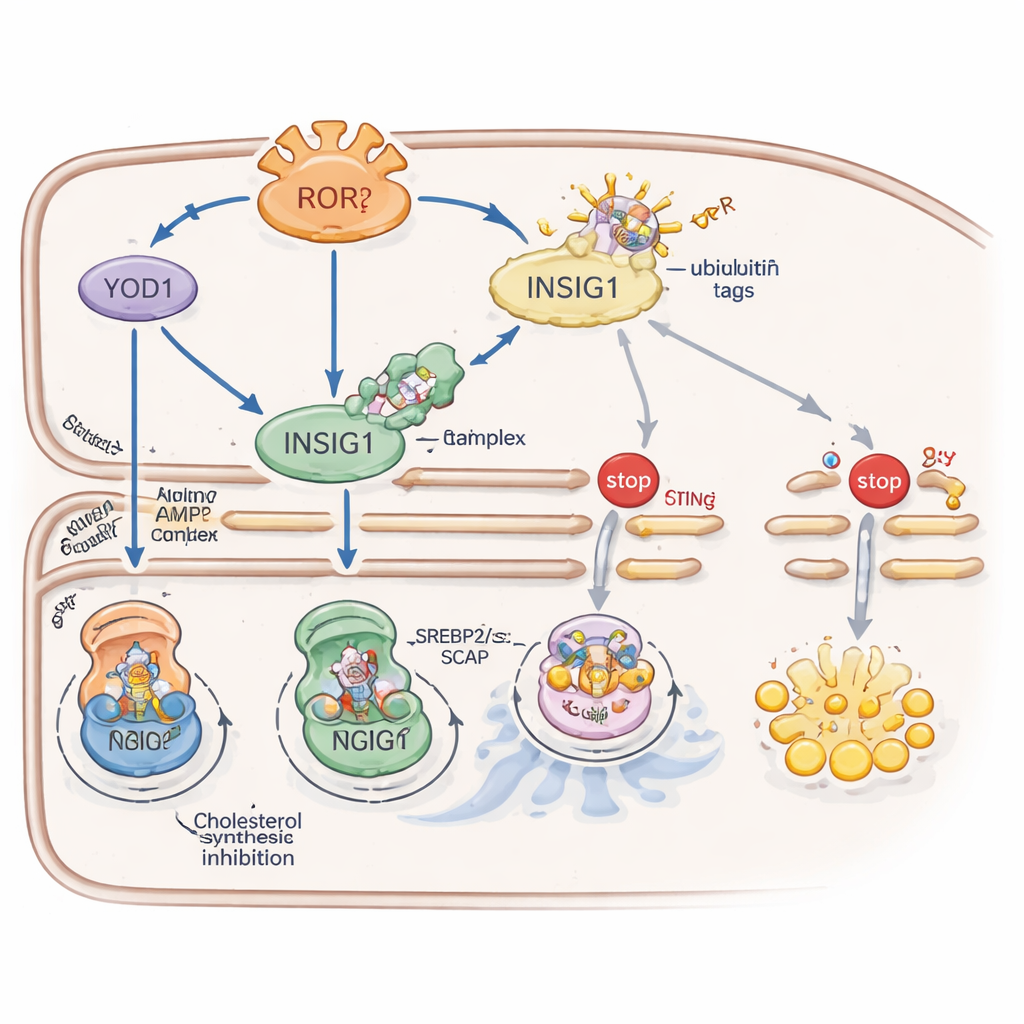
Quand l’interrupteur protecteur tombe en panne dans le diabète et le vieillissement
Dans un environnement diabétique — hyperglycémie et excès de lipides, stress oxydatif et dommages à l’ADN — plusieurs mécanismes conspirent pour éteindre RORγ. Une protéine liant l’ADN appelée CTCF devient plus active et réprime le gène RORγ, réduisant sa production. Parallèlement, une signalisation AMPK altérée et une activité réduite d’un autre régulateur, SIRT1, diminuent la translocation de RORγ vers le noyau et affaiblissent son ancrage sur les gènes cibles. Chez des souris génétiquement modifiées pour être déficientes en RORγ uniquement dans les cellules tubulaires, le diabète et le vieillissement ont entraîné une accumulation de cholestérol, une inflammation, une fibrose et des marqueurs de sénescence beaucoup plus marquées, confirmant que la perte de cet interrupteur accélère directement les lésions rénales.
Réactiver RORγ comme option thérapeutique potentielle
Parce que RORγ est affaibli mais pas totalement absent dans la maladie, les auteurs ont testé si restaurer son activité pouvait protéger les reins. L’apport supplémentaire de RORγ spécifiquement dans les cellules tubulaires, ou l’administration d’exosomes chargés en protéine RORγ, a amélioré la structure et la fonction rénales chez des souris diabétiques et âgées : la fuite d’albumine a diminué, la fibrose s’est atténuée, et l’activité des gènes liés au cholestérol et à l’inflammation a baissé. Ils ont aussi identifié un composé naturel issu de Ganoderma lucidum (un champignon médicinal), appelé ganodermanontriol, qui se lie à RORγ et renforce son activité. Chez des souris diabétiques, ce composé a renforcé les voies en aval de RORγ, maîtrisé la production de cholestérol et la signalisation STING, et atténué les lésions rénales.
Ce que cela signifie pour les futurs traitements rénaux
Ce travail révèle RORγ comme un coordinateur central reliant le statut énergétique de la cellule rénale à la gestion des lipides et aux réponses immunitaires innées. Lorsqu’il est actif, il stabilise INSIG1 et empêche à la fois la synthèse du cholestérol et les alarmes inflammatoires de dérailler. Lorsqu’il est supprimé, comme dans le diabète et le vieillissement, les reins deviennent vulnérables à la surcharge lipidique, à l’inflammation chronique et à la fibrose. En montrant que RORγ peut être réactivé par délivrance génique, approches basées sur des exosomes ou agonistes de petites molécules, l’étude met en lumière une stratégie prometteuse pour ralentir ou prévenir la néphropathie diabétique et le déclin rénal lié à l’âge.
Citation: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Mots-clés: maladie rénale diabétique, métabolisme du cholestérol, immunité innée, rein vieillissant, récepteurs nucléaires