Clear Sky Science · nl
Energieregulerend molecuul RORγ reguleert cholesterolmetabolisme en immuunsignalen bij diabetische nierziekte en veroudering
Waarom dit onderzoek belangrijk is voor mensen met diabetes en verouderende nieren
Diabetische nierziekte en de natuurlijke veroudering van de nieren zijn twee van de belangrijkste oorzaken waardoor mensen uiteindelijk dialyse of een transplantatie nodig hebben. Deze studie onthult een eerder onbekende "energie-sensorische schakelaar" binnen nierbuizencellen die helpt cholesterol en ontsteking onder controle te houden. Wanneer deze schakelaar, een molecuul genaamd RORγ, uitgeschakeld raakt, hoopt vet en ontstekingsschade zich op in de nieren. Wanneer hij weer geactiveerd wordt, worden de nieren beschermd. Inzicht in dit regelsysteem wijst op nieuwe manieren om nierschade bij zowel diabetes als veroudering te vertragen.
De verborgen verbinding tussen energiegebruik, vet en nierbeschadiging
Nierbuizen voeren veel van het opruimwerk van het lichaam uit en verbruiken veel energie om dat te doen. Bij zowel diabetes als veroudering hopen deze cellen overtollige lipiden, vooral cholesterol, op en raken ze ontstoken en verhard. De auteurs onderzochten nierweefsel van diabetische muizen, oudere muizen en mensen met diabetes. In alle drie vonden ze dat RORγ — een nucleair eiwit dat cellen helpt energie te voelen en genen te reguleren — consequent verlaagd was, vooral in buizencellen. Lagere RORγ-niveaus waren geassocieerd met slechtere nierfunctie, meer littekenvorming en hogere markers van celveroudering, wat suggereert dat RORγ normaal gesproken als beschermer van de tubulaire gezondheid fungeert. 
Hoe RORγ de aanmaak van cholesterol en immuunalarmen onder controle houdt
Het team ontdekte dat RORγ tubulecellen beschermt door een ander eiwit, INSIG1, te stabiliseren, dat in het membraan van een intern compartiment, het endoplasmatisch reticulum, zit. INSIG1 fungeert normaal als poortwachter en voorkomt dat een cholesterolbevorderende factor (SREBP2) en een ontstekingsactiverende sensor (STING) naar het Golgi-apparaat reizen — het verzendcentrum van de cel — waar ze volledig actief worden. Bij diabetes of veroudering, wanneer RORγ laag is, wordt INSIG1 snel gemarkeerd voor afbraak en afgebroken, faalt de poort en nemen zowel cholesterolsynthese als ontstekingssignalen sterk toe.
De twee hulp-routes die RORγ gebruikt om INSIG1 te stabiliseren
RORγ versterkt INSIG1 via twee aanvullende hulpmechanismen. Ten eerste schakelt het een eiwit genaamd YOD1 in dat ubiquitine-tags — moleculaire "verwijder mij"-signalen — van INSIG1 verwijdert, waardoor de afbraak vertraagt. Ten tweede verhoogt RORγ de activiteit van een energiesensorenzym, AMPK, door de niveaus van een scaffold-eiwit genaamd CAB39 te vergroten dat de upstream-activator van AMPK samenbrengt. Actief AMPK voegt vervolgens een fosfaatgroep toe aan INSIG1 op een specifieke plaats, wat de interactie met een enzym dat het anders zou richten op afbraak verzwakt. Gezamenlijk laten YOD1 en AMPK INSIG1 langer bestaan, waardoor zowel cholesterolsynthese als STING-gedreven immuunactiviteit strak worden geremd. 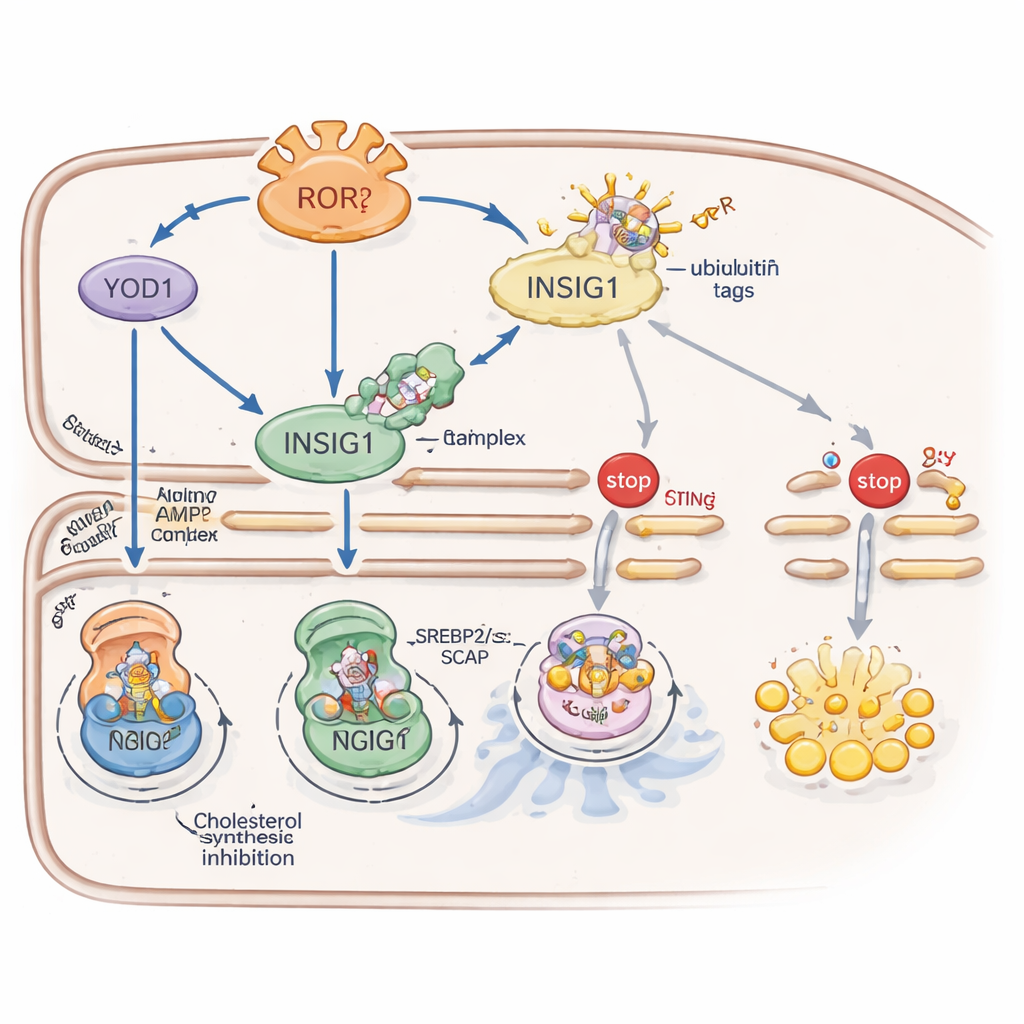
Wanneer de beschermende schakel faalt bij diabetes en veroudering
In een diabetische omgeving — hoge suikers en vetten, oxidatieve stress en DNA-schade — werken meerdere mechanismen samen om RORγ uit te schakelen. Een DNA-bindend eiwit genaamd CTCF wordt actiever en drukt het RORγ-gen neer, waardoor de productie afneemt. Tegelijkertijd verminderen aangetaste AMPK-signalen en verminderde activiteit van een andere regulator, SIRT1, de beweging van RORγ naar de kern en verzwakken ze zijn binding aan doelgenen. In muizen die zodanig gemodificeerd zijn dat ze RORγ alleen in tubulecellen missen, veroorzaakten diabetes en veroudering veel sterkere cholesterolophoping, ontsteking, fibrose en markers van cellulaire senescentie, wat bevestigt dat het verlies van deze schakelaar direct de nierbeschadiging versnelt.
RORγ weer activeren als potentiële therapie
Aangezien RORγ verzwakt maar niet volledig afwezig is bij ziekte, testten de auteurs of het herstellen van zijn activiteit de nieren kon beschermen. Het gericht toedienen van extra RORγ aan tubulecellen, of het leveren van exosomen geladen met RORγ-eiwit, verbeterde nierstructuur en -functie bij diabetische en oudere muizen: albumineverlies nam af, littekenvorming nam af en cholesterol- en ontstekingsgenen werden minder actief. Ze identificeerden ook een natuurlijke verbinding uit Ganoderma lucidum (een geneeskrachtige paddenstoel), ganodermanontriol genoemd, die aan RORγ bindt en zijn activiteit versterkt. Bij diabetische muizen versterkte deze verbinding de downstream-paden van RORγ, temperde cholesterolsynthese en STING-signalerng en verzachtte nierschade.
Wat dit betekent voor toekomstige nierbehandelingen
Dit werk onthult RORγ als een centrale coördinator die de energiestatus van de niercel koppelt aan vetverwerking en aangeboren immuunreacties. Wanneer hij actief is, stabiliseert hij INSIG1 en voorkomt hij dat zowel cholesterolsynthese als immuunalarmen uit de hand lopen. Wanneer hij onderdrukt is, zoals bij diabetes en veroudering, worden nieren kwetsbaar voor lipidestapeling, chronische ontsteking en littekenvorming. Door aan te tonen dat RORγ opnieuw geactiveerd kan worden met genlevering, exosoom-gebaseerde benaderingen of kleine-molecuulagonisten, benadrukt de studie een veelbelovende nieuwe strategie om diabetische nierziekte en leeftijdsgebonden nierachteruitgang te vertragen of te voorkomen.
Bronvermelding: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Trefwoorden: diabetische nierziekte, cholesterolmetabolisme, innate immuniteit, verouderende nier, nucleaire receptoren