Clear Sky Science · ru
Молекула, отслеживающая энергию RORγ, регулирует метаболизм холестерина и иммунную сигнализацию при диабетической болезни почек и старении
Почему это исследование важно для людей с диабетом и стареющими почками
Диабетическая болезнь почек и естественное старение почек — две основные причины, по которым людям в конечном счёте требуется диализ или трансплантация. В этом исследовании обнаружен ранее не распознанный «энергетический переключатель» в клетках почечных канальцев, который помогает контролировать уровни холестерина и воспаление. Когда этот переключатель, молекула RORγ, выключается, в почках накапливаются жир и воспалительные повреждения. При его повторной активации почки оказываются защищёнными. Понимание этой системы управления указывает на новые подходы к замедлению повреждения почек при диабете и старении.
Скрытая связь между расходом энергии, жиром и повреждением почек
Канальцы почек выполняют большую часть «уборочной» работы организма и требуют для этого большого количества энергии. При диабете и старении эти клетки накапливают избыточные липиды, особенно холестерин, и становятся воспалёнными и рубцованными. Авторы изучили ткань почек у диабетических мышей, старых мышей и людей с диабетом. Во всех трёх группах они обнаружили устойчивое снижение RORγ — ядерного белка, помогающего клеткам ощущать энергетический статус и регулировать гены — особенно в клетках канальцев. Низкие уровни RORγ коррелировали с худшей функцией почек, большим количеством фиброза и повышенными маркерами клеточного старения, что указывает на то, что RORγ обычно действует как защитник здоровья канальцев. 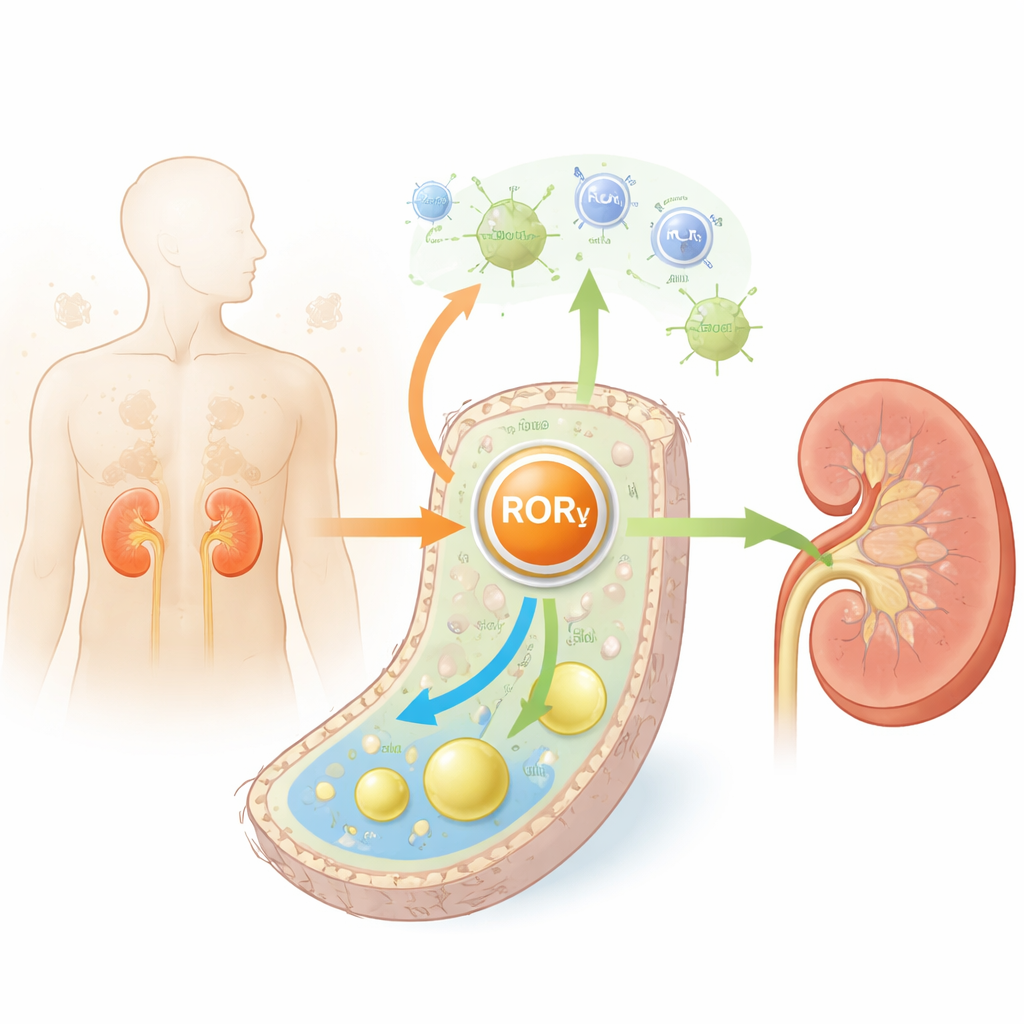
Как RORγ сдерживает синтез холестерина и иммунные сигнализации
Команда показала, что RORγ защищает клетки канальцев, стабилизируя другой белок — INSIG1, расположенный в мембране внутренней структуры, называемой эндоплазматическим ретикулумом. INSIG1 обычно выполняет роль стража, не давая фактору, стимулирующему холестерин (SREBP2), и датчику воспаления (STING) переместиться в аппарат Гольджи, где они становятся полностью активными. При диабете или старении, когда RORγ снижен, INSIG1 быстро помечается для разрушения и разрушается, «ворота» дают сбой, и синтез холестерина вместе с воспалительной сигнализацией резко возрастает.
Два вспомогательных пути, которыми RORγ стабилизирует INSIG1
RORγ укрепляет INSIG1 через два взаимодополняющих механизма. Во-первых, он активирует белок YOD1, который удаляет метки убиквитина — молекулярные «пометь и уничтожь» сигналы — с INSIG1, замедляя его деградацию. Во-вторых, RORγ повышает активность энергетического сенсора AMPK, увеличивая уровни каркасного белка CAB39, который собирает активатор AMPK. Активный AMPK затем фосфорилирует INSIG1 в определённом участке, ослабляя его взаимодействие с ферментом, нацеленным на разрушение. Вместе YOD1 и AMPK продлевают срок жизни INSIG1, удерживая синтез холестерина и STING-опосредованную иммунную активность под строгим контролем. 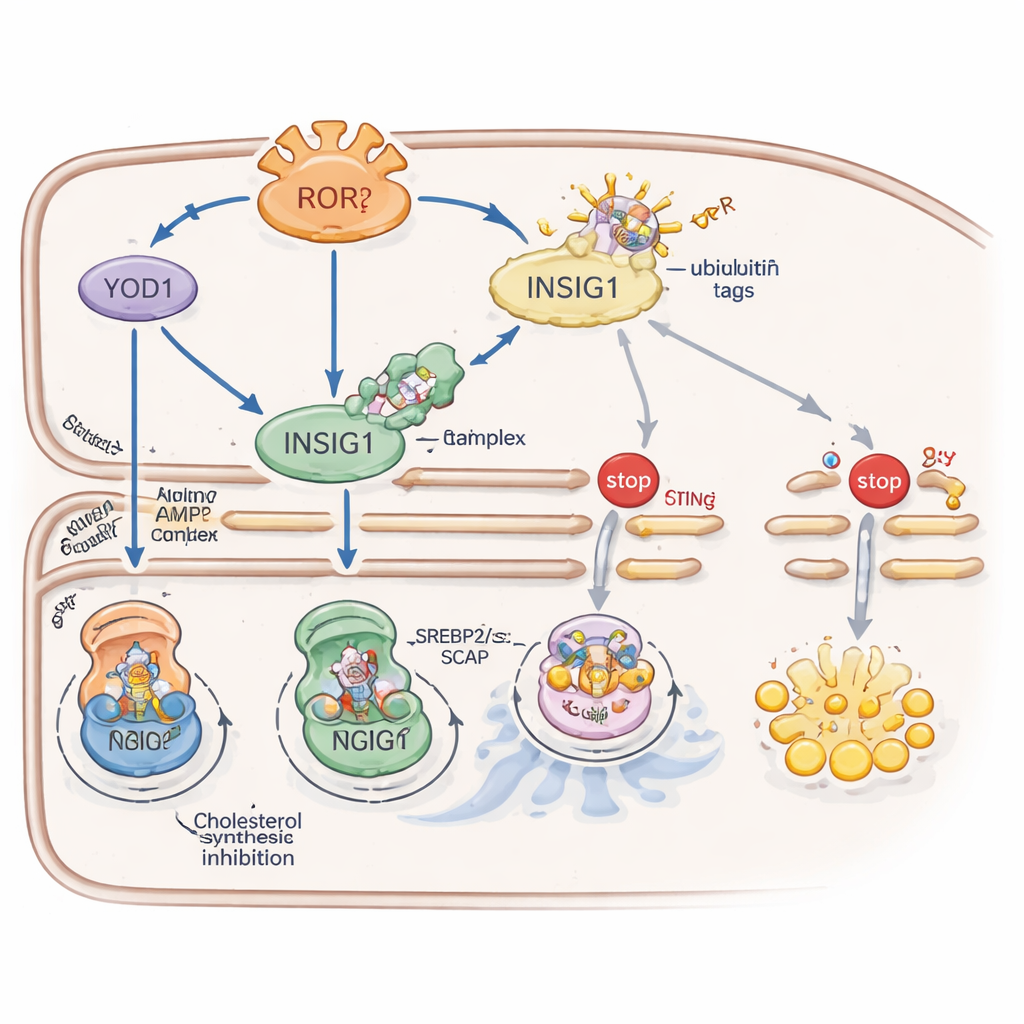
Когда защитный переключатель выходит из строя при диабете и старении
В диабетической среде — при высоком содержании сахара и жиров, окислительном стрессе и повреждении ДНК — несколько механизмов сговариваются, чтобы отключить RORγ. Белок, связывающий ДНК, CTCF, становится более активным и подавляет ген RORγ, снижая его экспрессию. Одновременно нарушенная сигнализация AMPK и сниженная активность другого регулятора, SIRT1, уменьшают транспорт RORγ в ядро и ослабляют его влияние на целевые гены. У мышей, у которых RORγ удалён только в клетках канальцев, диабет и старение вызывали значительно более выраженное накопление холестерина, воспаление, фиброз и маркеры клеточного старения, что подтверждает: потеря этого переключателя напрямую ускоряет повреждение почек.
Активация RORγ как потенциальная терапия
Поскольку при болезни RORγ ослаблен, но не полностью отсутствует, авторы проверили, можно ли восстановить его активность для защиты почек. Доставка дополнительного RORγ непосредственно в клетки канальцев или применение экзосом, загруженных белком RORγ, улучшали структуру и функцию почек у диабетических и старых мышей: уменьшалось выделение белка с мочой, снижался фиброз, а активность генов, связанных с холестерином и воспалением, падала. Они также выявили натуральное соединение из Ganoderma lucidum (лекарственного гриба), ганодерманонтриол, которое связывается с RORγ и усиливает его активность. У диабетических мышей это соединение активировало пути, управляемые RORγ, сдерживало синтез холестерина и сигнализацию STING и ослабляло повреждение почек.
Что это значит для будущих терапий почек
Эта работа выявляет RORγ как центрального координатора, который связывает энергетический статус клеток почечных канальцев с обработкой липидов и реакциями врожденного иммунитета. В активном состоянии он стабилизирует INSIG1 и не допускает неконтролируемого увеличения синтеза холестерина и воспалительных сигналов. При угнетении, как при диабете и старении, почки становятся уязвимы к перегрузке липидами, хроническому воспалению и фиброзу. Демонстрация того, что RORγ можно реактивировать с помощью генной доставки, экзосом или малых молекул-агонистов, подчёркивает многообещающую стратегию для замедления или предотвращения диабетической болезни почек и возрастного снижения функции почек.
Цитирование: Liang, Z., Xiang, J., Yang, G. et al. Energy-sensing molecule RORγ regulates cholesterol metabolism and immune signaling in diabetic kidney disease and aging. Nat Commun 17, 2906 (2026). https://doi.org/10.1038/s41467-026-69724-2
Ключевые слова: диабетическая болезнь почек, метаболизм холестерина, врожденный иммунитет, стареющая почка, ядерные рецепторы