Clear Sky Science · sv
En reversibel allosterisk hämmare av GlyT2 för neuropatisk smärta utan on‑target‑biverkningar
Nytt hopp för svårbehandlad nervsmärta
Neuropatisk smärta — ihållande smärta orsakad av nervskada — svarar ofta dåligt på standardbehandlingar och driver patienter mot långvarig opioidanvändning. Denna studie presenterar en ny kandidatmolekyl som dämpar nervsignaltrafiken i ryggmärgen utan den tunga bördan av beroende eller svåra biverkningar. Genom att visa både hur läkemedlet verkar på atomnivå och hur det beter sig i djur beskriver forskarna en väg mot säkrare, icke‑opioida lindringar för kronisk nervsmärta.
Varför dagens smärtmediciner inte räcker
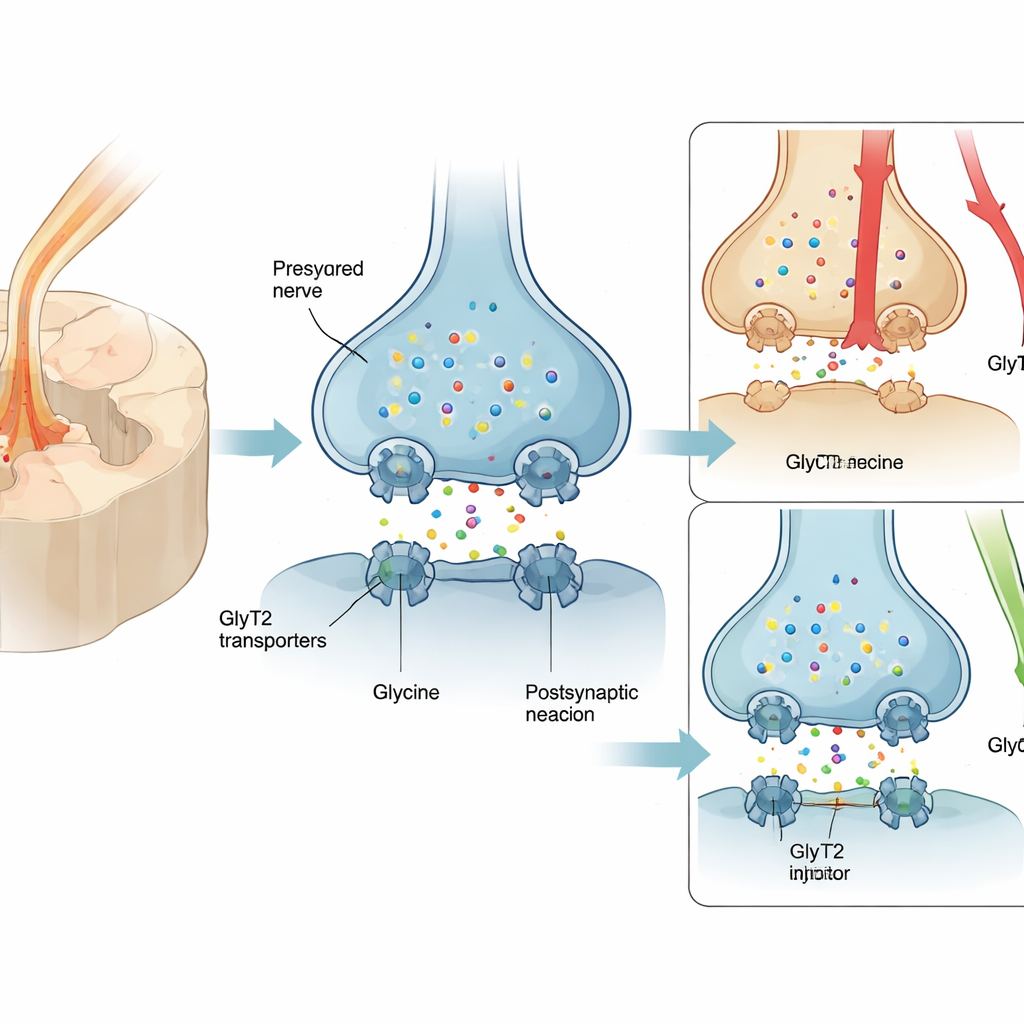
Många med nervsmärta får pregabalin eller närbesläktade läkemedel, men endast ungefär en av fyra patienter upplever betydande lindring och biverkningar som yrsel och dåsighet är vanliga. Som följd används opioider ofta trots risken för beroende. Ett lovande alternativt mål är ett protein kallat GlyT2, som sitter på nervterminaler i ryggmärgen och återupptar glycin, en dämpande signalsubstans som minskar smärtimpulser. Att öka glycin i dessa synapser kan stärka ryggmärgens naturliga ”broms” på smärta. Tidigare GlyT2‑hämmare satt dock för hårt fast i transportören och orsakade allvarliga on‑target‑problem — skakningar, anfall och till och med död hos djur — vilket stod i vägen för klinisk utveckling.
Ett mildare sätt att påverka en viktig smärtspärr
Teamet designade RPI‑GLYT2‑82, en ny förening byggd på skelettet från en potent äldre hämmare, ORG25543, men med avsiktligt svagare bindning och snabbare avgång. I grodyggcellsägg omkonstruerade att uttrycka mänskligt GlyT2 blockerade RPI‑GLYT2‑82 transportören vid sub‑mikromolära koncentrationer men tvättades ut inom minuter, medan ORG25543 förblev kvar mycket längre. Viktigt är att RPI‑GLYT2‑82 föredrog GlyT2 framför den närbesläktade GlyT1, som är utbredd i hela hjärnan, vilket minskar risken för omfattande störning av glycinsignalering. Föreningen blockerade transport även vid höga glycinhalter, vilket bekräftar att den verkar vid en separat regleringsplats snarare än att direkt konkurrera med glycin självt.
Att se smärtbrytaren i atomärt detalj
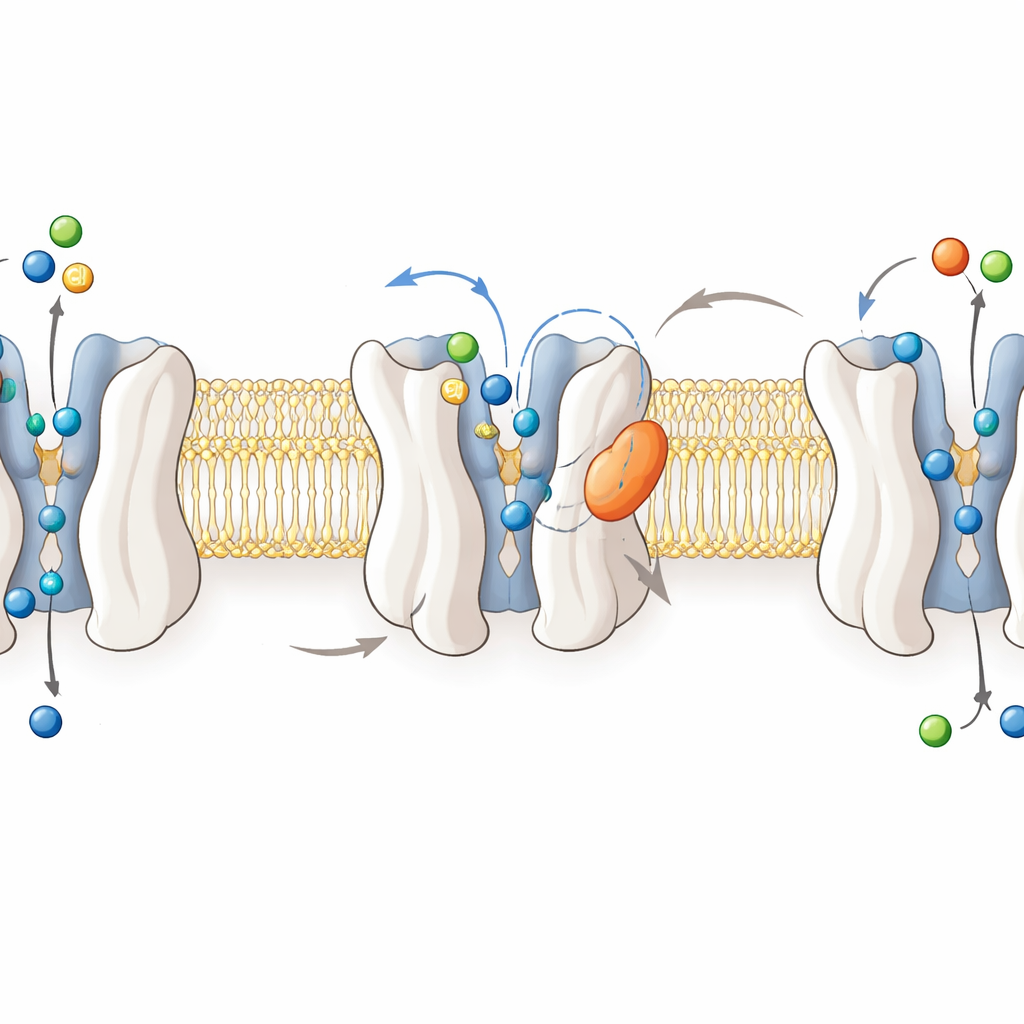
För att förstå hur läkemedlet fungerar löste forskarna högupplösta kryo‑elektronmikroskopiska strukturer av mänskligt GlyT2 i fyra tillstånd: tomt, med glycin bundet, och bundet till antingen ORG25543 eller RPI‑GLYT2‑82. Dessa bilder visar GlyT2 som ett bunt av tolv membran‑spännade helixar som växlar mellan inåtvända och utåtvända former när de förflyttar glycin, natrium och klorid över cellmembranet. Glycin sitter djupt i en central ficka när transportören är ”ockluderad”, skyddad från båda sidor av membranet. I kontrast ligger båda hämmarna i en ”allosterisk” ficka på proteinets utsida, kilade mellan helixar och en flexibel slinga. Där skiljer de åt nyckelport‑restider åt och fäster en viktig ”portvakt”‑leucin utanför den centrala fickan, vilket fryser GlyT2 i en utåtroterad, icke‑transportande konformation.
Vad som gör den nya molekylen säkrare
RPI‑GLYT2‑82 och ORG25543 binder samma allosteriska plats och gör många av samma kontakter, men subtila kemiska förändringar ändrar hur de ligger i fickan. Datorsimuleringar visade att ORG25543 ligger djupt i en tät hydrofob nisch, med ett kompakt ringsystem som passar som en plugg och stabiliserar det låsta tillståndet. RPI‑GLYT2‑82 har däremot en skrymmande, mer polär ring och en mer påfrestad orientering av en av sina aromatiska grupper. Dessa egenskaper försvagar dess grepp, ökar rörligheten i fickan och gör att den lättare drar sig tillbaka till omgivande lösning — vilket förklarar dess lägre potenti men mycket snabbare reversibilitet. Mutationer i närliggande aminosyror som lossar dessa interaktioner påskyndar frisättningen av båda hämmarna ytterligare, vilket understryker hur lokal geometri finjusterar läkemedlets residensstid och därmed säkerheten.
Test av smärtlindring och säkerhet i djur
I musmodeller där ischiasnerven delvis skadats utvecklar djuren mekanisk och kall allodyni — smärta av lätt beröring eller mild nedkylning. När RPI‑GLYT2‑82 gavs genom injektion minskade båda typerna av överkänslighet i en dosberoende manner, med maximal lindring en till tre timmar efter dosering. Vinsten var i vissa tester jämförbar med referensläkemedel som gabapentin eller pregabalin, om än inte överallt överlägsen. Viktigt är att doser som lindrade smärta inte påverkade balans, greppstyrka eller andning, och även en femfaldigt högre dos gav endast övergående, reversibla motoriska och respiratoriska effekter. I ett conditioned place‑preference‑test — en standardmetod för att undersöka läkemedels belönande effekter — utvecklade möss en tydlig preferens för morfin, men inte för RPI‑GLYT2‑82, vilket tyder på låg risk för beroendelika förstärkningseffekter.
Vad detta betyder för framtida smärtbehandlingar
Tillsammans visar arbetet att det är möjligt att ställa in en GlyT2‑hämmare som förstärker kroppens egna hämmande glycinsignalering, lindrar neuropatisk smärta i djur och undviker de svåra on‑target‑biverkningar som hindrade tidigare föreningar. Genom att tillhandahålla detaljerade strukturritningar av GlyT2 i arbete och demonstrera fördelarna med ett reversibelt, allosteriskt angreppssätt öppnar studien dörren för en ny klass av icke‑opioida smärtläkemedel. Med vidare optimering av potens, selektivitet och farmakokinetik kan analoger till RPI‑GLYT2‑82 så småningom ge patienter med kronisk nervsmärta ett effektivt alternativ som är mindre riskfyllt än långvarig opioidterapi.
Citering: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Nyckelord: neuropatisk smärta, glycintransportör, icke‑opioid analgetikum, allosterisk hämning, kryo‑EM‑struktur