Clear Sky Science · it
Un inibitore allosterico reversibile di GlyT2 per il dolore neuropatico senza effetti collaterali on‑target
Una nuova speranza per il dolore nervoso ostinato
Il dolore neuropatico — dolore persistente causato da danno nervoso — spesso resiste ai trattamenti standard e spinge i pazienti verso l’uso cronico di oppiacei. Questo studio presenta un nuovo candidato farmaco a piccola molecola che attenua il traffico di segnali nervosi nel midollo spinale senza il pesante fardello di dipendenza o gravi effetti collaterali. Rivelando sia il meccanismo d’azione a livello atomico sia il comportamento negli animali, i ricercatori delineano una strada verso un sollievo non oppioide e più sicuro per il dolore cronico da nervo.
Perché i farmaci attuali non bastano
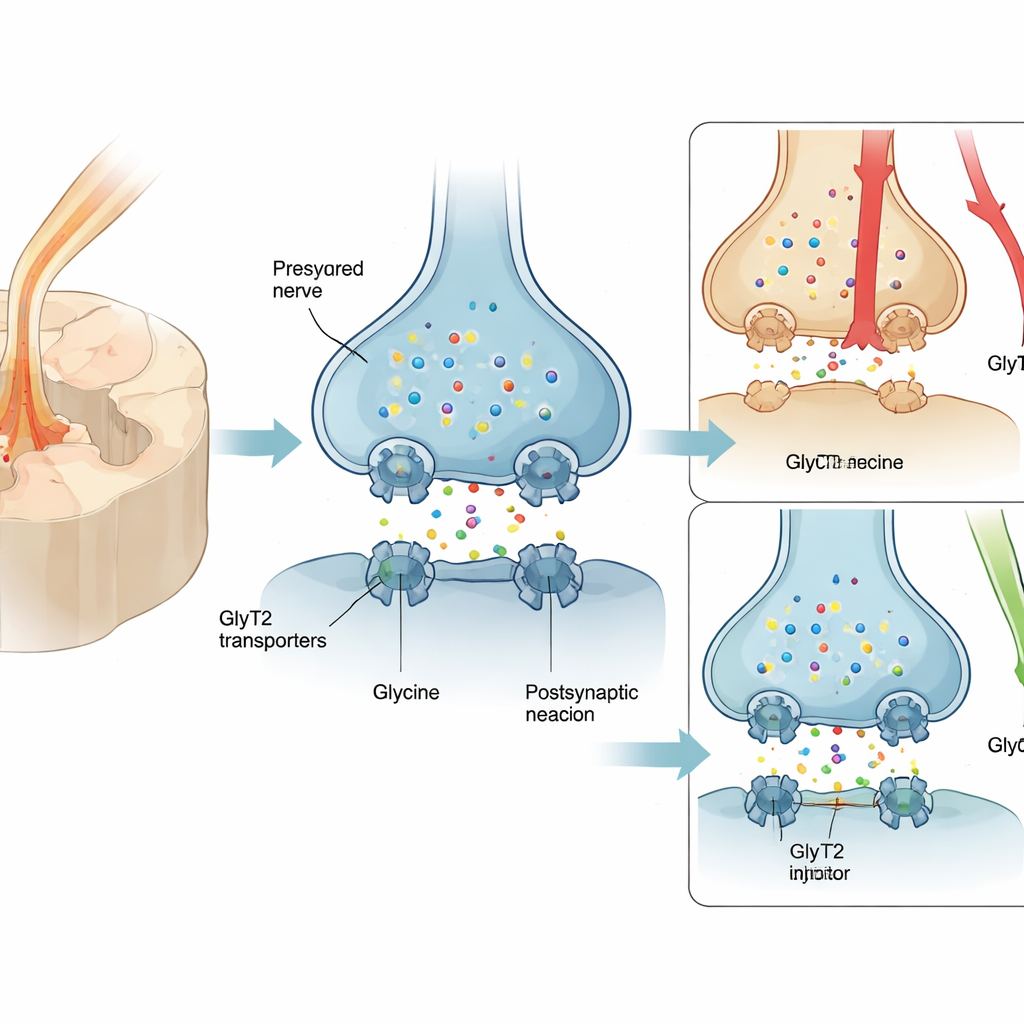
Molte persone con dolore neuropatico ricevono prescrizioni di pregabalin o farmaci affini, ma solo circa uno su quattro ottiene un sollievo significativo, e effetti collaterali come vertigini e sonnolenza sono comuni. Di conseguenza, gli oppiacei vengono spesso impiegati nonostante il rischio di dipendenza. Un bersaglio alternativo promettente è una proteina chiamata GlyT2, presente sulle terminazioni nervose nel midollo spinale e responsabile del riciclo della glicina, un mediatore chimico calmante che attenua i segnali di dolore. Aumentare la glicina intorno a queste sinapsi può rafforzare i “freni” naturali del midollo sul dolore. Tuttavia, i precedenti bloccanti di GlyT2 si legavano troppo saldamente al trasportatore e causarono seri problemi on‑target — tremori, crisi e persino morte negli animali — bloccandone lo sviluppo clinico.
Un modo più dolce per modulare una chiave del dolore
Il gruppo ha progettato RPI‑GLYT2‑82, un nuovo composto costruito sullo scaffold di un potente inibitore più vecchio, ORG25543, ma intenzionalmente tarato per legarsi meno fortemente e rilasciarsi più rapidamente. In cellule d’uovo di rana ingegnerizzate per esprimere GlyT2 umano, RPI‑GLYT2‑82 ha bloccato il trasportatore a concentrazioni sub‑micromolari ma è stato lavato via in pochi minuti, mentre ORG25543 è rimasto legato molto più a lungo. È cruciale che RPI‑GLYT2‑82 preferisca GlyT2 rispetto al suo stretto parente GlyT1, diffuso in tutto il cervello, riducendo il rischio di una vasta alterazione della segnalazione della glicina. Il composto ha bloccato il trasporto anche in presenza di elevate concentrazioni di glicina, confermando che agisce in un sito di controllo separato invece di competere direttamente con la glicina stessa.
Osservare l’interruttore del dolore a dettaglio atomico
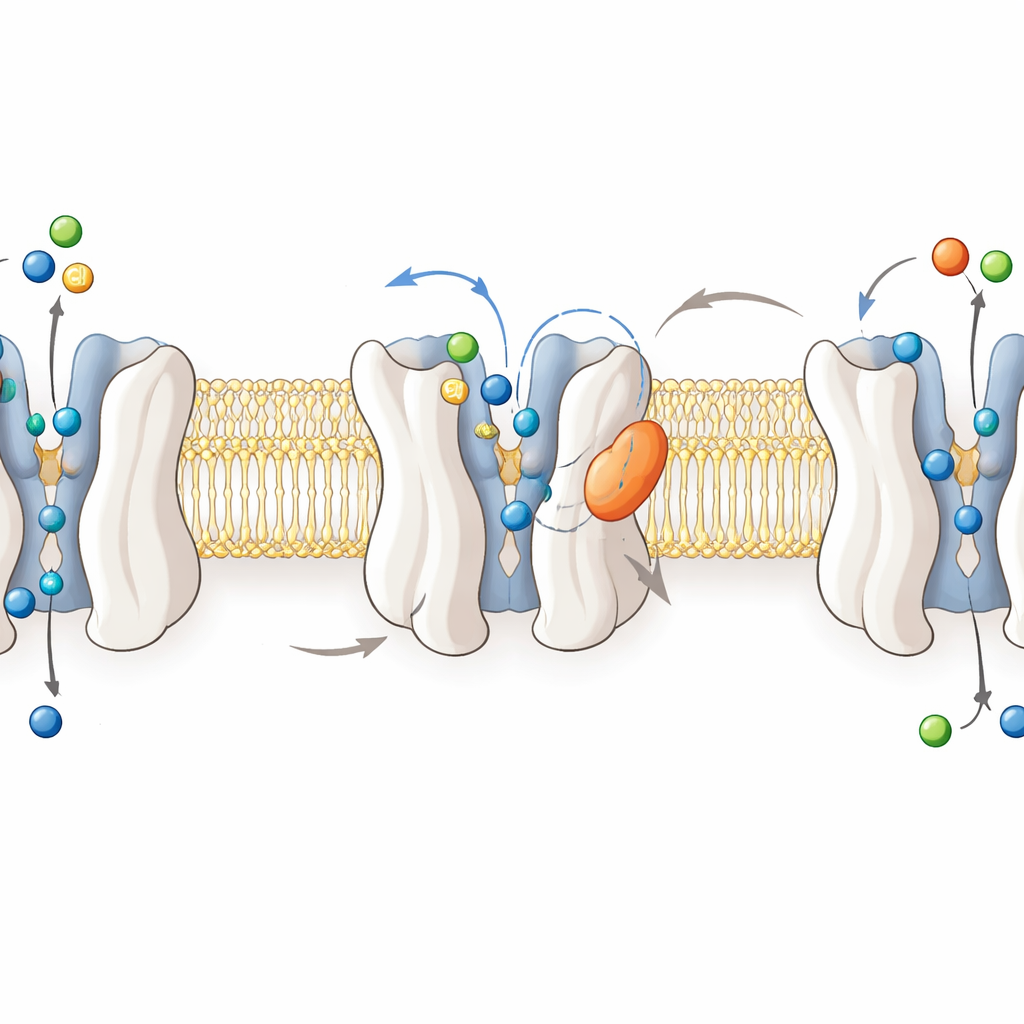
Per comprendere il funzionamento del farmaco, i ricercatori hanno risolto strutture ad alta risoluzione mediante crio‑microscopia elettronica di GlyT2 umano in quattro stati: vuoto, legato alla glicina e associato sia a ORG25543 che a RPI‑GLYT2‑82. Queste immagini mostrano GlyT2 come un fascio di dodici eliche transmembrana che oscillano tra conformazioni rivolte all’interno e all’esterno mentre trasportano glicina, sodio e cloruro attraverso la membrana cellulare. La glicina si trova in profondità in una tasca centrale quando il trasportatore è “occluso”, schermata da entrambi i lati della membrana. Al contrario, entrambi gli inibitori alloggiano in una tasca allosterica esterna alla proteina, incuneati tra eliche e un anello flessibile. Lì separano residui chiave della porta e fissano una leucina “portinaia” importante all’esterno della tasca centrale, bloccando GlyT2 in una posa aperta verso l’esterno e non trasportante.
Cosa rende la nuova molecola più sicura
RPI‑GLYT2‑82 e ORG25543 si legano allo stesso sito allosterico e stabiliscono molti contatti simili, ma sottili modifiche chimiche ne cambiano la sistemazione nella tasca. Simulazioni al computer hanno rivelato che ORG25543 si incunea profondamente in una nicchia idrofobica compatta, con un sistema ad anelli che calza come un tappo e stabilizza lo stato bloccato. Al contrario, RPI‑GLYT2‑82 porta un anello più voluminoso e più polare e un orientamento più tensionato di uno dei suoi gruppi aromatici. Queste caratteristiche indeboliscono la sua presa, aumentano il movimento all’interno della tasca e la rendono più propensa a tornare nella soluzione circostante — spiegando la sua minore potenza ma la reversibilità molto più rapida. Mutazioni in amminoacidi vicini che allentano ulteriormente queste interazioni accelerano il rilascio di entrambi gli inibitori, sottolineando come la geometria locale regoli il tempo di permanenza del farmaco e, di conseguenza, la sicurezza.
Testare sollievo dal dolore e sicurezza negli animali
In modelli murini in cui il nervo sciatico è parzialmente danneggiato, gli animali sviluppano allodinia meccanica e al freddo — dolore da lieve tocco o da lieve raffreddamento. Somministrato per iniezione, RPI‑GLYT2‑82 ha ridotto entrambi i tipi di ipersensibilità in modo dose‑dipendente, con il picco di sollievo che compare una‑tre ore dopo la somministrazione. Il grado di beneficio è stato simile a quello dei farmaci di riferimento gabapentin o pregabalin in alcuni test, sebbene non superiore in assoluto. Importante, dosi che alleviavano il dolore non hanno compromesso equilibrio, forza di presa o respirazione, e anche una dose cinque volte superiore ha causato solo effetti motori e respiratori transitori e reversibili. In un test di preferenza condizionata del luogo — un metodo standard per sondare la ricompensa da farmaco — i topi hanno sviluppato una chiara preferenza per la morfina, ma non per RPI‑GLYT2‑82, suggerendo un basso rischio di effetti rinforzanti simili alla dipendenza.
Cosa significa per i futuri trattamenti del dolore
Nel complesso, il lavoro dimostra che è possibile calibrare un inibitore di GlyT2 che potenzia la segnalazione inibitoria naturale della glicina, allevia il dolore neuropatico negli animali ed evita i gravi effetti on‑target che avevano ostacolato i composti precedenti. Fornendo dettagliate mappe strutturali di GlyT2 in azione e dimostrando i vantaggi di un approccio allosterico e reversibile, lo studio apre la porta a una nuova classe di analgesici non‑oppioidi. Con ulteriori ottimizzazioni di potenza, selettività e farmacocinetica, analoghi di RPI‑GLYT2‑82 potrebbero infine offrire ai pazienti con dolore cronico da nervo un’opzione efficace meno rischiosa rispetto alla terapia oppiacea a lungo termine.
Citazione: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Parole chiave: dolore neuropatico, trasportatore della glicina, analgesico non‑opioide, inibizione allosterica, struttura cryo‑EM