Clear Sky Science · ar
مثبط آللوستيري قابل للعكس لـ GlyT2 لألم الأعصاب دون آثار جانبية مرتبطة بالمستهدف
أمل جديد لألم الأعصاب العنيد
الألم العصبي—الألم المستمر الناتج عن تلف الأعصاب—غالبًا ما يقاوم العلاجات القياسية ويدفع المرضى نحو استخدام الأفيونات على المدى الطويل. تقدم هذه الدراسة مرشح دوائي جديد صغير الجزيء يقلل من حركة إشارات الأعصاب في الحبل الشوكي دون عبء الإدمان أو الآثار الجانبية الشديدة. من خلال كشف كيفية عمل الدواء على المستوى الذري وسلوكه في الحيوانات، يرسم الباحثون مسارًا نحو تخفيف غير أفيوني وأكثر أمانًا للألم العصبي المزمن.
لماذا تخفق أدوية الألم الحالية
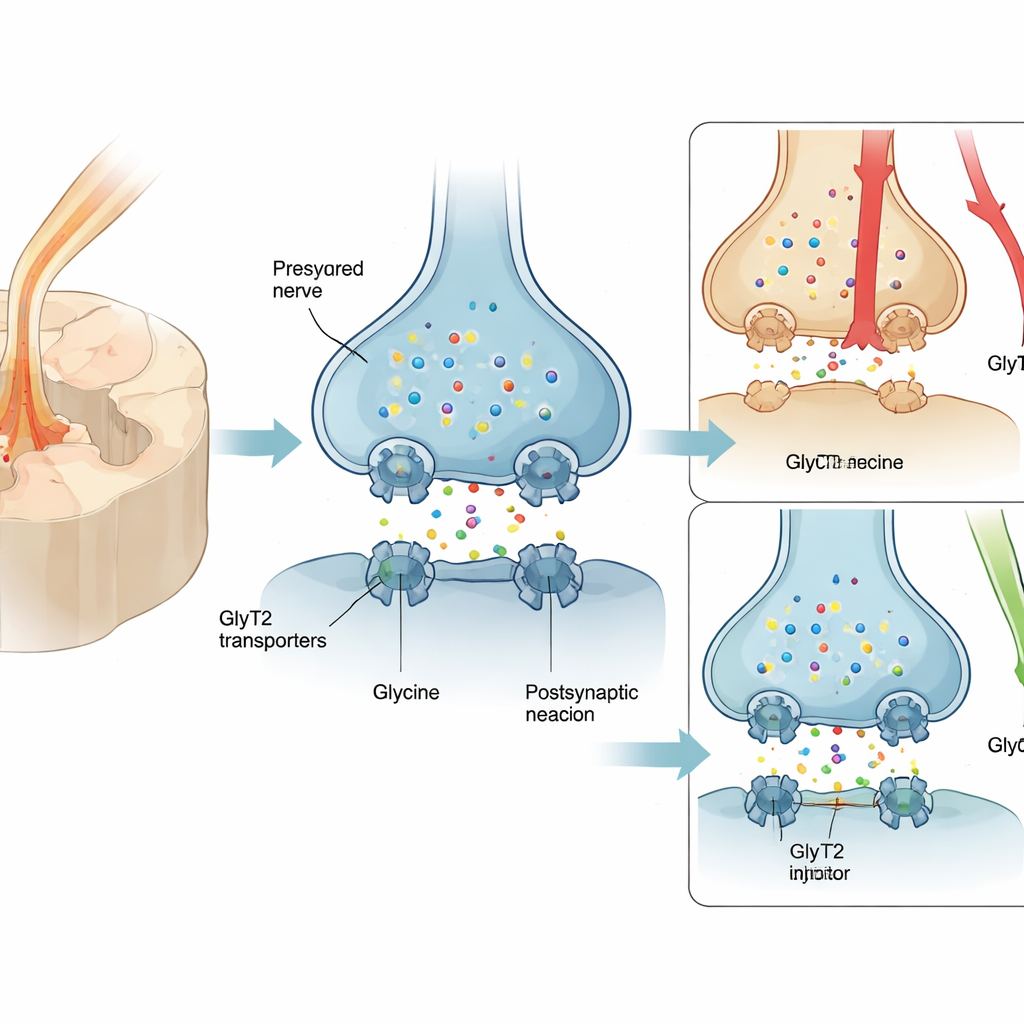
يُوصف للعديد من المصابين بألم الأعصاب بريجابالين أو أدوية قريبة منه، ومع ذلك يحقق حوالي شخص من كل أربعة فقط تخفيفًا ذا مغزى، وتعد آثار جانبية مثل الدوار والنعاس شائعة. نتيجة لذلك تُستخدم الأفيونات كثيرًا رغم خطر الاعتماد. أحد الأهداف الواعدة البديلة هو بروتين يدعى GlyT2، الذي يوجد على النهايات العصبية في الحبل الشوكي ويعيد تدوير الغليسين، الناقل الكيميائي المهدئ الذي يخفف إشارات الألم. زيادة مستوى الغليسين حول هذه المشابك يمكن أن تقوّي "الفرامل" الطبيعية للحبل الشوكي على الألم. لكن مثبطات GlyT2 السابقة التزمت بالناقِل بشدة وتسببت بمشكلات خطيرة مرتبطة بالمستهدف—رجفان، نوبات وحتى وفاة في الحيوانات—مما أعاق تقدمها إلى العيادة.
طريقة ألطف لتحريك بوابة ألم رئيسية
صمم الفريق المركب RPI‑GLYT2‑82، مركبًا جديدًا مبنيًا على هيكل مثبط قديم قوي، ORG25543، لكن تم ضبطه عمدًا ليرتبط بشكل أقل إحكامًا وليطلق بسرعة أكبر. في خلايا بيوض الضفدع المهندَسة لإنتاج GlyT2 البشري، عطل RPI‑GLYT2‑82 الناقل عند تراكيز دون ميكرومولارية لكنه زال خلال دقائق، بينما ظل ORG25543 ملتصقًا لفترة أطول بكثير. والأهم أن RPI‑GLYT2‑82 فضل GlyT2 على القريب منه GlyT1، المنتشر في الدماغ، مما يقلل خطر تعطيل إشارات الغليسين على نطاق واسع. حجب المركب النقل حتى عندما كانت مستويات الغليسين عالية، مما يؤكد أنه يعمل في موقع تحكم منفصل بدلًا من التنافس المباشر مع الغليسين نفسه.
رؤية مفتاح الألم بتفصيل ذري
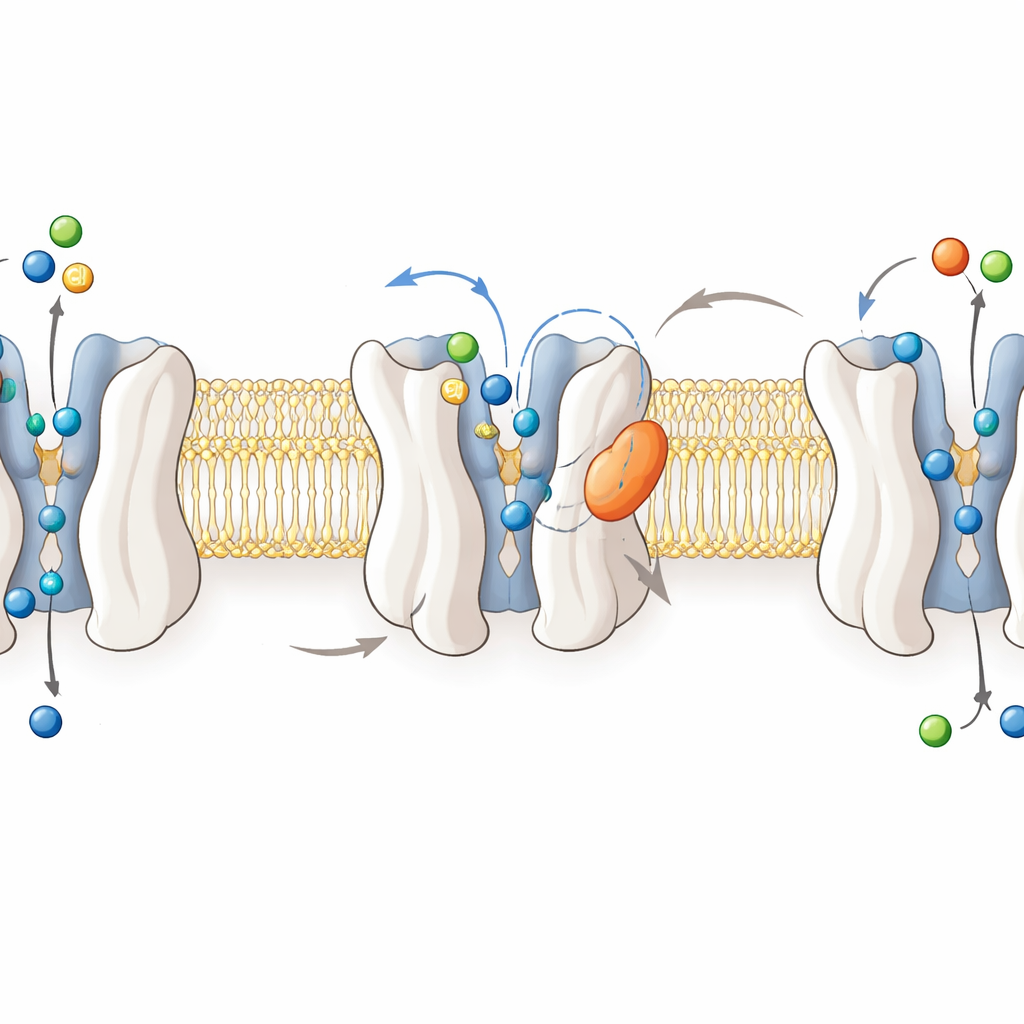
لفهم كيفية عمل الدواء حلل الباحثون هياكل GlyT2 البشري عالية الدقة باستخدام التبريد الإلكتروني المجهري في أربع حالات: خالٍ، حامل للغليسين، ومقيد إما بـ ORG25543 أو RPI‑GLYT2‑82. تُظهر هذه الصور GlyT2 كمجموعة من اثني عشر حلزونًا عابِرًا للغشاء تتأرجح بين أشكال مواجهة للداخل ومواجهة للخارج أثناء نقل الغليسين والصوديوم والكلوريد عبر غشاء الخلية. يجلس الغليسين عميقًا في جيب مركزي عندما يكون الناقل "مغلقًا"، محميًا من جانبي الغشاء. بالمقابل، يترسخ كلا المثبطين في جيب "آلوستيري" في الخارج، محشورين بين الحلزونات وحلقة مرنة. هناك يبعدان بقايا بوابات رئيسية ويضغطان ليوسين "حارس البوابة" خارج الجيب المركزي، مجمدين GlyT2 في وضع مفتوح نحو الخارج وغير ناقل.
ما الذي يجعل الجزيء الجديد أكثر أمانًا
يرتبط كل من RPI‑GLYT2‑82 وORG25543 بنفس الموقع الآلوستيري ويقيمان العديد من الاتصالات نفسها، لكن تعديلات كيميائية طفيفة تغير كيفية تموضعهما في الجيب. كشفت محاكيات الحاسوب أن ORG25543 ينغمس عميقًا في فجوة هيدروفوبية محكمة، بنظام حلقي مضغوط يناسب كالقابس ويثبت حالة القفل. بالمقابل، يحمل RPI‑GLYT2‑82 حلقة أكبر وأكثر قطبية وتوجهًا أكثر توترًا لإحدى مجموعاته العطرية. تضعف هذه السمات قبضته، وتزيد حركته داخل الجيب، وتجعل من المرجح أن يعود إلى المحلول المحيط—مفسرة قوته الأقل لكن قابليته الأسرع للانعكاس. تؤدي طفرات في الأحماض الأمينية القريبة التي تضعف هذه التفاعلات إلى تسريع تحرير كلا المثبطين، مما يبرز كيف تضبط الهندسة المحلية زمن بقاء الدواء ومن ثم السلامة.
اختبار تخفيف الألم والسلامة في الحيوانات
في نماذج فئران تُصاب فيها العصب الوركي بضرر جزئي، تطور الحيوانات فرط تألم ميكانيكي وبرودة—ألم من لمسة خفيفة أو تبريد طفيف. عند إعطائه عن طريق الحقن، خفّض RPI‑GLYT2‑82 كلا نوعي فرط الحساسية بجرعة‑اعتماد، مع ظهور الذروة التخفيفية بعد ساعة إلى ثلاث ساعات من الجرعة. كانت درجة الفائدة مماثلة لأدوية مرجعية مثل غابابنتين أو بريجابالين في اختبارات معينة، وإن لم تكن متفوقة في كل المجالات. والأهم أن الجرعات التي خففت الألم لم تضعف التوازن أو قوة القبضة أو التنفس، وحتى جرعة أعلى خمس مرات أسببت آثارًا حركية وتنفسية عابرة وقابلة للعكس فقط. في اختبار تفضيل المكان المشروط—وهو طريقة معيارية لاختبار المكافأة الدوائية—طورت الفئران تفضيلًا واضحًا للمورفين، لكن ليس لـ RPI‑GLYT2‑82، ما يشير إلى مخاطر منخفضة لآثار تعزيزية شبيهة بالإدمان.
ماذا يعني هذا لعلاجات الألم المستقبلية
تُظهر النتائج معًا أنه من الممكن ضبط مثبط GlyT2 يعزز إشارات الغليسين الكابحة في الجسم، يخفف الألم العصبي في الحيوانات، ويتجنب الآثار الجانبية الشديدة المرتبطة بالمستهدف التي أعاقت المركبات السابقة. من خلال توفير مخططات هيكلية مفصلة لـ GlyT2 أثناء العمل وإظهار فوائد نهج آلوستيري قابل للعكس، تفتح الدراسة الباب لفئة جديدة من مسكنات الألم غير الأفيونية. مع مزيد من تحسين القوة والانتقائية والحركية الدوائية، قد تعطي نظائر RPI‑GLYT2‑82 في نهاية المطاف المرضى المصابين بألم عصبي مزمن خيارًا فعالًا أقل خطورة من العلاج الأفيوني طويل الأمد.
الاستشهاد: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
الكلمات المفتاحية: ألم عصبي, ناقل الغليسين, مسكن غير أفيوني, المنع الآلوستيري, بنية التبريد الإلكتروني المجهري