Clear Sky Science · pt
Um inibidor alostérico reversível de GlyT2 para dor neuropática sem efeitos colaterais no alvo
Nova esperança para dores nervosas persistentes
Dor neuropática — dor duradoura causada por lesão nos nervos — frequentemente resiste aos tratamentos padrão e empurra pacientes para o uso prolongado de opioides. Este estudo apresenta um novo candidato a fármaco de pequena molécula que reduz o tráfego de sinais nervosos na medula espinhal sem o peso do vício ou efeitos colaterais graves. Ao revelar tanto o mecanismo de ação em nível atômico quanto o comportamento em animais, os pesquisadores delineiam um caminho rumo a um alívio mais seguro e não opióide para dor crônica de origem nervosa.
Por que os fármacos atuais deixam a desejar
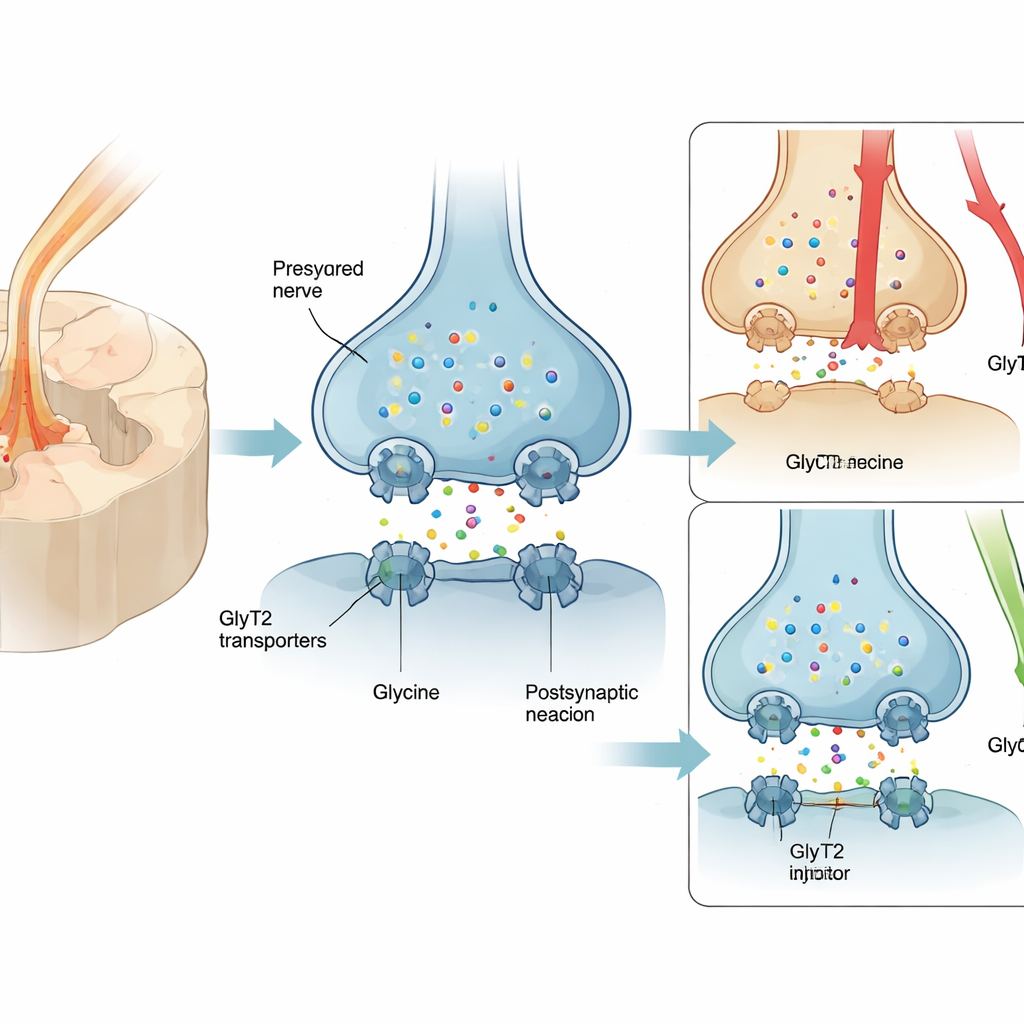
Muitas pessoas com dor nervosa recebem prescrição de pregabalina ou medicamentos relacionados, mas apenas cerca de um em cada quatro pacientes experimenta alívio significativo, e efeitos colaterais como tontura e sonolência são comuns. Como resultado, opioides são frequentemente usados apesar do risco de dependência. Um alvo promissor é uma proteína chamada GlyT2, que fica nas terminações nervosas da medula espinhal e recicla a glicina, um mensageiro químico calmante que atenua sinais de dor. Aumentar a glicina ao redor dessas sinapses pode reforçar os “freios” naturais da medula espinhal sobre a dor. No entanto, bloqueadores anteriores de GlyT2 se ligavam com tanta força ao transportador que causaram problemas sérios no próprio alvo — tremores, convulsões e até morte em animais — barrando seu caminho até a clínica.
Uma maneira mais suave de ajustar um ponto-chave da dor
A equipe projetou RPI‑GLYT2‑82, um novo composto construído a partir do arcabouço de um inibidor antigo e potente, ORG25543, mas intencionalmente ajustado para se ligar menos fortemente e se desligar mais rapidamente. Em ovos de rã modificados para produzir GlyT2 humano, RPI‑GLYT2‑82 bloqueou o transportador em concentrações submicromolares e foi eliminado em minutos, enquanto ORG25543 permaneceu aderido por muito mais tempo. Crucialmente, RPI‑GLYT2‑82 preferiu GlyT2 em relação ao parente próximo GlyT1, amplamente distribuído pelo cérebro, reduzindo o risco de perturbação generalizada da sinalização de glicina. O composto bloqueou o transporte mesmo com níveis altos de glicina, confirmando que age em um sítio de controle separado em vez de competir diretamente com a glicina.
Vendo o interruptor da dor em detalhe atômico
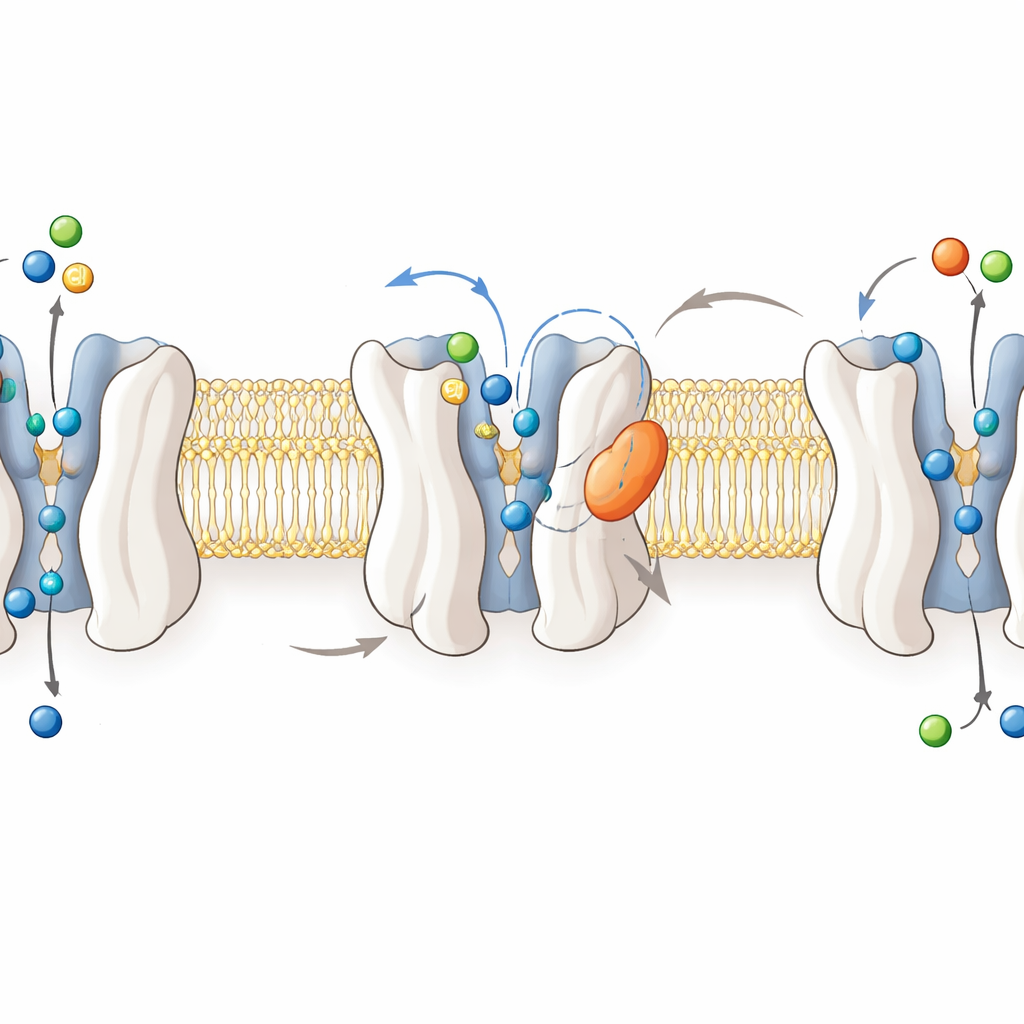
Para entender como o fármaco funciona, os pesquisadores resolveram estruturas de alta resolução por crio‑microscopia eletrônica de GlyT2 humano em quatro estados: vazio, carregando glicina, e ligado a ORG25543 ou RPI‑GLYT2‑82. Essas imagens mostram GlyT2 como um feixe de doze hélices transmembrana que alternam entre formas voltadas para dentro e para fora enquanto movem glicina, sódio e cloreto através da membrana celular. A glicina fica profundamente em um bolso central quando o transportador está “ocluído”, protegida de ambos os lados da membrana. Em contraste, ambos os inibidores se alojam em um bolso “alostérico” na face externa da proteína, encaixados entre hélices e um laço flexível. Ali, eles abrem resíduos-chave do portão e prendem uma leucina “guardião” importante fora do bolso central, congelando GlyT2 em uma conformação aberta para fora e não transportadora.
O que torna a nova molécula mais segura
RPI‑GLYT2‑82 e ORG25543 ligam‑se ao mesmo sítio alostérico e fazem muitos dos mesmos contatos, mas ajustes químicos sutis mudam como se acomodam no bolso. Simulações por computador revelaram que ORG25543 se aloja profundamente em um nicho hidrofóbico justo, com um sistema de anéis compacto que encaixa como uma tampa e estabiliza o estado travado. Em contraste, RPI‑GLYT2‑82 traz um anel mais volumoso e polar e uma orientação mais tensionada de um de seus grupos aromáticos. Essas características enfraquecem sua aderência, aumentam seu movimento dentro do bolso e tornam mais provável que retorne à solução circundante — explicando sua menor potência, mas reversibilidade muito mais rápida. Mutações em aminoácidos próximos que afrouxam essas interações aceleram ainda mais a liberação de ambos os inibidores, ressaltando como a geometria local regula o tempo de residência do fármaco e, consequentemente, a segurança.
Testando alívio da dor e segurança em animais
Em modelos murinos em que o nervo ciático é parcialmente lesionado, os animais desenvolvem alodinia mecânica e ao frio — dor causada por toque leve ou resfriamento moderado. Quando administrado por injeção, RPI‑GLYT2‑82 reduziu ambos os tipos de hipersensibilidade de forma dependente da dose, com alívio máximo aparecendo de uma a três horas após a dosagem. O grau de benefício foi semelhante ao de fármacos de referência como gabapentina ou pregabalina em certos testes, embora não superior em todos os pontos. Importante, doses que aliviaram a dor não prejudicaram equilíbrio, força de preensão ou respiração, e mesmo uma dose cinco vezes maior causou apenas efeitos motores e respiratórios transitórios e reversíveis. Em um teste de preferência de local condicionado — método padrão para investigar recompensa por drogas — os camundongos desenvolveram preferência clara por morfina, mas não por RPI‑GLYT2‑82, sugerindo baixo risco de efeitos reforçadores semelhantes ao vício.
O que isso significa para tratamentos futuros da dor
Em conjunto, o trabalho mostra que é possível ajustar um inibidor de GlyT2 que potencializa a sinalização inibitória natural mediada por glicina, alivia a dor neuropática em animais e evita os graves efeitos colaterais no alvo que prejudicaram compostos anteriores. Ao fornecer plantas estruturais detalhadas de GlyT2 em ação e demonstrar os benefícios de uma abordagem alostérica e reversível, o estudo abre caminho para uma nova classe de analgésicos não opióides. Com otimizações adicionais de potência, seletividade e farmacocinética, análogos de RPI‑GLYT2‑82 poderiam, eventualmente, oferecer aos pacientes com dor nervosa crônica uma opção eficaz e menos arriscada do que a terapia opióide de longo prazo.
Citação: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Palavras-chave: dor neuropática, transportador de glicina, analgésico não opióide, inibição alostérica, estrutura por crio‑EM