Clear Sky Science · ru
Обратимый аллостерический ингибитор GlyT2 для нейропатической боли без побочных эффектов на мишени
Новая надежда для упорной нервной боли
Нейропатическая боль — длительная боль, вызванная повреждением нервов — часто не поддаётся стандартной терапии и толкает пациентов к длительному использованию опиоидов. В этом исследовании представлен новый кандидат в малые молекулы, который снижает передачу нервных сигналов в спинном мозге без тяжёлого груза зависимости или серьёзных побочных эффектов. Показывая как молекулярный механизм действия препарата, так и его поведение в животных, авторы прокладывают путь к более безопасному, неопиоидному облегчению хронической нервной боли.
Почему действующие лекарства не идеальны
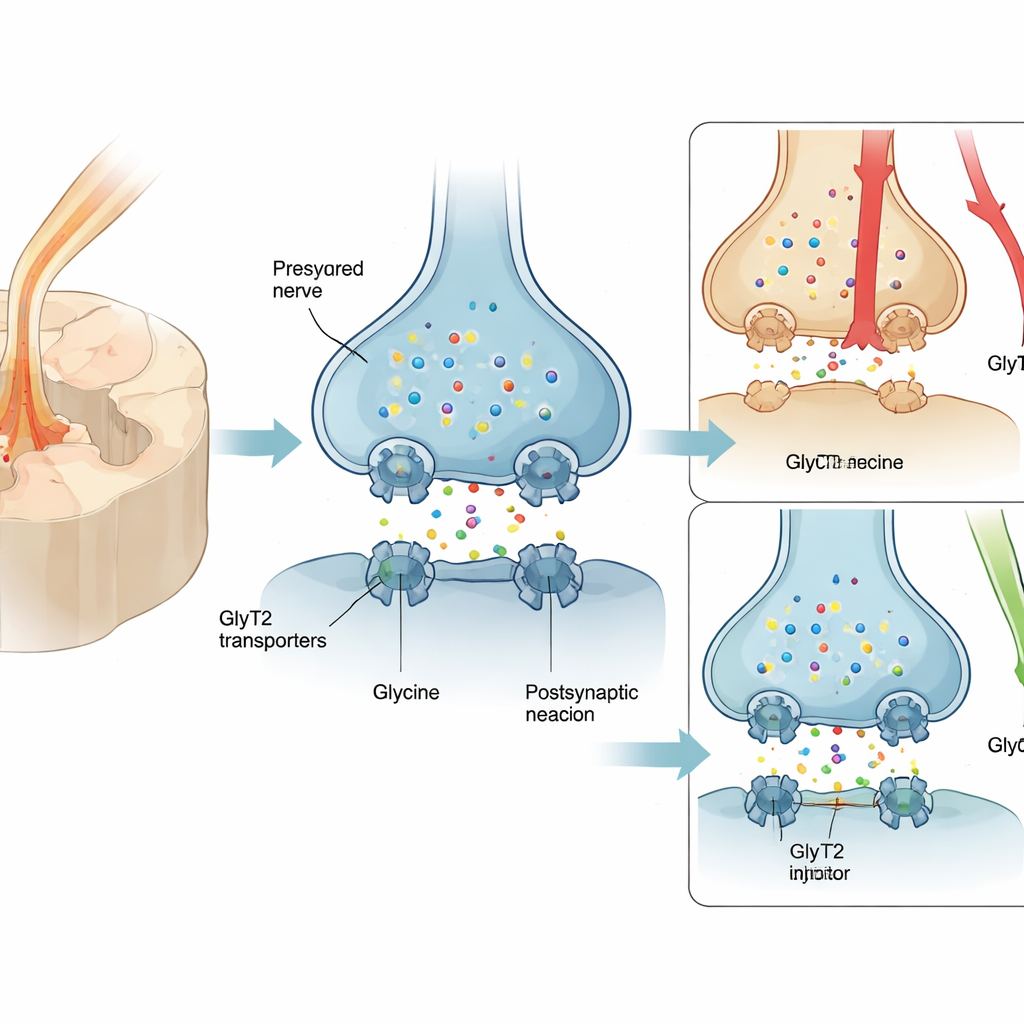
Многим людям с нервной болью назначают прегабалин или родственныe препараты, однако лишь примерно один из четырёх пациентов получает значительное облегчение, и такие побочные эффекты, как головокружение и сонливость, встречаются часто. В результате опиоиды нередко используются, несмотря на риск зависимости. Перспективной альтернативой является белок GlyT2, расположенный на окончаниях нервов в спинном мозге, который утилизирует глицин — тормозной нейромедиатор, ослабляющий болевые сигналы. Повышение уровня глицина у этих синапсов может усилить естественные «тормоза» спинного мозга. Однако прежние ингибиторы GlyT2 слишком прочно связывались с транспортером и вызывали серьёзные эффекты на мишени — тремор, судороги и даже гибель животных — что блокировало их продвижение в клинику.
Более мягкий способ подтолкнуть ключевой болевой «затвор»
Команда разработала RPI‑GLYT2‑82, новое соединение, основанное на скелете мощного старого ингибитора ORG25543, но целенаправленно настроенное так, чтобы связываться слабее и отпускать быстрее. В яйцеклетках лягушки, модифицированных для экспрессии человеческого GlyT2, RPI‑GLYT2‑82 блокировал транспортер в субмикромолярных концентрациях, но смывался в течение минут, тогда как ORG25543 оставался связан значительно дольше. Важно, что RPI‑GLYT2‑82 предпочитал GlyT2 своему близкому родственнику GlyT1, который широко распространён в головном мозге, что снижает риск массового наруше ния глицинергической сигнализации. Соединение блокировало транспорт даже при высоких уровнях глицина, подтверждая, что оно действует в отдельном регуляторном сайте, а не напрямую конкурирует с глицином.
Рассматриваем переключатель боли с атомным разрешением
Чтобы понять механизм действия препарата, исследователи получили структуры человеческого GlyT2 методом крио-электронной микроскопии с высоким разрешением в четырёх состояниях: пустой, с глицином и связанным либо с ORG25543, либо с RPI‑GLYT2‑82. Эти изображения показывают GlyT2 как пучок из двенадцати спиралей, пересекающих мембрану, которые качаются между внутрь- и наружно-ориентированными формами при переносе глицина, натрия и хлора через мембрану. Глицин находится глубоко в центральной карманной области, когда транспортер «окклюдирован», защищённый с обеих сторон мембраны. Напротив, оба ингибитора занимают «аллостерический» карман с внешней стороны белка, зажатые между спиралями и гибкой петлёй. Там они раздвигают ключевые остатки, образующие ворота, и фиксируют важную «шлюзовую» лейциновую группу вне центрального кармана, замораживая GlyT2 в наружно-открытом, не транспортирующем состоянии.
Что делает новую молекулу безопаснее
RPI‑GLYT2‑82 и ORG25543 связываются с тем же аллостерическим участком и устанавливают многие одинаковые контакты, но тонкие химические изменения меняют их положение в кармане. Компьютерные моделирования показали, что ORG25543 глубоко утапливается в плотной гидрофобной ниши, с компактной кольцевой системой, которая садится как пробка и стабилизирует заблокированное состояние. Напротив, RPI‑GLYT2‑82 несёт более громоздкое, более полярное кольцо и более напряжённую ориентацию одного из ароматических фрагментов. Эти особенности ослабляют его захват, увеличивают подвижность внутри кармана и повышают вероятность возвращения в окружающий раствор — что объясняет его меньшую мощность, но гораздо быструю обратимость. Мутации в близлежащих аминокислотах, ослабляющие эти взаимодействия, ещё больше ускоряют высвобождение обоих ингибиторов, подчёркивая, как локальная геометрия настраивает время резиденции лекарства и, следовательно, его безопасность.
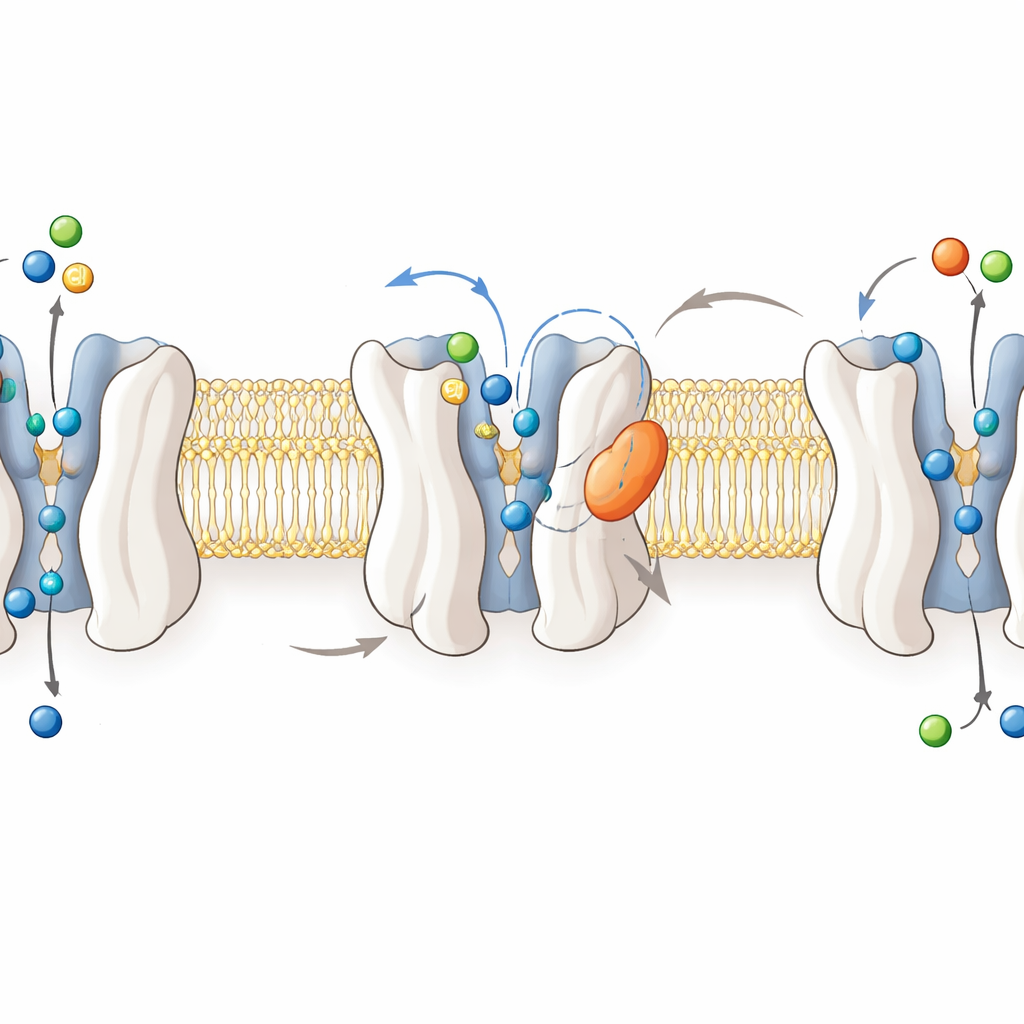
Испытания обезболивания и безопасности на животных
В моделях у мышей с частичным повреждением седалищного нерва животные развивают механическую и холодовую аллодинию — боль при лёгком прикосновении или при слабом охлаждении. При введении инъекцией RPI‑GLYT2‑82 уменьшал оба типа гиперчувствительности в дозозависимой манере, с пиком облегчения через один-три часа после дозы. Степень эффекта была схожа с таковой у референсных препаратов габапентина или прегабалина в ряде тестов, хотя не превосходила их повсеместно. Важно, что дозы, которые снимали боль, не нарушали равновесие, силу хвата или дыхание, и даже пятикратная повышенная доза вызывала лишь кратковременные, обратимые моторные и респираторные эффекты. В тесте обусловленного предпочтения места — стандартном методе оценки наркотического подкрепления — мыши явно проявляли предпочтение морфину, но не RPI‑GLYT2‑82, что свидетельствует о низком риске аддиктивных подкрепляющих эффектов.
Что это означает для будущих методов лечения боли
В совокупности работа показывает, что возможно подобрать ингибитор GlyT2, который усиливает собственную тормозную глицинергическую сигнализацию организма, облегчает нейропатическую боль у животных и избегает тяжёлых побочных эффектов на мишени, мешавших ранее разработкам. Предоставляя подробные структурные чертежи GlyT2 в действии и демонстрируя преимущества обратимого аллостерического подхода, исследование открывает путь к новому классу неопиоидных анальгетиков. С дальнейшей оптимизацией по части мощности, селективности и фармакокинетики аналоги RPI‑GLYT2‑82 в перспективе могут дать пациентам с хронической нервной болью эффективную опцию с меньшим риском по сравнению с длительной опиоидной терапией.
Цитирование: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Ключевые слова: нейропатическая боль, транспортёр глицина, неопиоидный анальгетик, аллостерическое ингибирование, структура методом крио-ЭМ