Clear Sky Science · de
Ein reversibler allosterischer Inhibitor von GlyT2 gegen neuropathische Schmerzen ohne on‑target Nebenwirkungen
Neue Hoffnung bei hartnäckigen Nervenschmerzen
Neuropathische Schmerzen — anhaltende Schmerzen durch Nervenschädigung — sprechen oft nicht auf Standardtherapien an und treiben Patientinnen und Patienten in langfristigen Opioidgebrauch. Diese Studie stellt einen neuen Wirkstoffkandidaten in Form einer kleinen Molekülverbindung vor, der die Nervenverkehrführung im Rückenmark dämpft, ohne die typische Last aus Abhängigkeit oder schweren Nebenwirkungen. Indem die Forschenden sowohl die Wirkungsweise auf atomarer Ebene als auch das Verhalten im Tiermodell zeigen, zeichnen sie einen Weg zu sichererem, nicht‑opioidem Schutz vor chronischen Nervenschmerzen.
Warum vorhandene Schmerzmittel versagen
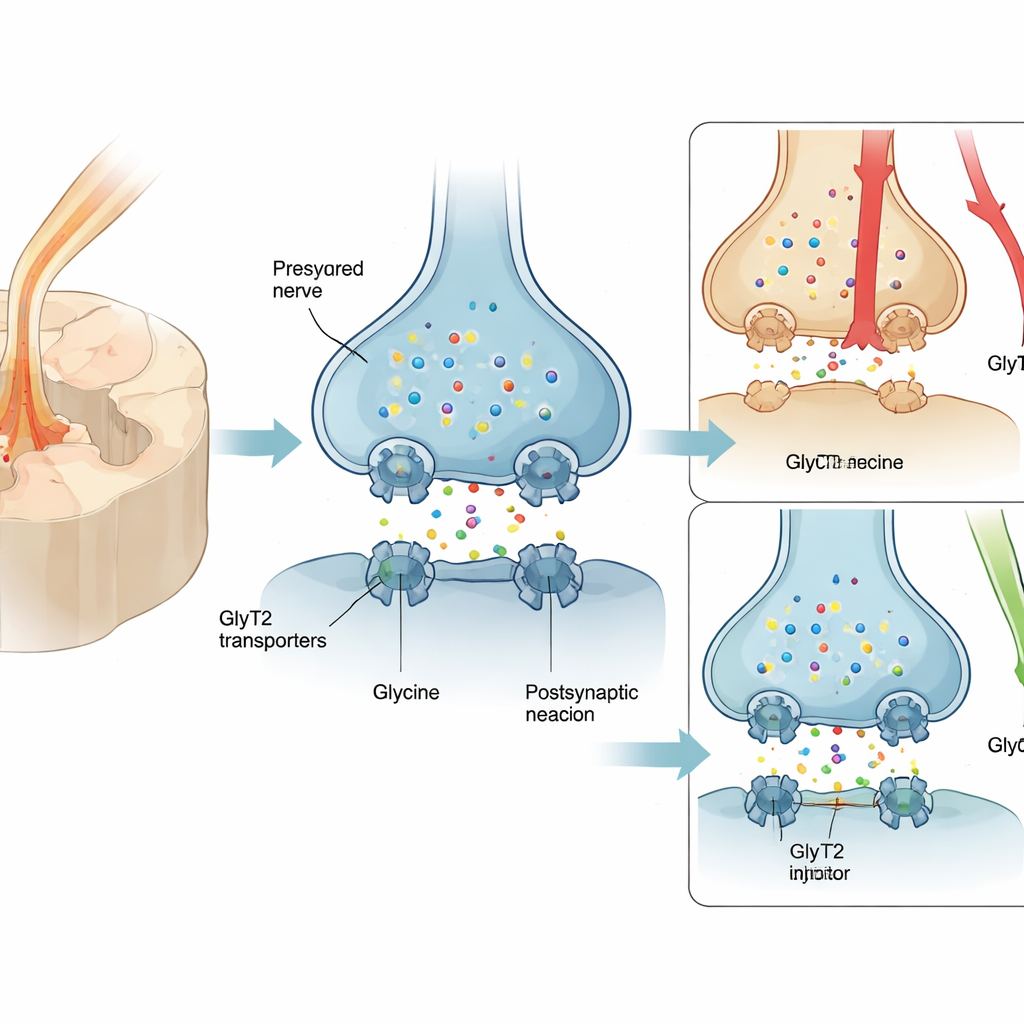
Viele Menschen mit Nervenschmerzen erhalten Pregabalin oder verwandte Medikamente, doch nur etwa einer von vier Patientinnen und Patienten erzielt eine bedeutsame Linderung, und Nebenwirkungen wie Schwindel und Benommenheit sind häufig. Daher werden Opioide trotz des Abhängigkeitsrisikos oft eingesetzt. Ein vielversprechendes alternatives Ziel ist das Protein GlyT2, das an Nervenendigungen im Rückenmark sitzt und Glycin recycelt, einen dämpfenden Neurotransmitter, der Schmerzsignale abschwächt. Eine Erhöhung der Glycinspiegel an diesen Synapsen kann die natürlichen „Bremsen“ des Rückenmarks gegen Schmerz stärken. Frühere GlyT2‑Blocker hingegen hafteten zu stark am Transporter und verursachten schwere on‑target Probleme — Tremor, Anfälle und sogar Tod bei Tieren — und verhinderten so ihren Weg in die Klinik.
Ein sanfterer Weg, ein wichtiges Tor zu beeinflussen
Das Team entwickelte RPI‑GLYT2‑82, eine neue Verbindung, aufgebaut auf dem Gerüst eines starken älteren Inhibitors, ORG25543, aber bewusst so abgestimmt, dass sie weniger fest bindet und schneller wieder ablösbar ist. In Froscheizellen, die so verändert wurden, dass sie menschliches GlyT2 produzieren, blockierte RPI‑GLYT2‑82 den Transporter in submikromolaren Konzentrationen, wusch sich jedoch innerhalb von Minuten aus, während ORG25543 deutlich länger gebunden blieb. Entscheidend bevorzugte RPI‑GLYT2‑82 GlyT2 gegenüber dem nahen Verwandten GlyT1, der im Gehirn weit verbreitet ist, wodurch das Risiko einer großflächigen Störung der Glycin‑Signalübertragung reduziert wird. Die Verbindung blockierte den Transport selbst bei hohen Glycinspiegeln, was bestätigt, dass sie an einer separaten Kontrollstelle wirkt und nicht direkt mit Glycin konkurriert.
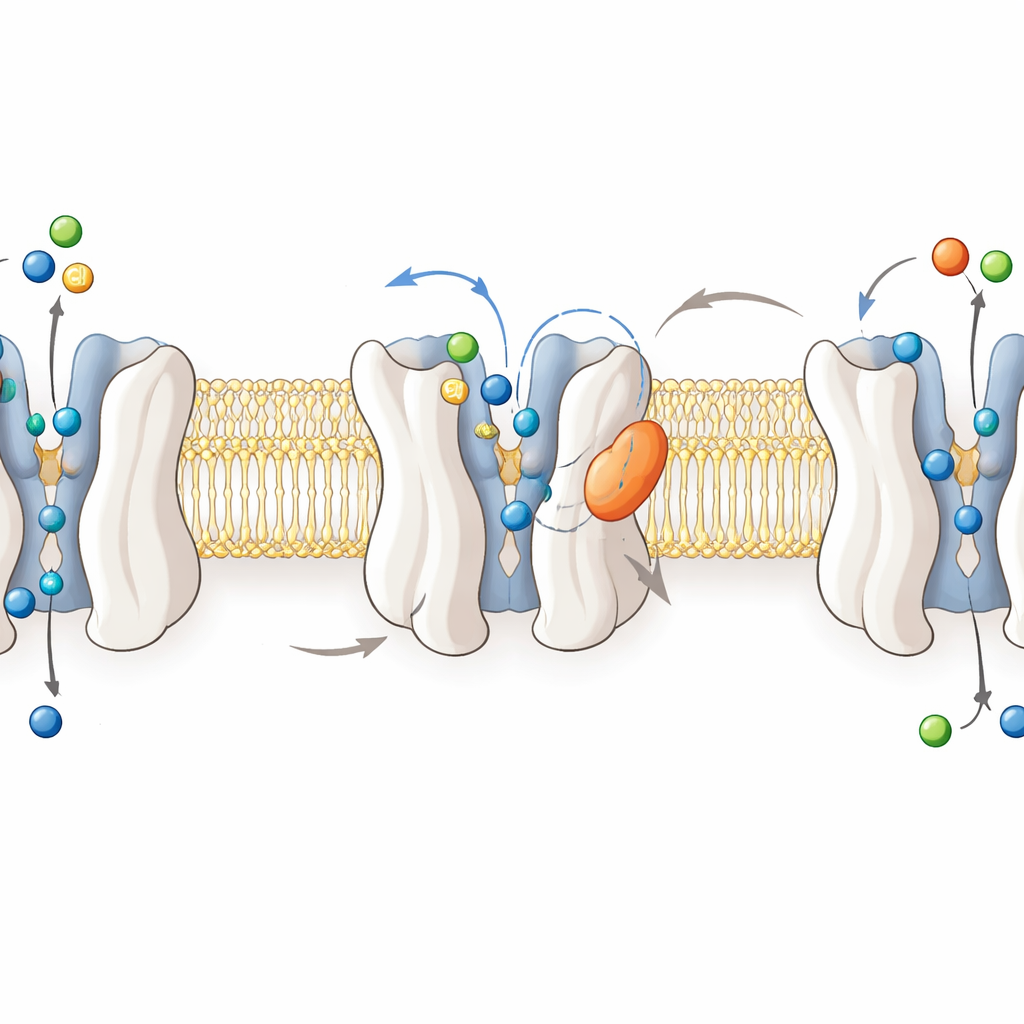
Das Schaltstück für Schmerz auf atomarer Ebene sehen
Um die Wirkungsweise zu verstehen, bestimmten die Forschenden hochauflösende Kryo‑Elektronenmikroskopie‑Strukturen des menschlichen GlyT2 in vier Zuständen: leer, mit Glycin beladen und gebunden an jeweils ORG25543 oder RPI‑GLYT2‑82. Diese Aufnahmen zeigen GlyT2 als Bündel aus zwölf membranüberspannenden Helices, das zwischen nach innen und nach außen geöffneten Formen schwankt, während es Glycin, Natrium und Chlorid durch die Membran transportiert. Glycin sitzt tief in einer zentralen Tasche, wenn der Transporter „okkludiert“ ist und vor beiden Seiten der Membran abgeschirmt liegt. Im Gegensatz dazu lagern sich beide Inhibitoren in einer externen „allosterischen“ Tasche des Proteins ein, zwischen Helices und einer flexiblen Schleife eingekeilt. Dort spreizen sie wichtige Gate‑Reste auseinander und klemmen eine wichtige „Torwächter“‑Leucin außerhalb der zentralen Tasche fest, wodurch GlyT2 in einer nach außen offenen, nicht transportierenden Konformation eingefroren wird.
Was das neue Molekül sicherer macht
RPI‑GLYT2‑82 und ORG25543 binden an dieselbe allosterische Stelle und stellen viele der gleichen Kontakte her, doch subtile chemische Änderungen verändern ihre Lage in der Tasche. Computersimulationen zeigten, dass ORG25543 tief in einer engen hydrophoben Nische sitzt, mit einem kompakten Ringsystem, das wie ein Stopfen passt und den gesperrten Zustand stabilisiert. Im Gegensatz dazu trägt RPI‑GLYT2‑82 einen voluminöseren, polareren Ring und eine angespanntere Ausrichtung einer seiner aromatischen Gruppen. Diese Eigenschaften schwächen seinen Halt, erhöhen seine Beweglichkeit in der Tasche und machen es wahrscheinlicher, dass es wieder in die umgebende Lösung entweicht — das erklärt die geringere Potenz, aber die deutlich schnellere Reversibilität. Mutationen in benachbarten Aminosäuren, die diese Wechselwirkungen weiter lockern, beschleunigen die Freisetzung beider Inhibitoren, was unterstreicht, wie die lokale Geometrie die Verweildauer eines Wirkstoffs und damit die Sicherheit einstellt.
Prüfung von Schmerzlinderung und Sicherheit im Tiermodell
In Mausmodellen mit teilweiser Schädigung des Ischiasnervs entwickeln die Tiere mechanische und kalte Allodynie — Schmerz durch leichte Berührung oder mildes Abkühlen. Bei Injektion reduzierte RPI‑GLYT2‑82 beide Formen der Überempfindlichkeit dosisabhängig, mit maximaler Linderung ein bis drei Stunden nach Gabe. Das Ausmaß der Wirkung war in bestimmten Tests mit den Referenzmitteln Gabapentin oder Pregabalin vergleichbar, wenn auch nicht durchgängig überlegen. Wichtig ist, dass schmerzlindernde Dosen weder Gleichgewicht noch Griffkraft oder Atmung beeinträchtigten, und selbst eine fünffach höhere Dosis nur vorübergehende, reversible motorische und respiratorische Effekte hervorrief. In einem Konditionierten Platzpräferenz‑Test — einem Standardverfahren zur Abfrage belohnender Drogenwirkungen — entwickelten Mäuse eine klare Präferenz für Morphin, nicht jedoch für RPI‑GLYT2‑82, was auf ein geringes Risiko konditionierter Suchtpotenz hindeutet.
Was das für künftige Schmerzbehandlungen bedeutet
Zusammengefasst zeigen die Ergebnisse, dass sich ein GlyT2‑Inhibitor so einstellen lässt, dass er die körpereigene inhibitorische Glycin‑Signalgebung verstärkt, neuropathische Schmerzen bei Tieren lindert und die schweren on‑target Nebenwirkungen vermeidet, die frühere Verbindungen behinderten. Indem die Studie detaillierte strukturelle Pläne von GlyT2 in Aktion liefert und den Nutzen eines reversiblen, allosterischen Ansatzes demonstriert, öffnet sie die Tür zu einer neuen Klasse nicht‑opioider Schmerzmittel. Mit weiterer Optimierung von Potenz, Selektivität und Pharmakokinetik könnten Analoga von RPI‑GLYT2‑82 Patientinnen und Patienten mit chronischen Nervenschmerzen schließlich eine wirksame Option bieten, die weniger riskant ist als eine langfristige Opioidtherapie.
Zitation: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Schlüsselwörter: neuropathische Schmerzen, Glycintransporter, nicht‑opioides Analgetikum, allosterische Hemmung, Cryo‑EM‑Struktur