Clear Sky Science · nl
Een reversibele allosterische remmer van GlyT2 voor neuropathische pijn zonder on‑target bijwerkingen
Nieuw perspectief voor hardnekkige zenuwpijn
Neuropathische pijn — aanhoudende pijn veroorzaakt door zenuwschade — is vaak resistent tegen gangbare behandelingen en duwt patiënten in de richting van langdurig opioïdengebruik. Deze studie introduceert een nieuw kandidaat‑kleinmolecuul dat de zenuwsignaaloverdracht in het ruggenmerg dempt zonder het zware lastpakket van verslaving of ernstige bijwerkingen. Door zowel te laten zien hoe het middel op atomair niveau werkt als hoe het zich in dieren gedraagt, schetsen de onderzoekers een route naar veiliger, niet‑opioïde verlichting van chronische zenuwpijn.
Waarom huidige pijnmiddelen tekortschieten
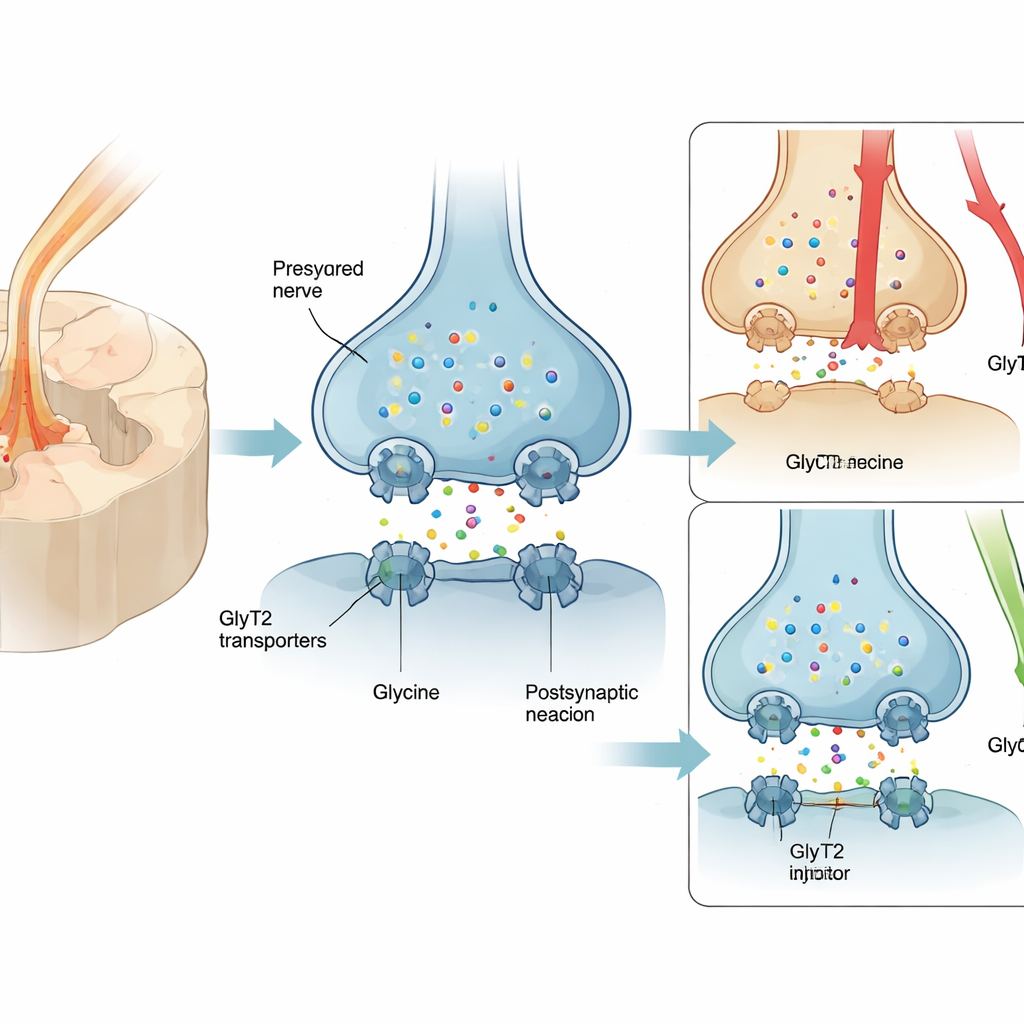
Veel mensen met zenuwpijn krijgen pregabaline of verwante middelen voorgeschreven, maar slechts ongeveer één op de vier patiënten ervaart zinvolle verlichting, en bijwerkingen zoals duizeligheid en slaperigheid zijn veelvoorkomend. Daarom worden opioïden vaak gebruikt ondanks het risico op afhankelijkheid. Een veelbelovend alternatief doelwit is een eiwit genaamd GlyT2, dat op zenuwuiteinden in het ruggenmerg zit en glycine recyclet — een kalmerende boodschapperstof die pijnsignalen dempt. Het versterken van glycine rond deze synapsen kan de natuurlijke ‘remmen’ op pijn in het ruggenmerg versterken. Eerdere GlyT2‑remmers kleefden echter te sterk aan de transporter en veroorzaakten ernstige on‑target problemen — tremoren, aanvallen en zelfs sterfte in dieren — waardoor hun doorgang naar de kliniek werd geblokkeerd.
Een genuanceerdere manier om een belangrijke pijnpoort te verstellen
Het team ontwierp RPI‑GLYT2‑82, een nieuwe verbinding gebouwd op het skelet van een krachtige oudere remmer, ORG25543, maar doelbewust afgestemd om minder strak te binden en sneller los te laten. In kikkereicellen die genetisch waren aangepast om menselijke GlyT2 te produceren, blokkeerde RPI‑GLYT2‑82 de transporter bij sub‑micromolaire concentraties, maar spoelde binnen enkele minuten uit, terwijl ORG25543 veel langer vast bleef zitten. Cruciaal is dat RPI‑GLYT2‑82 GlyT2 prefereerde boven zijn naaste verwant GlyT1, dat wijdverspreid in de hersenen voorkomt, waardoor het risico op brede verstoring van glycine‑signaleringsroutes afneemt. De verbinding remde het transport zelfs bij hoge glycineconcentraties, wat bevestigt dat hij op een aparte regelplek werkt in plaats van rechtstreeks met glycine te concurreren.
De pijnschakelaar in atomair detail zien
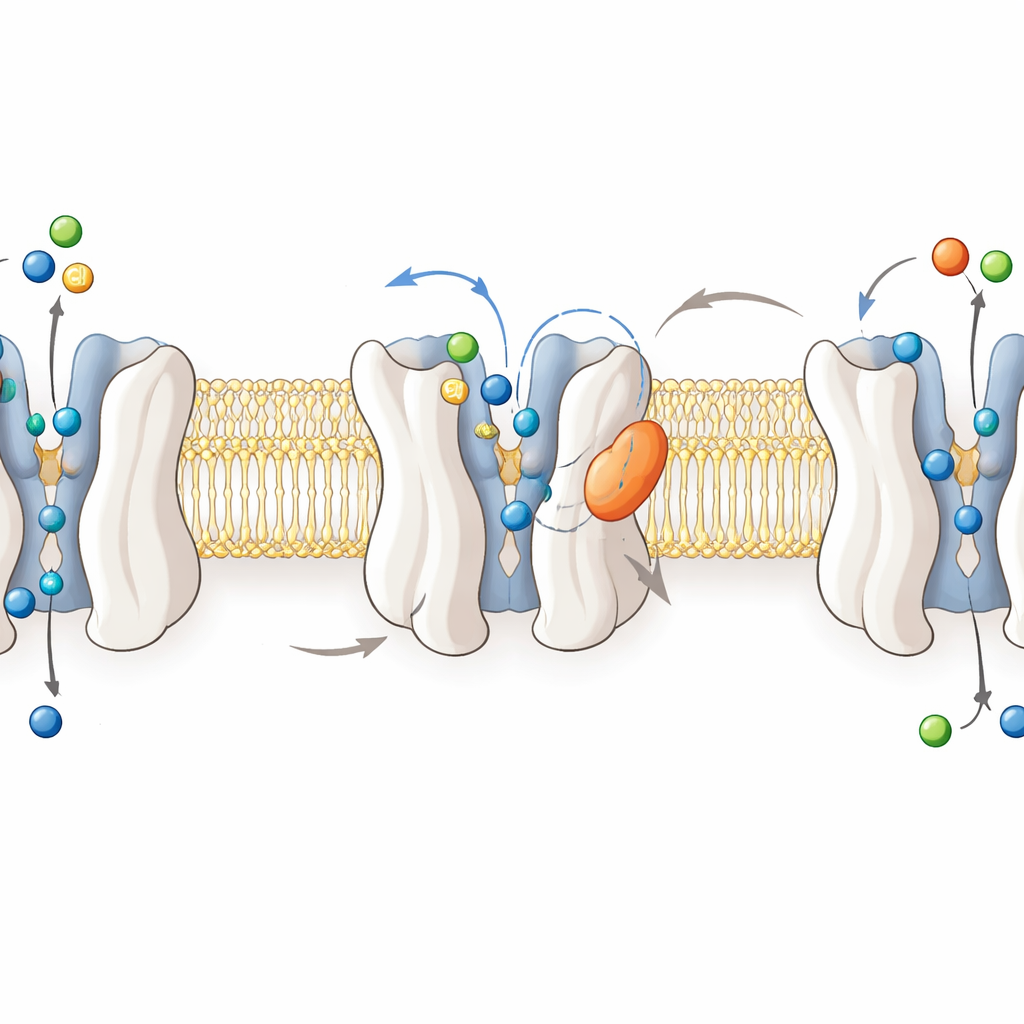
Om te begrijpen hoe het middel werkt, bepaalden de onderzoekers cryo‑elektronenmicroscopie‑structuren van menselijke GlyT2 met hoge resolutie in vier toestanden: leeg, glycine‑geladen en gebonden aan respectievelijk ORG25543 of RPI‑GLYT2‑82. Deze beelden tonen GlyT2 als een bundel van twaalf membraan‑spannende helices die schommelen tussen naar binnen‑ en naar buiten gekeerde vormen terwijl ze glycine, natrium en chloride over het celmembraan verplaatsen. Glycine ligt diep in een centraal pocket wanneer de transporter ‘geoccludeerd’ is, afgeschermd van beide zijden van het membraan. In tegenstelling daarmee nestelen beide remmers zich in een allosterische pocket aan de buitenkant van het eiwit, geklemd tussen helices en een flexibel lusje. Daar wrikken ze sleutelresiduen van het poortmechanisme uit elkaar en keren een belangrijke ‘poortwachter’‑leucine naar buiten toe, waardoor GlyT2 bevroren raakt in een naar buiten‑open, niet‑transporterende conformatie.
Wat het nieuwe molecuul veiliger maakt
RPI‑GLYT2‑82 en ORG25543 binden aan dezelfde allosterische plaats en maken veel van dezelfde contacten, maar subtiele chemische aanpassingen veranderen hoe ze in de pocket liggen. Computersimulaties toonden aan dat ORG25543 diep wegzakt in een strakke hydrofobe nis, met een compact ringenstelsel dat als een stop past en de vergrendelde toestand stabiliseert. Daarentegen draagt RPI‑GLYT2‑82 een volumineuzere, meer polaire ring en een meer gespannen oriëntatie van een van zijn aromatische groepen. Deze kenmerken verzwakken zijn greep, vergroten zijn bewegelijkheid in de pocket en maken het waarschijnlijker dat het terugvloeit naar de omringende oplossing — wat zijn lagere potentie maar veel snellere reversibiliteit verklaart. Mutaties in nabijgelegen aminozuren die deze interacties verder versoepelen, versnellen de vrijlating van beide remmers nog meer, wat benadrukt hoe de lokale geometrie de verblijftijd van het medicijn en daarmee de veiligheid afstemt.
Testen van pijnverlichting en veiligheid in dieren
In muismodellen waarin de nervus ischiadicus gedeeltelijk beschadigd is, ontwikkelen dieren mechanische en koude allodynie — pijn door lichte aanraking of milde verkoeling. Toegediend via injectie verminderde RPI‑GLYT2‑82 beide vormen van overgevoeligheid op een dosisafhankelijke manier, met piekverlichting een tot drie uur na toediening. De mate van voordeel was vergelijkbaar met die van referentiegeneesmiddelen gabapentine of pregabaline in bepaalde tests, al niet superieur over de hele linie. Belangrijk is dat doses die pijn verlichtten, balans, grijpkracht of ademhaling niet aantasten, en zelfs een vijfmaal hogere dosis slechts voorbijgaande, reversibele motorische en respiratoire effecten veroorzaakte. In een conditioned place‑preference‑test — een standaardmethode om drugsbeloning te onderzoeken — ontwikkelden muizen een duidelijke voorkeur voor morfine, maar niet voor RPI‑GLYT2‑82, wat wijst op een laag risico op verslavingsachtige versterkende effecten.
Wat dit betekent voor toekomstige pijnbehandelingen
Alles bij elkaar laat het werk zien dat het mogelijk is een GlyT2‑remmer te ontwikkelen die het lichaamseigen remmende glycine‑signaal versterkt, neuropathische pijn bij dieren verlicht en de ernstige on‑target bijwerkingen vermijdt die eerdere verbindingen parten speelden. Door gedetailleerde structurele blauwdrukken van GlyT2 in werking te bieden en de voordelen van een reversibele, allosterische benadering te demonstreren, opent de studie de deur naar een nieuwe klasse niet‑opioïde pijnstillers. Met verdere optimalisatie van potentie, selectiviteit en farmacokinetiek zouden analogen van RPI‑GLYT2‑82 uiteindelijk patiënten met chronische zenuwpijn een effectieve optie kunnen bieden die minder risicovol is dan langdurige opioïde therapie.
Bronvermelding: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Trefwoorden: neuropathische pijn, glycine‑transporter, niet‑opioïde analgeticum, allosterische remming, cryo‑EM‑structuur