Clear Sky Science · es
Un inhibidor alostérico reversible de GlyT2 para el dolor neuropático sin efectos secundarios dependientes del objetivo
Nueva esperanza para el dolor nervioso resistente
El dolor neuropático—dolor persistente causado por daño nervioso—suele resistir los tratamientos habituales y empuja a los pacientes hacia el uso prolongado de opioides. Este estudio presenta un nuevo candidato farmacológico de pequeña molécula que reduce el tráfico de señales nerviosas en la médula espinal sin la carga grave de la adicción o efectos secundarios severos. Al revelar tanto cómo actúa el fármaco a nivel atómico como cómo se comporta en animales, los investigadores trazan una vía hacia un alivio crónico del dolor nervioso más seguro y sin opioides.
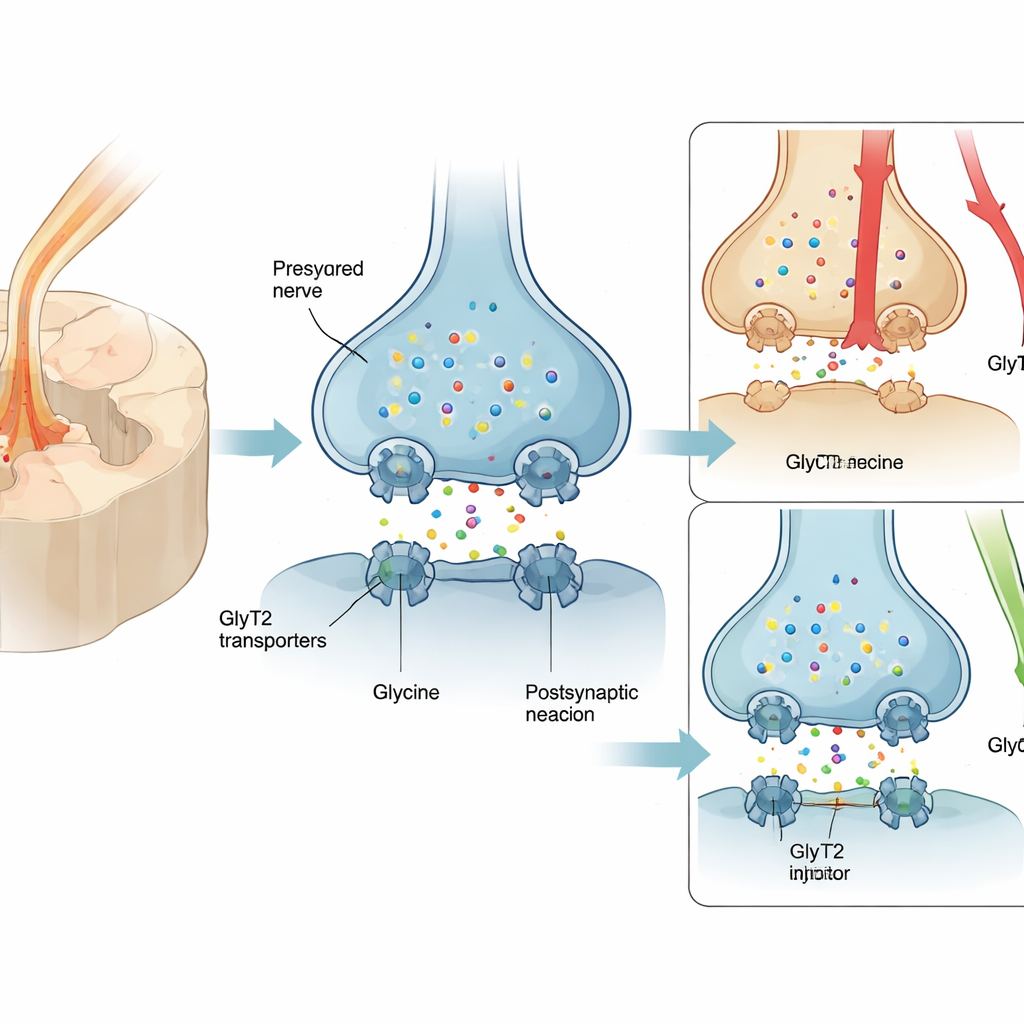
Por qué los fármacos actuales se quedan cortos
A muchas personas con dolor nervioso se les prescribe pregabalina u otros medicamentos relacionados, pero solo alrededor de uno de cada cuatro pacientes experimenta un alivio significativo, y los efectos secundarios como mareo y somnolencia son comunes. Como resultado, con frecuencia se usan opioides a pesar del riesgo de dependencia. Un blanco alternativo prometedor es una proteína llamada GlyT2, que se localiza en las terminaciones nerviosas de la médula espinal y recicla la glicina, un mensajero químico calmante que atenúa las señales de dolor. Incrementar la glicina en estas sinapsis puede fortalecer los “frenos” naturales de la médula espinal sobre el dolor. Sin embargo, inhibidores previos de GlyT2 se unían demasiado fuertemente al transportador y provocaban problemas graves dependientes del objetivo—temblores, convulsiones e incluso la muerte en animales—lo que impidió su avance clínico.
Una manera más suave de accionar un punto clave del dolor
El equipo diseñó RPI-GLYT2-82, un compuesto nuevo construido sobre el andamiaje de un inhibidor potente anterior, ORG25543, pero intencionadamente ajustado para unirse con menor firmeza y desprenderse más rápido. En óvulos de rana modificados para expresar GlyT2 humano, RPI-GLYT2-82 bloqueó el transportador a concentraciones submicromolares y, sin embargo, se lavó en cuestión de minutos, mientras que ORG25543 permaneció atrapado durante mucho más tiempo. De manera crucial, RPI-GLYT2-82 mostró preferencia por GlyT2 frente a su par cercano GlyT1, ampliamente distribuido en el cerebro, reduciendo el riesgo de una alteración generalizada de la señalización de glicina. El compuesto bloqueó el transporte incluso cuando los niveles de glicina eran altos, confirmando que actúa en un sitio de control separado en lugar de competir directamente con la glicina.
Ver el interruptor del dolor con detalle atómico
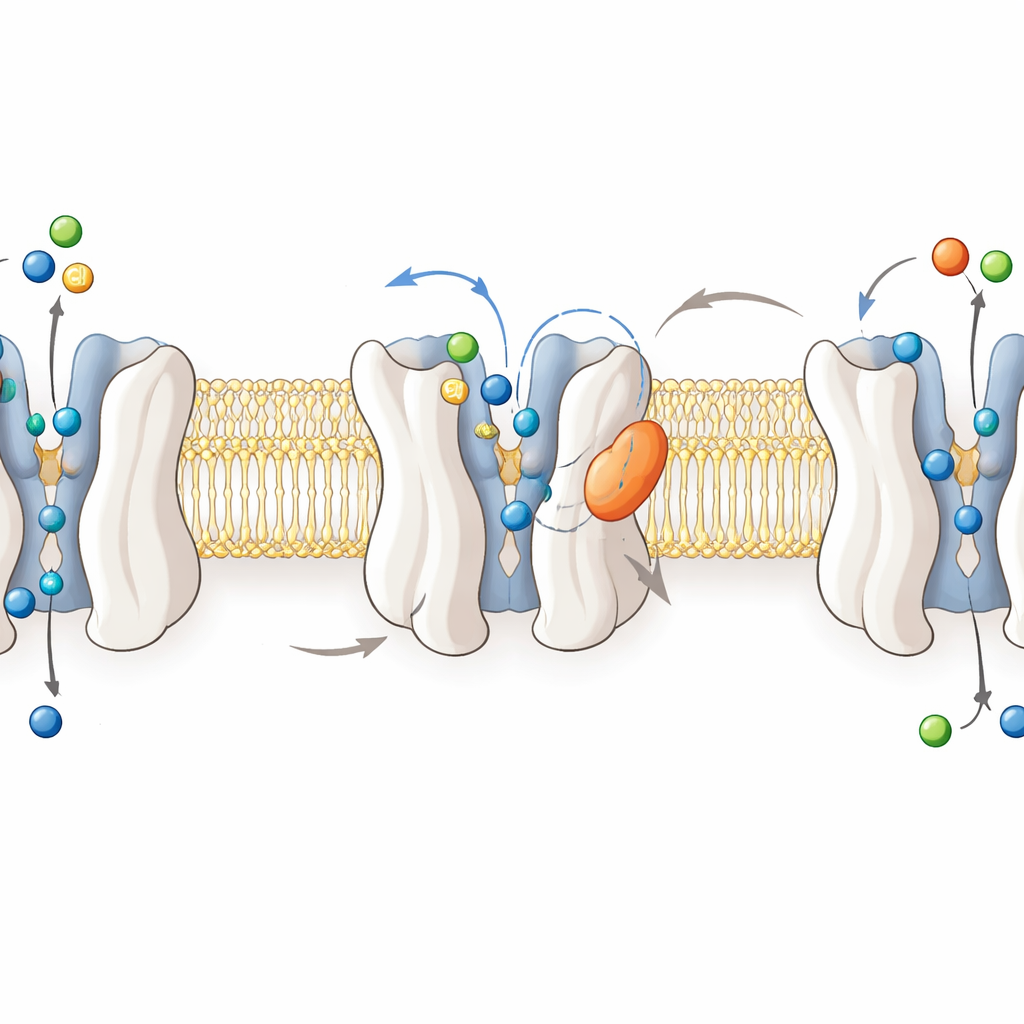
Para comprender cómo funciona el fármaco, los investigadores resolvieron estructuras de alta resolución por criomicroscopía electrónica de GlyT2 humano en cuatro estados: vacía, con glicina, y ligada a ORG25543 o a RPI-GLYT2-82. Estas imágenes muestran a GlyT2 como un conjunto de doce hélices que atraviesan la membrana y que oscilan entre configuraciones orientadas hacia el interior y hacia el exterior al desplazar glicina, sodio y cloruro a través de la membrana celular. La glicina se ubica profundamente en un bolsillo central cuando el transportador está “ocluido”, protegida de ambos lados de la membrana. En contraste, ambos inhibidores se alojan en un bolsillo “alostérico” en el exterior de la proteína, encajados entre hélices y un bucle flexible. Allí separan residuos clave de la compuerta y fijan una leucina «guardián» importante fuera del bolsillo central, congelando a GlyT2 en una conformación abierta hacia el exterior que impide el transporte.
Qué hace al nuevo compuesto más seguro
RPI-GLYT2-82 y ORG25543 se unen al mismo sitio alostérico y establecen muchos de los mismos contactos, pero sutiles ajustes químicos cambian su posición en el bolsillo. Simulaciones por ordenador revelaron que ORG25543 se anida profundamente en un nicho hidrofóbico ceñido, con un sistema de anillos compacto que encaja como un tapón y estabiliza el estado bloqueado. En contraste, RPI-GLYT2-82 porta un anillo más voluminoso y polar y una orientación más forzada de uno de sus grupos aromáticos. Estas características debilitan su agarre, aumentan su movimiento dentro del bolsillo y hacen que sea más probable que vuelva a la solución circundante, lo que explica su menor potencia pero mucha mayor reversibilidad. Mutaciones en aminoácidos cercanos que aflojan estas interacciones aceleran aún más la liberación de ambos inhibidores, subrayando cómo la geometría local ajusta el tiempo de residencia del fármaco y, en consecuencia, la seguridad.
Evaluación del alivio del dolor y la seguridad en animales
En modelos murinos con lesión parcial del nervio ciático, los animales desarrollan alodinia mecánica y alodinia al frío—dolor por un tacto ligero o por un enfriamiento leve. Administrado por inyección, RPI-GLYT2-82 redujo ambos tipos de hipersensibilidad de forma dosis-dependiente, con el máximo alivio entre una y tres horas tras la dosis. El grado de beneficio fue similar al de fármacos de referencia como gabapentina o pregabalina en ciertas pruebas, aunque no superior en todos los ensayos. Importante, las dosis que aliviaron el dolor no alteraron el equilibrio, la fuerza de agarre ni la respiración, y aun una dosis cinco veces mayor provocó solo efectos motores y respiratorios transitorios y reversibles. En una prueba de preferencia por lugar condicionado—un método estándar para explorar la recompensa por fármacos—los ratones desarrollaron una clara preferencia por la morfina, pero no por RPI-GLYT2-82, lo que sugiere bajo riesgo de efectos reforzantes similares a la adicción.
Qué significa esto para futuros tratamientos del dolor
En conjunto, el trabajo demuestra que es posible ajustar un inhibidor de GlyT2 que potencia la señalización inhibitoria natural de la glicina, alivia el dolor neuropático en animales y evita los graves efectos secundarios dependientes del objetivo que lastraban a compuestos anteriores. Al proporcionar planos estructurales detallados de GlyT2 en acción y demostrar los beneficios de un enfoque alostérico y reversible, el estudio abre la puerta a una nueva clase de analgésicos no opioides. Con optimizaciones adicionales en potencia, selectividad y farmacocinética, análogos de RPI-GLYT2-82 podrían eventualmente ofrecer a pacientes con dolor neuropático crónico una opción eficaz y con menos riesgo que la terapia opioide a largo plazo.
Cita: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Palabras clave: dolor neuropático, transportador de glicina, analgésico no opioide, inhibición alostérica, estructura por cryo-EM