Clear Sky Science · pl
Odwracalny inhibitor allosteryczny GlyT2 na ból neuropatyczny bez działań niepożądanych związanych z celem
Nowa nadzieja na uporczywy ból nerwowy
Ból neuropatyczny — utrzymujący się ból spowodowany uszkodzeniem nerwów — często opiera się standardowym terapiom i kieruje pacjentów w stronę długotrwałego stosowania opioidów. W tym badaniu przedstawiono nowego kandydata na lek małocząsteczkowy, który tłumi przepływ sygnałów nerwowych w rdzeniu kręgowym bez ciężkich konsekwencji w postaci uzależnienia czy poważnych działań niepożądanych. Poprzez pokazanie zarówno działania leku na poziomie atomowym, jak i jego zachowania u zwierząt, badacze wytyczają drogę do bezpieczniejszego, nienarkotycznego złagodzenia przewlekłego bólu neuropatycznego.
Dlaczego obecne leki przeciwbólowe zawodzą
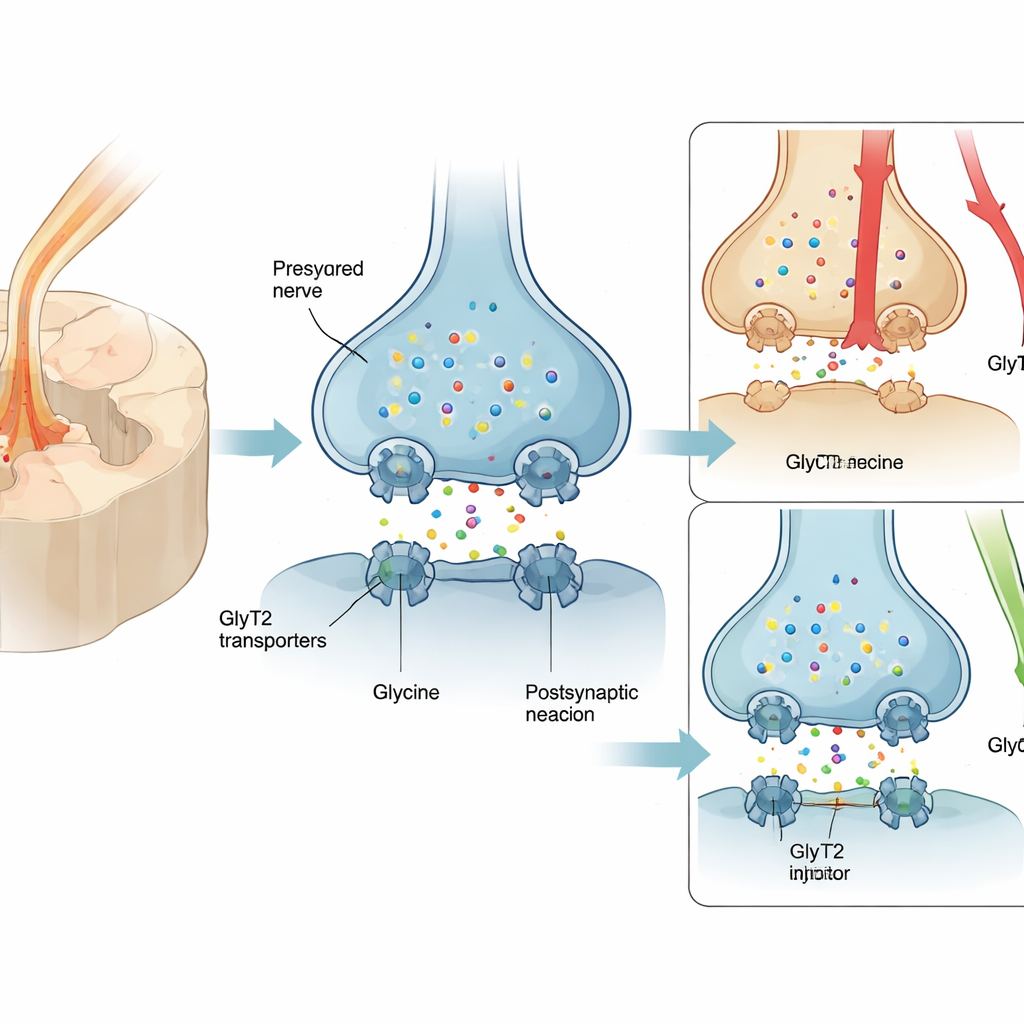
Wielu pacjentom z bólem neuropatycznym przepisuje się pregabalinę lub pokrewne leki, jednak tylko około jedna czwarta chorych doświadcza znaczącej ulgi, a skutki uboczne takie jak zawroty głowy i senność są powszechne. W efekcie opioidy są często stosowane pomimo ryzyka uzależnienia. Obiecującym alternatywnym celem jest białko zwane GlyT2, obecne na zakończeniach nerwowych w rdzeniu kręgowym, które odzyskuje glicynę — hamujący neurotransmiter zmniejszający sygnały bólowe. Zwiększenie stężenia glicyny przy tych synapsach może wzmocnić naturalne „hamulce” rdzenia kręgowego na ból. Wcześniejsze inhibitory GlyT2 jednak wiązały się zbyt mocno z transporterem i powodowały poważne działania niepożądane związane z celem — drżenia, drgawki, a nawet śmierć u zwierząt — co zablokowało ich rozwój kliniczny.
Delikatniejszy sposób na pstryczek w ważną bramkę bólu
Zespół opracował RPI-GLYT2-82, nowy związek zbudowany na szkielecie silniejszego, starszego inhibitora ORG25543, ale celowo dostrojony tak, by wiązać się słabiej i szybciej odłączać. W komórkach jaj żaby zmodyfikowanych do produkcji ludzkiego GlyT2, RPI-GLYT2-82 blokował transporter w stężeniach podmikromolowych, lecz wypłukiwał się w ciągu minut, podczas gdy ORG25543 pozostawał związany znacznie dłużej. Co istotne, RPI-GLYT2-82 preferował GlyT2 nad bliskim krewnym GlyT1, który jest szeroko rozpowszechniony w mózgu, zmniejszając ryzyko szeroko zakrojonego zaburzenia sygnalizacji glicynowej. Związek blokował transport nawet przy wysokich poziomach glicyny, potwierdzając, że działa w oddzielnym miejscu kontrolnym, a nie konkuruje bezpośrednio z glicyną.
Obserwacja przełącznika bólu w szczegółach atomowych
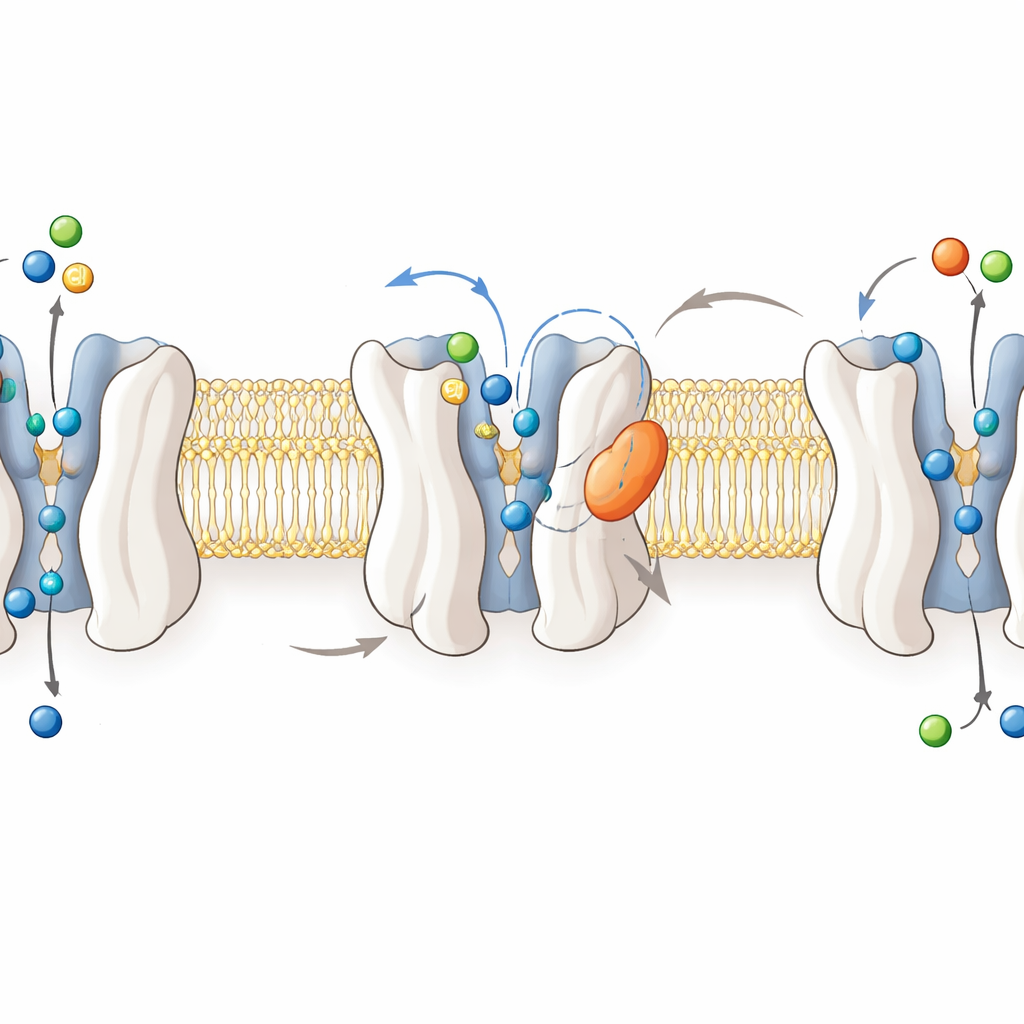
Aby zrozumieć sposób działania leku, badacze rozwiązywali struktury ludzkiego GlyT2 za pomocą wysokorozdzielczej krio‑elektronowej mikroskopii w czterech stanach: pustym, związanego z glicyną oraz związanych z ORG25543 lub RPI-GLYT2-82. Obrazy pokazują GlyT2 jako wiązkę dwunastu helis przechodzących przez błonę, które kołyszą się między konfiguracjami zwróconymi do wnętrza i zewnątrz w trakcie przemieszczania glicyny, sodu i chlorków przez błonę komórkową. Glicyna znajduje się głęboko w centralnej kieszeni, gdy transporter jest „zablokowany”, osłonięta z obu stron błony. Natomiast oba inhibitory zagnieżdżają się w kieszeni „allosterycznej” po zewnętrznej stronie białka, klinując się między helisami a elastyczną pętlą. Tam rozdzielają kluczowe reszty tworzące bramkę i ustalają ważną „strażnikową” leucynę na zewnątrz centralnej kieszeni, zamrażając GlyT2 w pozycji otwartej na zewnątrz, nieprowadzącej transportu.
Co czyni nową cząsteczkę bezpieczniejszą
RPI-GLYT2-82 i ORG25543 wiążą to samo miejsce allosteryczne i tworzą wiele tych samych kontaktów, ale subtelne chemiczne zmiany wpływają na ich ułożenie w kieszeni. Symulacje komputerowe wykazały, że ORG25543 wpasowuje się głęboko w ciasną hydrofobową niszę, z zwartym systemem pierścieniowym pasującym jak korek i stabilizującym zablokowany stan. Natomiast RPI-GLYT2-82 ma bardziej objętościowy, polarny pierścień i bardziej napiętą orientację jednej z grup aromatycznych. Te cechy osłabiają jego uchwyt, zwiększają ruchomość w kieszeni i sprawiają, że częściej ucieka z powrotem do otaczającego roztworu — co tłumaczy niższą podatność na działanie, ale znacznie szybszą odwracalność. Mutacje w pobliskich aminokwasach, które dodatkowo poluzowują te interakcje, przyspieszają uwolnienie obu inhibitorów, podkreślając, jak lokalna geometria dostraja czas przebywania leku i w konsekwencji jego bezpieczeństwo.
Testy łagodzenia bólu i bezpieczeństwa u zwierząt
W modelach mysich, w których nerw kulszowy jest częściowo uszkodzony, zwierzęta rozwijają allodynię mechaniczną i termiczną — ból wywołany lekkim dotykiem lub łagodnym ochłodzeniem. Po podaniu w formie wstrzyknięcia, RPI-GLYT2-82 zmniejszał oba rodzaje nadwrażliwości w sposób zależny od dawki, z maksymalną ulgą pojawiającą się w ciągu jednej do trzech godzin po podaniu. Stopień korzyści był podobny do działania leków referencyjnych, gabapentyny lub pregabaliny, w niektórych testach, choć nie przewyższał ich we wszystkich. Co ważne, dawki łagodzące ból nie upośledzały równowagi, siły chwytu ani oddychania, a nawet pięciokrotnie wyższa dawka powodowała jedynie przejściowe, odwracalne efekty motoryczne i oddechowe. W teście preferencji miejsca warunkowanego — standardowej metodzie badania nagradzającego działania leku — myszy wykształciły wyraźną preferencję dla morfiny, ale nie dla RPI-GLYT2-82, co sugeruje niskie ryzyko efektów wzmacniających podobnych do uzależnienia.
Co to oznacza dla przyszłych terapii bólu
Podsumowując, praca pokazuje, że możliwe jest dostrojenie inhibitora GlyT2, który wzmacnia własną hamującą sygnalizację glicynową organizmu, łagodzi ból neuropatyczny u zwierząt i unika poważnych działań niepożądanych związanych z celem, które uniemożliwiały wcześniejszym związkom rozwój. Dostarczając szczegółowych struktur GlyT2 w działaniu i demonstrując zalety odwracalnego, allosterycznego podejścia, badanie otwiera drzwi do nowej klasy nienarkotycznych leków przeciwbólowych. Przy dalszej optymalizacji mocy, selektywności i farmakokinetyki, analogi RPI-GLYT2-82 mogłyby w przyszłości dać pacjentom z przewlekłym bólem nerwowym skuteczną opcję mniej ryzykowną niż długotrwała terapia opioidowa.
Cytowanie: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Słowa kluczowe: ból neuropatyczny, transportera glicyny, niefarmakologiczny analgetyk, inhibicja allosteryczna, struktura cryo-EM