Clear Sky Science · fr
Un inhibiteur allostérique réversible de GlyT2 pour la douleur neuropathique sans effets indésirables ciblés
Un nouvel espoir pour la douleur nerveuse récalcitrante
La douleur neuropathique — douleur persistante causée par des lésions nerveuses — résiste souvent aux traitements standards et pousse les patients vers un usage prolongé d’opioïdes. Cette étude présente un nouveau candidat médicament de petite taille qui réduit le trafic des signaux nerveux dans la moelle épinière sans le lourd lot d’addiction ou d’effets indésirables graves. En révélant à la fois le mode d’action atomique du composé et son comportement chez l’animal, les chercheurs dessinent une voie vers un soulagement non opioïde et plus sûr pour la douleur nerveuse chronique.
Pourquoi les antalgiques actuels sont insuffisants
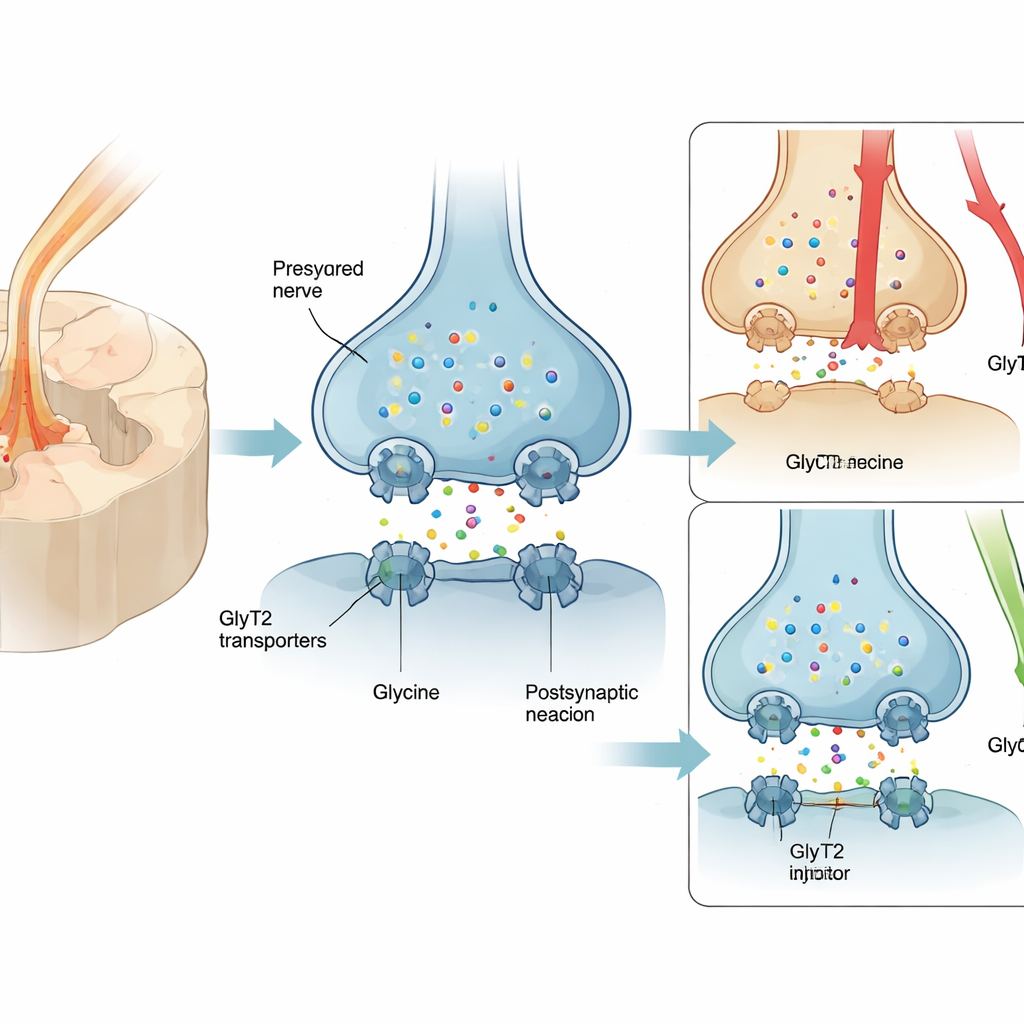
Beaucoup de personnes souffrant de douleur nerveuse se voient prescrire de la prégabaline ou des médicaments apparentés, pourtant seulement environ un patient sur quatre ressent un soulagement significatif, et des effets secondaires tels que vertiges et somnolence sont fréquents. Par conséquent, les opioïdes sont souvent utilisés malgré le risque de dépendance. Une cible alternative prometteuse est une protéine nommée GlyT2, présente sur les terminaisons nerveuses de la moelle épinière et responsable du recyclage de la glycine, un neuromédiateur inhibiteur qui atténue les signaux douloureux. Augmenter la glycine autour de ces synapses peut renforcer les « freins » naturels de la moelle épinière sur la douleur. Toutefois, les premiers bloqueurs de GlyT2 se liaient trop fermement au transporteur et provoquaient des problèmes graves liés à la cible — tremblements, convulsions et même décès chez l’animal — ce qui a empêché leur développement clinique.
Une manière plus douce de moduler une porte clé de la douleur
L’équipe a conçu RPI‑GLYT2‑82, un nouveau composé dérivé de l’ossature d’un inhibiteur ancien et puissant, ORG25543, mais délibérément ajusté pour se lier moins fermement et se dissocier plus rapidement. Dans des ovocytes de xénope exprimant le GlyT2 humain, RPI‑GLYT2‑82 bloquait le transporteur à des concentrations sub‑micromolaires tout en se lavant en quelques minutes, alors que ORG25543 restait attaché beaucoup plus longtemps. Fait crucial, RPI‑GLYT2‑82 préférait GlyT2 à son homologue rapproché GlyT1, abondant dans tout le cerveau, réduisant ainsi le risque d’une perturbation généralisée du signal glycinergique. Le composé inhibait le transport même en présence de niveaux élevés de glycine, confirmant qu’il agit sur un site de contrôle distinct plutôt que par compétition directe avec la glycine elle‑même.
Observer l’interrupteur de la douleur en détail atomique
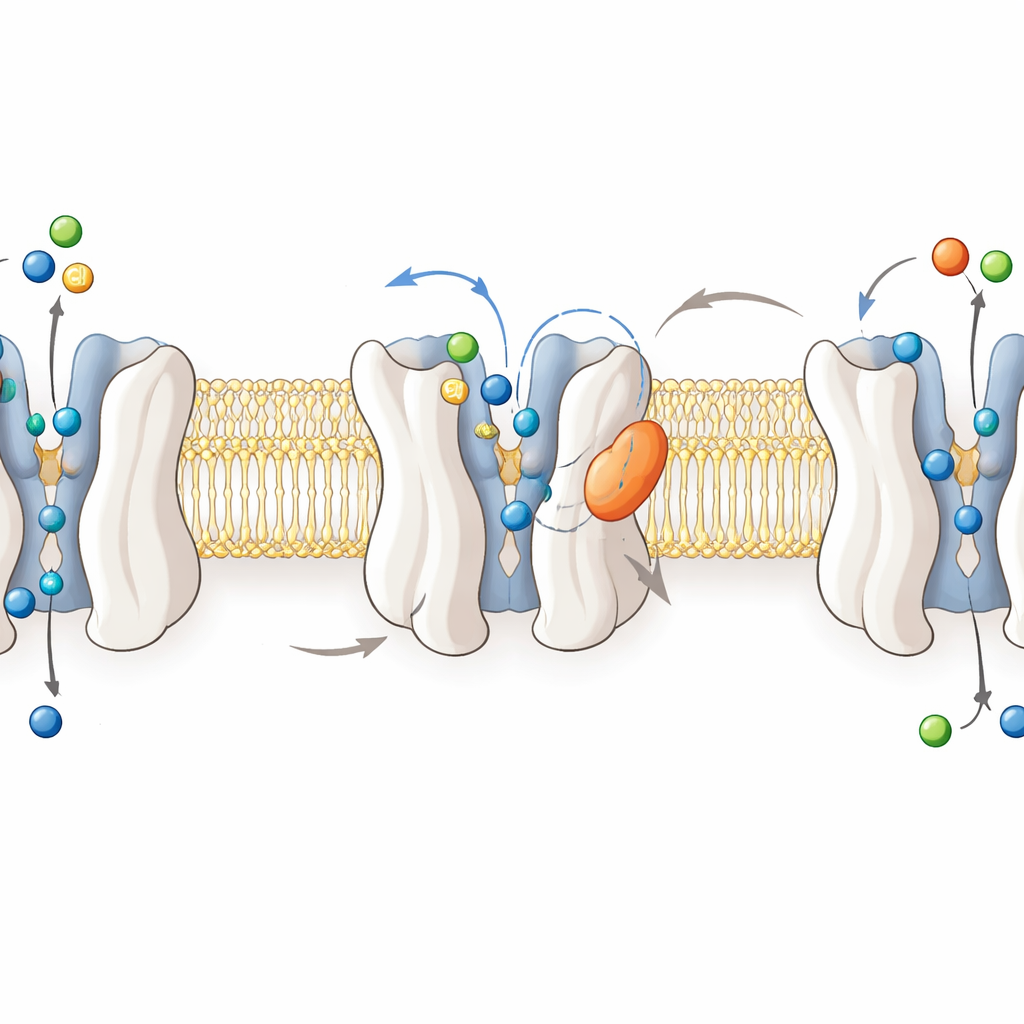
Pour comprendre le mode d’action du médicament, les chercheurs ont résolu des structures à haute résolution par cryo‑microscopie électronique du GlyT2 humain dans quatre états : vide, lié à la glycine, et lié soit à ORG25543 soit à RPI‑GLYT2‑82. Ces images montrent GlyT2 comme un faisceau de douze hélices transmembranaires qui basculent entre des conformations tournée vers l’intérieur et tournée vers l’extérieur pour déplacer la glycine, le sodium et le chlorure à travers la membrane cellulaire. La glycine se loge profondément dans une poche centrale lorsque le transporteur est « occlus », protégée des deux faces de la membrane. En revanche, les deux inhibiteurs s’insinuent dans une poche allostérique à l’extérieur de la protéine, coinçant entre des hélices et une boucle flexible. Là, ils écartent des résidus clés de la porte et maintiennent un leucine « gardien » important à l’extérieur de la poche centrale, figant GlyT2 dans une conformation ouverte vers l’extérieur et incapable de transporter.
Ce qui rend la nouvelle molécule plus sûre
RPI‑GLYT2‑82 et ORG25543 se lient au même site allostérique et établissent de nombreux contacts similaires, mais des ajustements chimiques subtils modifient leur positionnement dans la poche. Des simulations informatiques ont révélé que ORG25543 s’insère profondément dans une niche hydrophobe étroite, avec un système d’anneaux compact qui s’ajuste comme un bouchon et stabilise l’état verrouillé. En revanche, RPI‑GLYT2‑82 possède un anneau plus volumineux et plus polaire et une orientation plus contrainte d’un de ses groupements aromatiques. Ces caractéristiques affaiblissent sa prise, augmentent sa mobilité dans la poche et le rendent plus susceptible de retourner dans la solution environnante — expliquant sa moindre puissance mais une réversibilité beaucoup plus rapide. Des mutations d’acides aminés voisins qui relâchent ces interactions accélèrent encore la libération des deux inhibiteurs, soulignant comment la géométrie locale module le temps de résidence du médicament et, par conséquent, sa sécurité.
Évaluer le soulagement de la douleur et la sécurité chez l’animal
Dans des modèles murins où le nerf sciatique est partiellement lésé, les animaux développent une allodynie mécanique et thermique — douleur au toucher léger ou au refroidissement modéré. Lors d’injections, RPI‑GLYT2‑82 réduisait ces deux types d’hypersensibilité de façon dose‑dépendante, le pic d’effet apparaissant une à trois heures après l’administration. L’amplitude du bénéfice était comparable à celle des médicaments de référence gabapentine ou prégabaline pour certains tests, bien que pas supérieure de manière universelle. Surtout, des doses soulageant la douleur n’altéraient ni l’équilibre, ni la force de préhension, ni la respiration, et même une dose cinq fois plus élevée ne provoquait que des effets moteurs et respiratoires transitoires et réversibles. Dans un test de préférence de lieu conditionnée — méthode standard pour évaluer le potentiel de renforcement d’un médicament — les souris développaient une préférence marquée pour la morphine, mais pas pour RPI‑GLYT2‑82, suggérant un faible risque d’effets addictifs de type renforcement.
Ce que cela signifie pour les traitements futurs de la douleur
Pris ensemble, les résultats montrent qu’il est possible d’optimiser un inhibiteur de GlyT2 qui renforce la signalisation inhibitrice naturelle à la glycine, soulage la douleur neuropathique chez l’animal et évite les graves effets indésirables ciblés qui ont compromis les composés antérieurs. En fournissant des plans structuraux détaillés du GlyT2 en action et en démontrant les avantages d’une approche allostérique réversible, l’étude ouvre la voie à une nouvelle classe d’antidouleurs non opioïdes. Avec une optimisation supplémentaire de la puissance, de la sélectivité et des propriétés pharmacocinétiques, des analogues de RPI‑GLYT2‑82 pourraient éventuellement offrir aux patients souffrant de douleurs nerveuses chroniques une option efficace et moins risquée que la thérapie opioïde à long terme.
Citation: Cantwell Chater, R.P., Peiser-Oliver, J., Pati, T.K. et al. A reversible allosteric inhibitor of GlyT2 for neuropathic pain without on-target side effects. Nat Commun 17, 2828 (2026). https://doi.org/10.1038/s41467-026-69616-5
Mots-clés: douleur neuropathique, transporteur de glycine, analgésique non opioïde, inhibition allostérique, structure cryo‑EM