Clear Sky Science · sv
Struktur- och mekanistisk insikt i azetidin-associerade αKG-NHFe-enzymet OkaE med multifunktionell katalys
Varför ett litet enzym spelar roll för framtida läkemedel och bekämpningsmedel
Många potenta läkemedel och insektsbekämpningsmedel bygger på komplexa ringformiga molekyler som är svåra för kemister att konstruera. Denna studie avslöjar hur ett enda svampenenzym, kallat OkaE, kan forma en sådan ring — en ovanligt påfrestad fyrledad azetidin — och sedan ytterligare omforma molekylen på flera olika sätt. Att förstå hur OkaE fungerar kan inspirera mer hållbara vägar till nya läkemedel och mycket selektiva insektsmedel som skonar människor och andra ryggradsdjur.
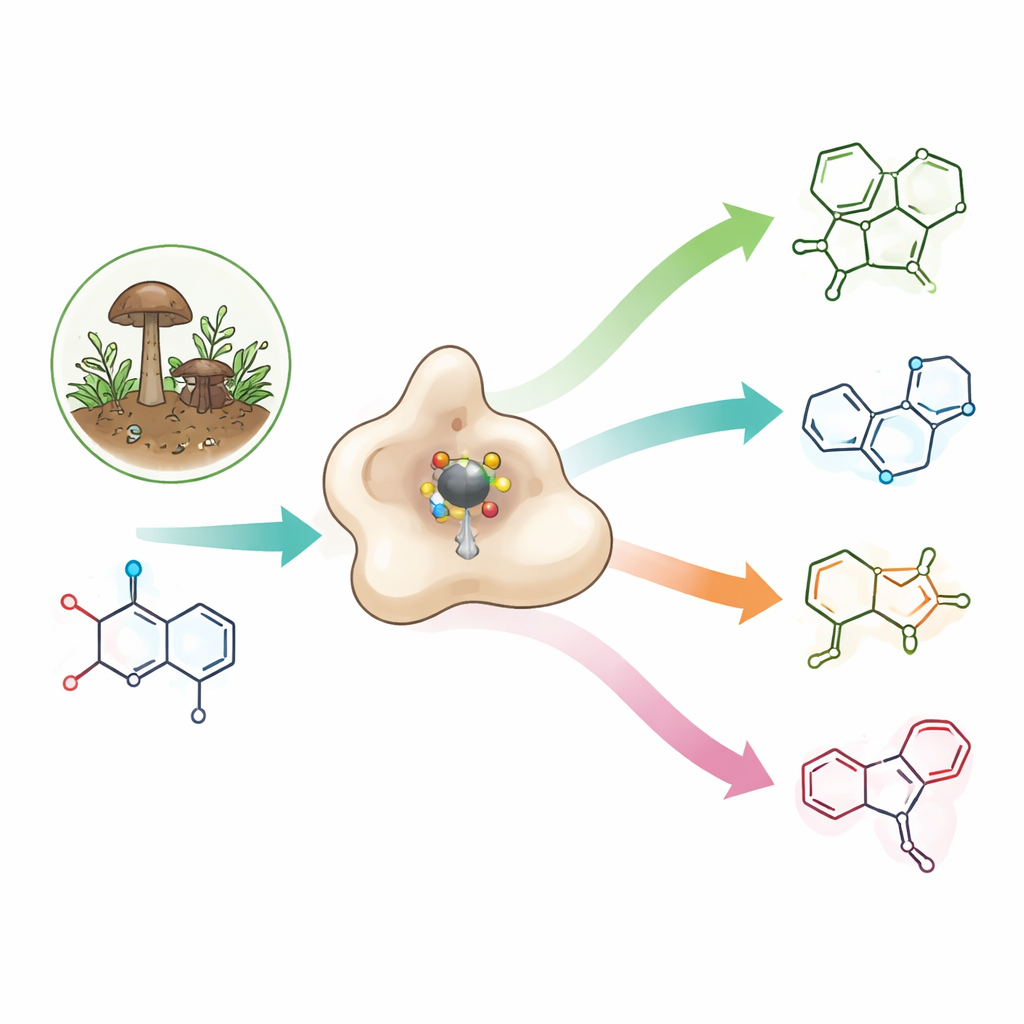
En sällsynt byggsten med stor farmaceutisk potential
Azetidiner är små fyrledade kväveringar som innehåller mycket spänning i en liten volym. Denna spänning ger ofta användbara egenskaper: azetidiner kan förbättra hur läkemedelsmolekyler passar sina mål, rör sig i kroppen och löser sig i vatten. De förekommer redan i experimentella antibiotika, anticancerläkemedel och potentiella Alzheimer‑läkemedel, samt i okaraminer — naturliga insektsgifter som vissa svampar producerar och som selektivt stör jonkanaler i ryggradslösa djur samtidigt som de lämnar mänskliga kanaler intakta. Eftersom azetidinringar är så spända och instabila kräver kemisk syntes av dem ofta flera energikrävande steg och hårda förhållanden.
Naturens ovanliga lösning: enzymet OkaE
Svampar tacklar denna utmaning med specialiserade enzymer. De flesta kända enzymer som bildar azetidiner förenar en kolatom med en kväveatom med hjälp av en vanlig cellulär kofaktor kallad SAM. OkaE bryter mot den regeln. Det tillhör en stor familj järnberoende enzymer som normalt inför syreatomer i molekyler. OkaE använder järn och ett hjälpämne, alfa‑ketoglutarat, för att bilda en mycket reaktiv järn–oxygen‑art som kan avlägsna väteatomer från sitt substrat, okaramine A. Till skillnad från sina släktingar formar OkaE azetidinringen genom att skapa en ny kol–kol‑bindning inne i denna redan komplexa naturprodukt, vilket gör det till ett undantag även inom en mycket mångsidig enzymfamilj.
Ett enzym, många kemiska trick
När forskarna studerade renat OkaE i provrör förväntade de sig bara bildandet av azetidin och en enkel oxidation. Istället fann de en liten kemisk fabrik. Med utgångspunkt i okaramine A producerade OkaE minst fyra nya molekyler, kallade neuokaraminer I–IV, förutom kända mellanprodukter. Dessa produkter visade att OkaE kan utföra en kaskad av omvandlingar: bilda azetidinringen, införa hydroxylgrupper, omvandla en alkohol till en karboxylsyra, bryta bindningar i den ursprungliga ramen och till och med installera en extra liten treledad syre-ring (en epoxid). Genom att variera mängden av dess kosubstrat, alfa‑ketoglutarat, och mata OkaE med olika mellanprodukter kartlade teamet hur dessa reaktioner förgrenar sig från en enda utgångsmolekyl inom en eller några enzymcykler.
Hur form och rörelse styr reaktionerna
För att se hur OkaE väljer mellan dessa möjligheter löste författarna högupplösta kristallstrukturer av enzymet bundet till metall, hjälpämne och okaramine A, och kombinerade dem med kvantmekaniska datorsimuleringar. OkaE har det klassiska "jelly‑roll"-veckade formatet som är typiskt för dess enzymfamilj, men dess aktiva säte är dekorerat med svavelinnehållande metioninrester och en tryptofan som omsluter ena änden av okaramine genom subtila ”Met–π”‑interaktioner mellan svavelatomer och aromatiska ringar. Detta nätverk håller substratet så att två specifika positioner — en på en kolatom intill azetidinringen och en på en närliggande hydroxylgrupp — pekar mot det reaktiva järn–oxygen‑centret. Simulatorer visar att efter syreativering vrider sig järn–oxygen‑fragmentet till en orientering där det kan abstrahera ett väte från endera platsen, vilket skapar en förgrening i reaktionsvägen. Att förändra enstaka rester i metionin–tryptofan‑nätverket skjuter substratet närmare den ena eller andra platsen, vilket förenklar produktmängden eller till och med får OkaE:s aktivitet att kollapsa till en enda huvudreaktion.
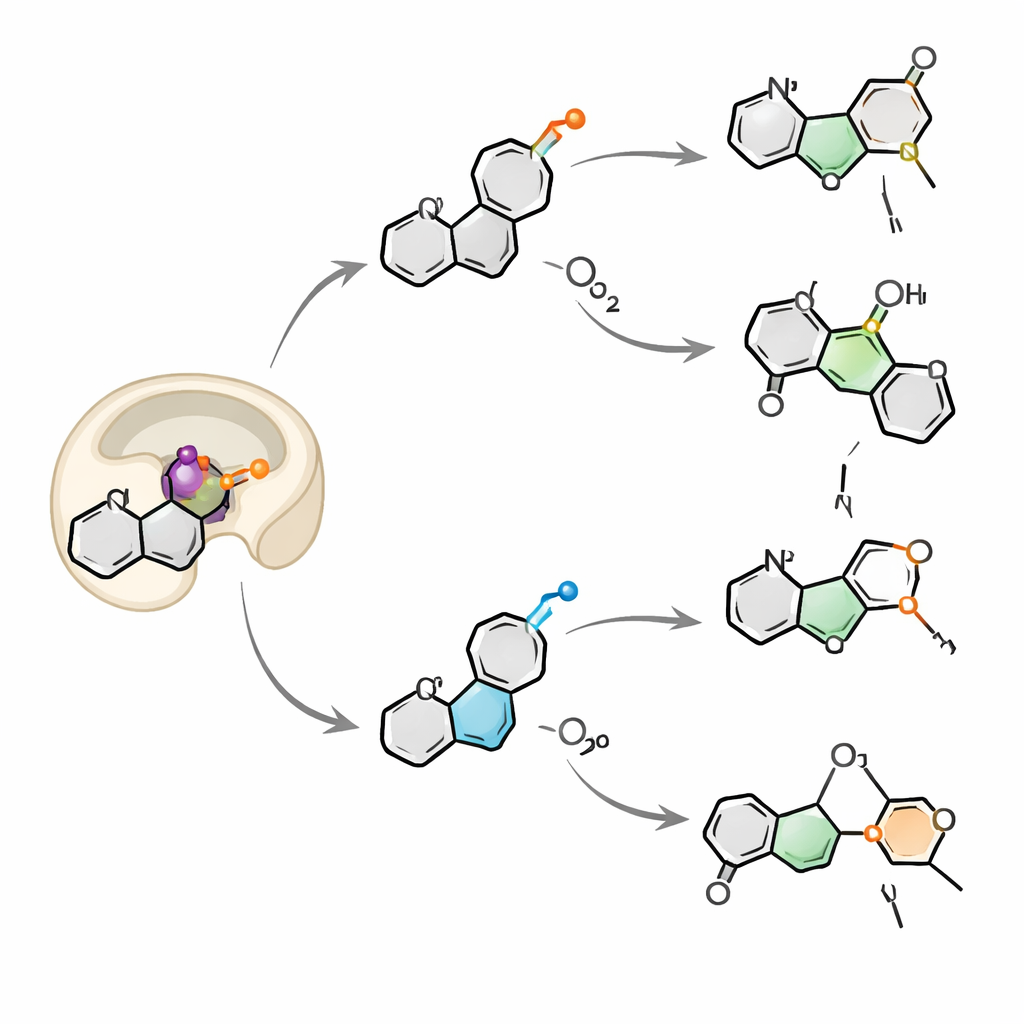
Att andas in två syre samtidigt
Genom att spåra syreatomer märkta med den tyngre isotopen 18O upptäckte teamet att OkaE hämtar syre från både molekylärt syre i luften och från vatten i lösningen. För de flesta produkter kan syret som är bundet till järnet bytas ut med vatten innan det hamnar i molekylen, vilket förklarar de blandade märkningsmönstren. En produkt, neuokaramine IV, skilde ut sig: dess mönster kunde endast förklaras om en andra syremolekyl fångas upp och byggs in i samma substrat inom en enda katalytisk cykel, vilket bildar och sedan bryter en känslig peroxidbrygga. Denna "två‑andas"‑mekanism är extremt sällsynt för denna enzymfamilj och understryker hur flexibelt OkaE kan koreografera radikala och positivt laddade mellanprodukter inom samma aktiva säte.
Vad detta betyder för framtida design
Enkelt uttryckt är OkaE ett molekylärt multiverktyg. Det kan inte bara sammanfoga en svår ring som kemister kämpar med att framställa, utan också omforma den ringen och dess omgivning till flera distinkta skelett — allt medan det drivs av luft, järn och en enkel cellulär syra. Genom att avslöja hur ett specifikt interaktionsnätverk i proteinet positionerar sitt substrat och hur en vridande järn–oxygen‑enhet öppnar olika reaktionskanaler ger detta arbete en ritning för att designa "programmerbara" biokatalysatorer. Sådana skräddarsydda enzymer kan effektivisera sentida modifieringar av naturprodukter och hjälpa kemister att framställa bättre läkemedel och insektsmedel med mindre avfall och större precision.
Citering: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Nyckelord: azetidinbiosyntes, icke‑hemjärnenzym, okaramine‑insektsgifter, biokatalysator‑engineering, oxidativa kaskadreaktioner