Clear Sky Science · pl
Strukturalne i mechanistyczne spojrzenie na związany z azetydyną enzym αKG‑NHFe OkaE o wielofunkcyjnej katalizie
Dlaczego mały enzym ma znaczenie dla przyszłych leków i pestycydów
Wiele silnych leków i insektycydów opiera się na złożonych, pierścieniowych cząsteczkach, które trudno zsyntetyzować metodami chemicznymi. To badanie ujawnia, jak pojedynczy enzym grzybowy, nazwany OkaE, potrafi ukształtować jeden z takich pierścieni — nietypowo napięty, czteroczłonowy azetydyn — a następnie wielokrotnie przekształcić tę cząsteczkę na różne sposoby. Zrozumienie działania OkaE może zainspirować bardziej ekologiczne drogi do nowych leków i wysoce selektywnych środków ochrony roślin, które oszczędzają ludzi i inne kręgowce.
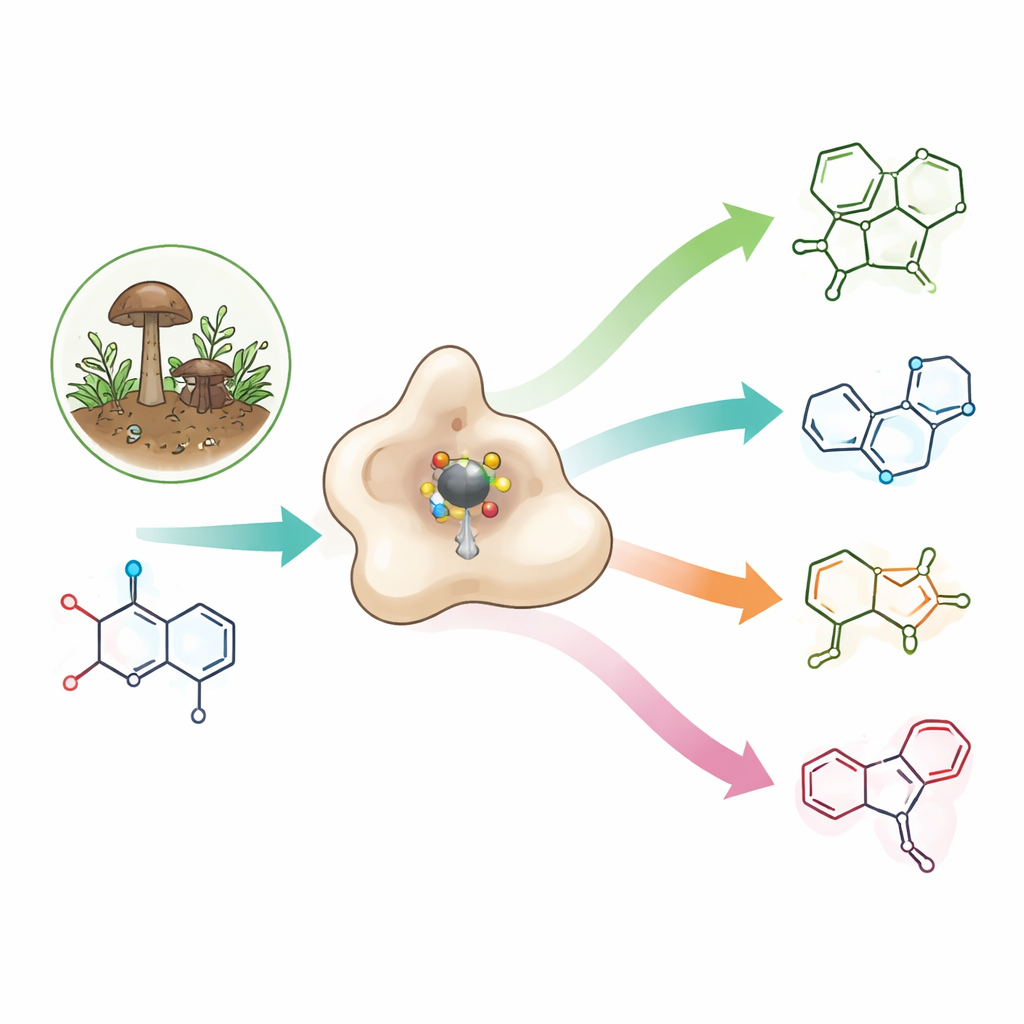
Rzadki element budulcowy o dużym potencjale farmaceutycznym
Azetydyny to małe, czteroczłonowe pierścienie zawierające azot, które kumulują dużo naprężenia w niewielkiej strukturze. To naprężenie często przekłada się na użyteczne właściwości: azetydyny mogą poprawiać dopasowanie leków do ich celów, ich dystrybucję w organizmie i rozpuszczalność w wodzie. Występują już w badanych antybiotykach, środkach przeciwnowotworowych i potencjalnych lekach na Alzheimera, a także w okaraminach — naturalnych insektycydach wytwarzanych przez niektóre grzyby, które selektywnie wyłączają kanały nerwowe u bezkręgowców, nie naruszając kanałów u ludzi. Jednak ponieważ pierścienie azetydynowe są tak naprężone i niestabilne, chemicy zwykle potrzebują kilku energochłonnych etapów i ostrych warunków, by je wytworzyć.
Nietypowe rozwiązanie natury: enzym OkaE
Grzyby rozwiązują ten problem za pomocą wyspecjalizowanych enzymów. Większość znanych enzymów tworzących azetydyny łączy atom węgla z atomem azotu przy użyciu powszechnego kofaktora komórkowego zwanego SAM. OkaE łamie tę zasadę. Należy do dużej rodziny enzymów zależnych od żelaza, które zazwyczaj wprowadzają atomy tlenu do cząsteczek. OkaE wykorzystuje żelazo i pomocniczą cząsteczkę — alfa‑ketoglutaran — aby utworzyć wysoce reaktywny fragment żelazo–tlen zdolny do odrywania atomów wodoru z substratu, okaraminy A. W przeciwieństwie do bliźniaczych enzymów, OkaE tworzy pierścień azetydynowy, tworząc nowe wiązanie węgiel–węgiel wewnątrz już złożonego produktu naturalnego, co czyni go wyróżnikiem nawet w tej bardzo wszechstronnej rodzinie enzymów.
Jeden enzym, wiele chemicznych sztuczek
Kiedy badacze zbadali oczyszczony OkaE w probówce, spodziewali się jedynie utworzenia azetydyny i prostego utlenienia. Zamiast tego odkryli małą fabrykę chemiczną. Rozpoczynając od okaraminy A, OkaE wytworzył co najmniej cztery nowe cząsteczki, nazwane neuokaraminami I–IV, oprócz znanych pośredników. Produkty te wykazały, że OkaE może przeprowadzać kaskadę przekształceń: tworzenie pierścienia azetydynowego, dodawanie grup hydroksylowych, przekształcanie alkoholu w kwas karboksylowy, rozrywanie wiązań w pierwotnym szkielecie, a nawet wprowadzanie dodatkowego, małego trójczłonowego pierścienia zawierającego tlen (epoksyd). Poprzez zmienianie ilości jego ko‑substratu, alfa‑ketoglutaranu, oraz podawanie OkaE różnych pośredników, zespół odwzorował, jak te reakcje rozgałęziają się z pojedynczej cząsteczki wyjściowej w ramach jednego lub kilku cykli enzymatycznych.
Jak kształt i ruch kierują reakcjami
Aby zobaczyć, jak OkaE wybiera między tymi możliwościami, autorzy rozwiązali struktury krystaliczne enzymu o wysokiej rozdzielczości związane z metalem, cząsteczką pomocniczą i okaraminą A, i połączyli je z symulacjami komputerowymi na poziomie kwantowym. OkaE ma klasyczny fałd „jelly‑roll” charakterystyczny dla jego rodziny, ale jego miejsce aktywne jest ozdobione resztami metioniny zawierającymi siarkę oraz tryptofanem, które podtrzymują jeden koniec okaraminy przez subtelne oddziaływania „Met–π” między atomami siarki a pierścieniami aromatycznymi. Ta sieć utrzymuje substrat tak, że dwie specyficzne pozycje — jedna na atomie węgla obok pierścienia azetydynowego i jedna na pobliskiej grupie hydroksylowej — skierowane są ku reaktywnemu centrum żelazo–tlen. Symulacje pokazują, że po aktywacji tlenu fragment żelazo–tlen obraca się do orientacji, w której może oderwać wodór z któregokolwiek z tych miejsc, tworząc widełki w ścieżce reakcji. Zmiana pojedynczych reszt w sieci metionina–tryptofan przesuwa substrat bliżej jednego lub drugiego miejsca, upraszczając mieszaninę produktów, a nawet redukując aktywność OkaE do jednej dominującej reakcji.
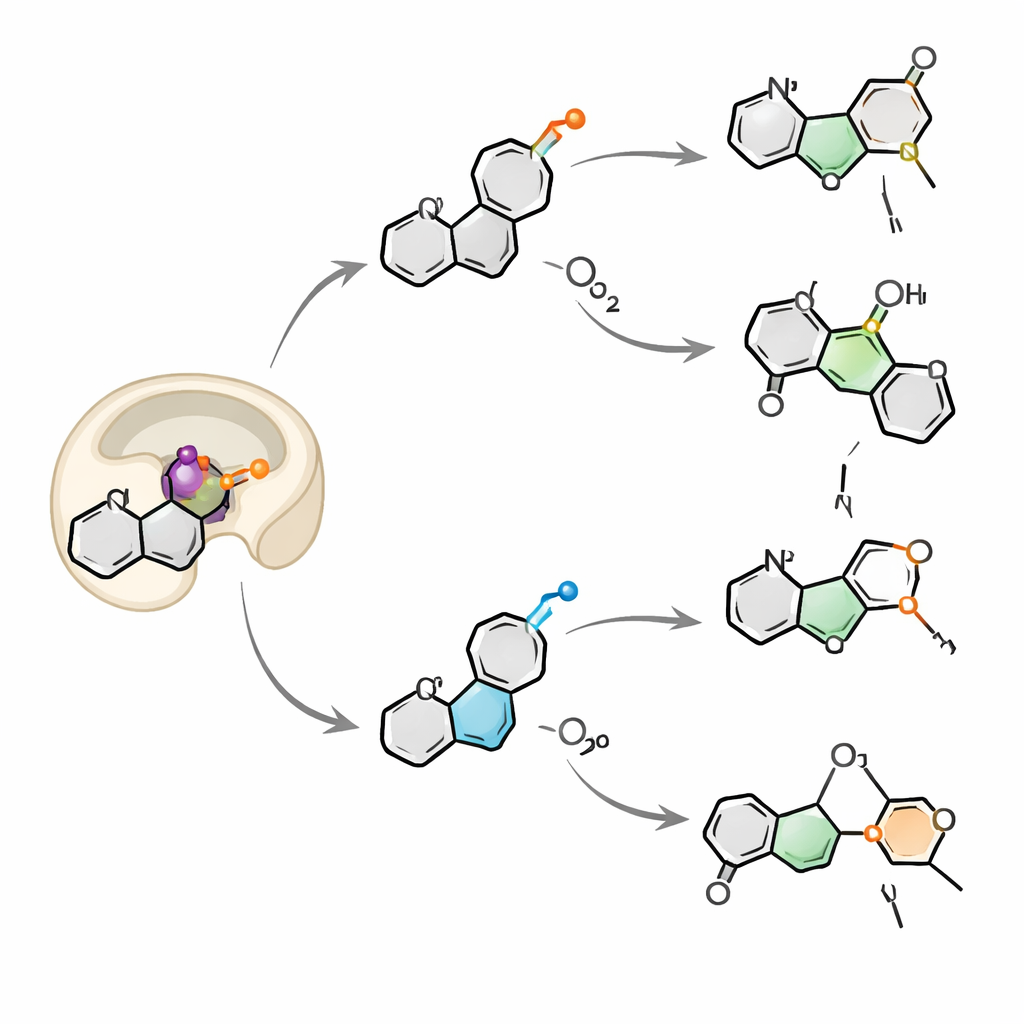
Wdychanie dwóch atomów tlenu naraz
Śledząc atomy tlenu znakowane cięższym izotopem 18O, zespół odkrył, że OkaE czerpie tlen zarówno z tlenu cząsteczkowego w powietrzu, jak i z wody w roztworze. Dla większości produktów tlen związany z żelazem może wymieniać się z wodą zanim trafi do cząsteczki, co wyjaśnia mieszane wzory znakowania. Jeden produkt, neuokaramina IV, wyróżniał się: jego wzór można wyjaśnić tylko wtedy, gdy drugi atom tlenu zostaje uchwycony i wbudowany w ten sam substrat w ramach pojedynczego cyklu katalitycznego, tworząc, a potem rozrywając delikatny mostek nadtlenkowy. Ten mechanizm „dwóch oddechów” jest niezwykle rzadki dla tej rodziny enzymów i podkreśla, jak elastycznie OkaE potrafi koordynować rodnikowe i dodatnio naładowane pośredniki w tym samym miejscu aktywnym.
Co to oznacza dla przyszłego projektowania
Mówiąc prosto, OkaE to molekularne narzędzie wielofunkcyjne. Potrafi nie tylko złożyć trudny pierścień, z którym chemicy mają problemy, ale też przekształcić ten pierścień i jego otoczenie w kilka odmiennych szkieletów — wszystko to działając na powietrzu, żelazie i prostym kwasie komórkowym. Ujawniając, jak specyficzna sieć oddziaływań w białku pozycjonuje substrat i jak obracający się fragment żelazo–tlen otwiera różne kanały reakcyjne, ta praca dostarcza wzorca do projektowania „programowalnych” biokatalizatorów. Takie dopasowane enzymy mogłyby uprościć modyfikacje naturalnych produktów na późnych etapach syntezy, pomagając chemikom tworzyć lepsze leki i insektycydy przy mniejszej ilości odpadów i większej precyzji.
Cytowanie: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Słowa kluczowe: biosynteza azetydyn, enzym niehemowy żelazowy, owadobójcze okaraminy, inżynieria biokatalizatorów, reakcje kaskadowe utleniające