Clear Sky Science · fr
Aperçus structuraux et mécanistiques de l’enzyme αKG-NHFe associé à l’azetidine, OkaE, à catalyse multifonctionnelle
Pourquoi une minuscule enzyme compte pour les médicaments et pesticides de demain
Beaucoup de médicaments puissants et d’insecticides reposent sur des molécules complexes en anneau qui sont difficiles à synthétiser chimiquement. Cette étude révèle comment une unique enzyme fongique, nommée OkaE, peut façonner l’un de ces anneaux — une azetidine à quatre membres, inhabituellement tendue — puis remodeler la molécule de plusieurs manières différentes. Comprendre le fonctionnement d’OkaE pourrait inspirer des voies plus écologiques vers de nouveaux médicaments et des agents de lutte antiparasitaire très sélectifs qui épargnent les humains et autres vertébrés.
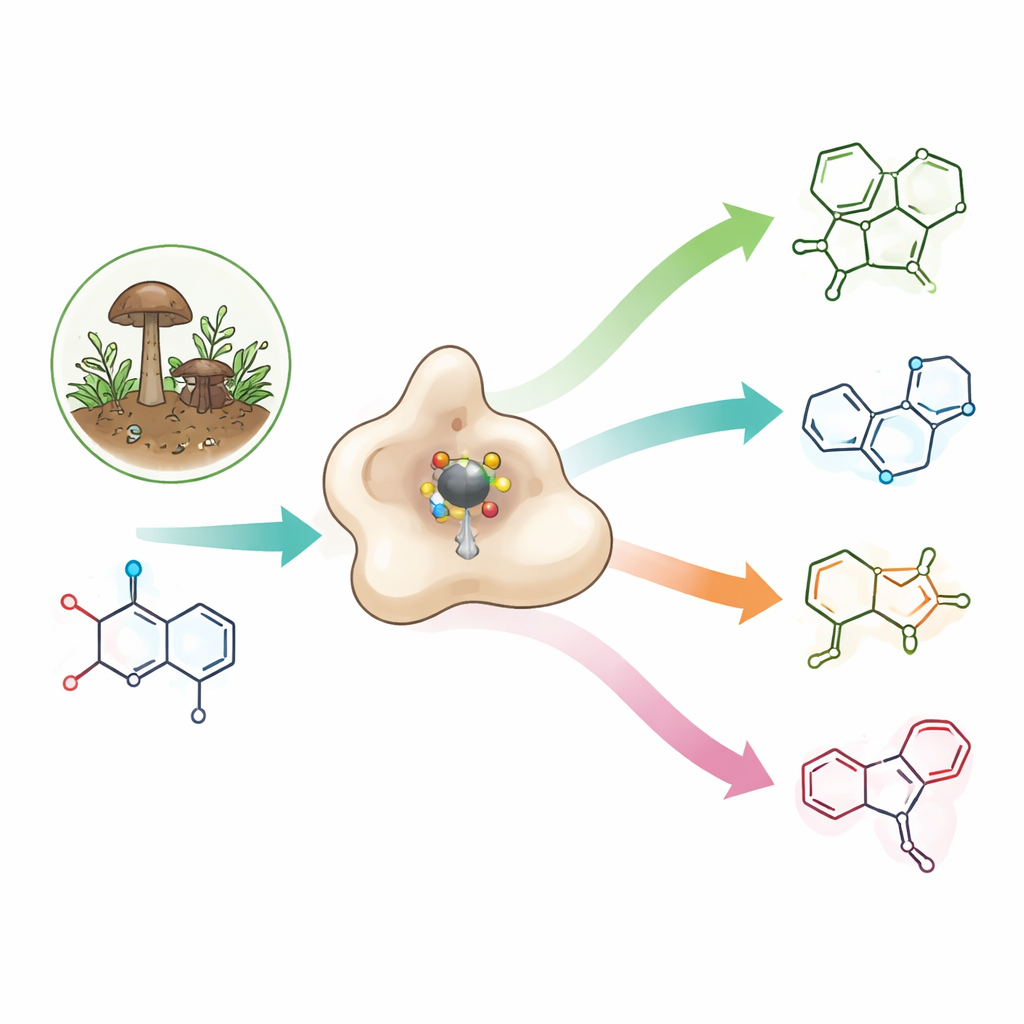
Un bloc de construction rare au fort potentiel pharmaceutique
Les azetidines sont de petits anneaux azotés à quatre membres qui concentrent beaucoup de tension dans un espace réduit. Cette tension confère souvent des propriétés utiles : les azetidines peuvent améliorer l’ajustement d’une molécule médicamenteuse à sa cible, sa mobilité dans l’organisme et sa solubilité dans l’eau. On les trouve déjà dans des antibiotiques expérimentaux, des agents anticancéreux et des candidats contre la maladie d’Alzheimer, ainsi que dans les okaramines — des insecticides naturels produits par certains champignons qui désactivent sélectivement des canaux nerveux chez les invertébrés tout en laissant intactes les versions humaines. Pourtant, parce que les anneaux d’azetidine sont si tendus et instables, les chimistes doivent généralement recourir à plusieurs étapes énergivores et à des conditions sévères pour les synthétiser.
La solution inhabituelle de la nature : l’enzyme OkaE
Les champignons affrontent ce défi à l’aide d’enzymes spécialisées. La plupart des enzymes connues formant des azetidines lient un atome de carbone à un atome d’azote en utilisant un cofacteur cellulaire courant appelé SAM. OkaE rompt cette règle. Elle appartient à une grande famille d’enzymes dépendantes du fer qui insèrent normalement des atomes d’oxygène dans des substrats. OkaE utilise le fer et une molécule auxiliaire, l’alpha‑céto‑glutarate, pour former une espèce fer–oxygène hautement réactive capable d’arracher des atomes d’hydrogène à son substrat, l’okaramine A. Contrairement à ses parentes, OkaE forge l’anneau d’azetidine en créant une nouvelle liaison carbone–carbone à l’intérieur de ce produit naturel déjà complexe, ce qui en fait une exception même au sein d’une famille d’enzymes très versatile.
Une enzyme, de nombreux tours chimiques
Quand les chercheurs ont étudié OkaE purifiée en éprouvette, ils s’attendaient à observer seulement la formation de l’azetidine et une oxydation simple. Ils ont trouvé à la place une petite usine chimique. À partir de l’okaramine A, OkaE a produit au moins quatre nouvelles molécules, nommées neuokaramines I–IV, en plus d’intermédiaires connus. Ces produits montrent qu’OkaE peut réaliser une cascade de transformations : formation de l’azetidine, ajout de groupes hydroxyle, conversion d’un alcool en acide carboxylique, ouverture de liaisons dans le squelette originel, et même installation d’un petit anneau oxygéné à trois membres (un époxyde). En variant la quantité de son co‑substrat, l’alpha‑céto‑glutarate, et en alimentant OkaE avec différents intermédiaires, l’équipe a cartographié comment ces réactions se ramifient à partir d’une molécule unique au sein d’un ou de quelques cycles enzymatiques.
Comment la forme et le mouvement orientent les réactions
Pour comprendre comment OkaE choisit entre ces possibilités, les auteurs ont résolu des structures cristallines à haute résolution de l’enzyme liée au métal, au cofacteur et à l’okaramine A, et les ont combinées avec des simulations informatiques au niveau quantique. OkaE présente le pli classique en « jelly‑roll » de sa famille, mais son site actif est orné de résidus méthionine contenant du soufre et d’un tryptophane qui soutiennent une extrémité de l’okaramine via de subtiles interactions « Met–π » entre atomes de soufre et cycles aromatiques. Ce réseau maintient le substrat de sorte que deux positions spécifiques — l’une sur un carbone adjacent à l’azetidine, l’autre sur un groupe hydroxyle voisin — font face au centre réactif fer–oxygène. Les simulations montrent qu’après activation de l’oxygène, le fragment fer–oxygène pivote dans une orientation qui lui permet d’arracher un hydrogène depuis l’un ou l’autre site, créant une bifurcation dans la voie réactionnelle. Modifier un seul résidu du réseau méthionine–tryptophane rapproche le substrat d’un site plutôt que de l’autre, simplifiant le mélange de produits ou même réduisant l’activité d’OkaE à une seule réaction principale.
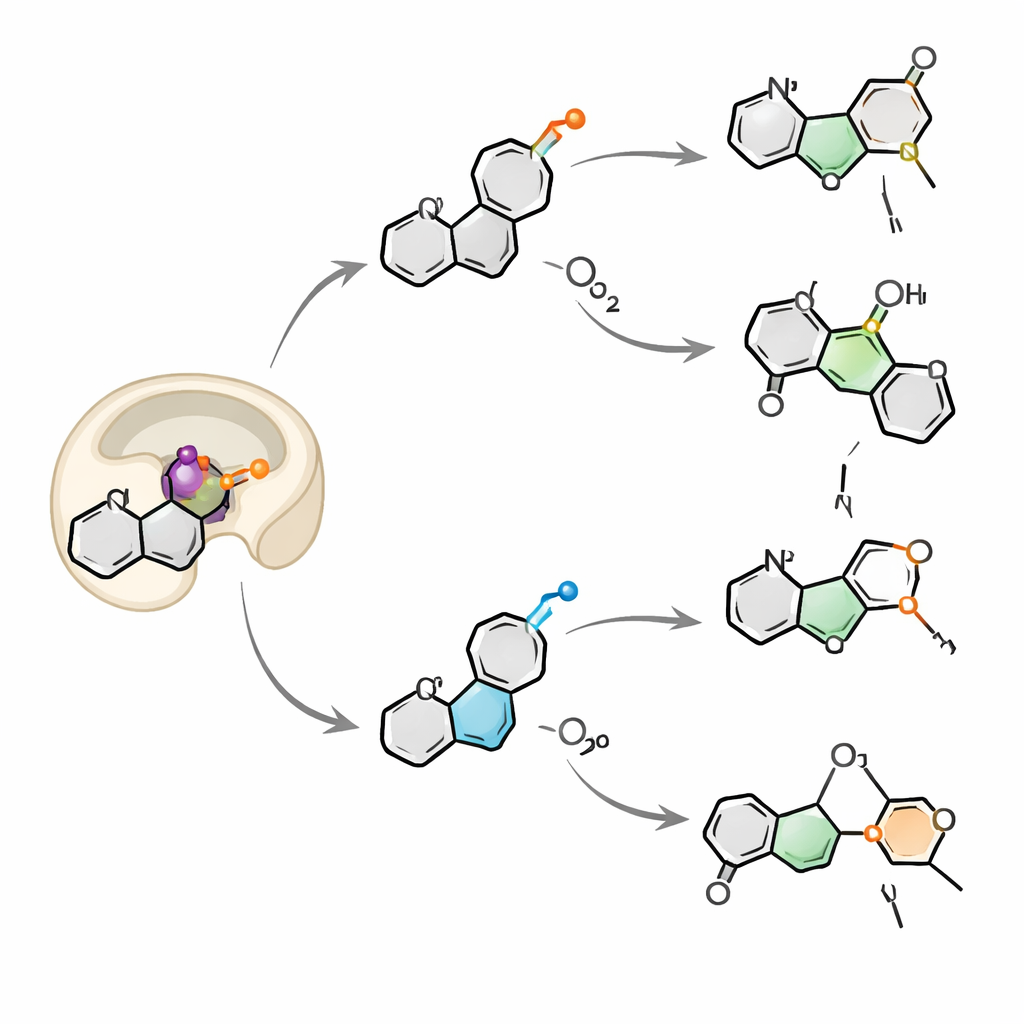
Respirer deux oxygènes à la fois
En traçant des atomes d’oxygène marqués avec l’isotope plus lourd 18O, l’équipe a découvert qu’OkaE puise l’oxygène à la fois dans l’oxygène moléculaire de l’air et dans l’eau en solution. Pour la plupart des produits, l’oxygène lié au fer peut échanger avec l’eau avant d’aboutir dans la molécule, expliquant les schémas de marquage mixtes. Un produit, neuokaramine IV, s’est distingué : son schéma ne pouvait s’expliquer que si une seconde molécule d’oxygène était capturée et incorporée dans le même substrat au cours d’un seul cycle catalytique, formant puis rompant un pont peroxyde délicat. Ce mécanisme de « double respiration » est extrêmement rare pour cette famille d’enzymes et souligne la flexibilité d’OkaE à orchestrer des intermédiaires radicaux et chargés positivement au sein d’un même site actif.
Ce que cela implique pour la conception future
En termes simples, OkaE est un outil moléculaire polyvalent. Elle peut non seulement assembler un anneau difficile que les chimistes peinent à fabriquer, mais aussi refaçonner cet anneau et son environnement en plusieurs échafaudages distincts — tout en fonctionnant à l’air, au fer et à un simple acide métabolique. En révélant comment un réseau d’interactions spécifique dans la protéine positionne son substrat et comment une unité fer–oxygène pivotante ouvre différentes voies réactionnelles, ce travail fournit une feuille de route pour l’ingénierie de biocatalyseurs « programmables ». De tels enzymes sur mesure pourraient simplifier la modification en fin d’étape des produits naturels, aidant les chimistes à concevoir de meilleurs médicaments et insecticides avec moins de déchets et une plus grande précision.
Citation: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Mots-clés: biosynthèse de l’azetidine, enzyme non‑hémique à fer, insecticides okaramines, ingénierie de biocatalyseurs, réactions en cascade oxydatives