Clear Sky Science · it
Approfondimenti strutturali e meccanicistici sull’enzima αKG‑NHFe associato all’azetidina OkaE con catalisi multifunzionale
Perché un piccolo enzima conta per i farmaci e i pesticidi del futuro
Molti farmaci potenti e insetticidi si basano su molecole complesse ad anello che sono difficili da costruire chimicamente. Questo studio rivela come un singolo enzima fungino, chiamato OkaE, possa plasmare uno di questi anelli—un’azetidina a quattro membri insolitamente tesa—e poi rimodellare ulteriormente la molecola in modi diversi. Comprendere come funziona OkaE potrebbe ispirare vie più verdi per nuovi farmaci e agenti di controllo degli insetti altamente selettivi che risparmino gli esseri umani e altri vertebrati.
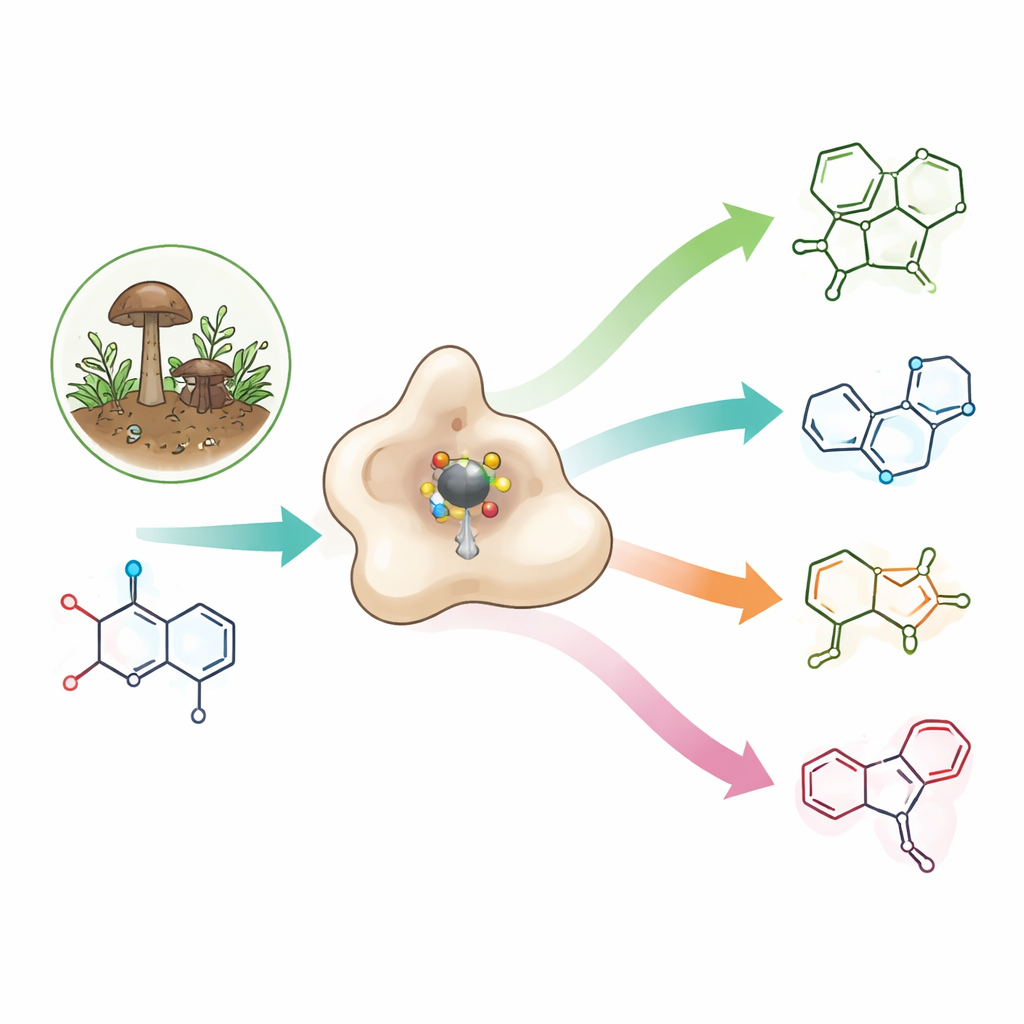
Un blocco da costruzione raro con grande promessa farmaceutica
Le azetidine sono minuscoli anelli azotati a quattro membri che accumulano molta tensione in uno spazio ridotto. Questa tensione si traduce spesso in proprietà utili: le azetidine possono migliorare il modo in cui le molecole farmaceutiche si legano ai loro bersagli, si distribuiscono nell’organismo e si solubilizzano in acqua. Appaiono già in antibiotici sperimentali, agenti anticancro e potenziali farmaci per l’Alzheimer, oltre che nelle okaramine—insetticidi naturali prodotti da alcuni funghi che disabilitano selettivamente canali nervosi negli invertebrati lasciando intatti quelli umani. Tuttavia, poiché gli anelli di azetidina sono così tesi e instabili, i chimici di solito necessitano di diversi passaggi energivori e condizioni aggressive per costruirli.
La soluzione insolita della natura: l’enzima OkaE
I funghi affrontano questa sfida con enzimi specializzati. La maggior parte degli enzimi noti che formano azetidine collega un atomo di carbonio a un atomo di azoto usando un cofattore cellulare comune chiamato SAM. OkaE infrange quella regola. Appartiene a una grande famiglia di enzimi dipendenti dal ferro che normalmente inseriscono atomi di ossigeno nelle molecole. OkaE utilizza ferro e una molecola ausiliaria, l’alfa‑chetoglutarato, per formare una specie ferro‑ossigeno altamente reattiva capace di strappare atomi di idrogeno dal suo substrato, l’okaramina A. Diversamente dai suoi parenti, OkaE forgia l’anello di azetidina creando un nuovo legame carbonio‑carbonio all’interno di questo prodotto naturale già complesso, rendendolo un’anomalia anche all’interno di una famiglia enzimatica molto versatile.
Un enzima, molti trucchi chimici
Quando i ricercatori hanno studiato OkaE purificato in provetta, si aspettavano solo la formazione dell’azetidina e una semplice ossidazione. Invece hanno trovato una piccola fabbrica chimica. Partendo dall’okaramina A, OkaE ha prodotto almeno quattro nuove molecole, chiamate neuokaramine I–IV, oltre a intermedi noti. Questi prodotti hanno mostrato che OkaE può eseguire una cascata di trasformazioni: formare l’anello di azetidina, aggiungere gruppi ossidrilici, convertire un alcool in un acido carbossilico, aprire legami nella struttura originale e persino installare un ulteriore anello ossigenato a tre membri (un epossido). Variando la quantità del co‑substrato, l’alfa‑chetoglutarato, e alimentando OkaE con diversi intermedi, il team ha mappato come queste reazioni si diramino a partire da una singola molecola iniziale in uno o pochi cicli enzimatici.
Come forma e movimento guidano le reazioni
Per capire come OkaE seleziona tra queste possibilità, gli autori hanno risolto strutture cristalline ad alta risoluzione dell’enzima legato al metallo, alla molecola ausiliaria e all’okaramina A, e le hanno combinate con simulazioni computazionali a livello quantistico. OkaE presenta il classico ripiegamento a “jelly‑roll” della sua famiglia enzimatica, ma il suo sito attivo è decorato con residui di metionina contenenti zolfo e con un triptofano che cullano un’estremità dell’okaramina tramite sottili interazioni “Met–π” tra atomi di zolfo e anelli aromatici. Questa rete mantiene il substrato in modo che due posizioni specifiche—una su un carbonio adiacente all’anello di azetidina e una su un gruppo ossidrilico vicino—puntino verso il centro ferro‑ossigeno reattivo. Le simulazioni mostrano che, dopo l’attivazione dell’ossigeno, il frammento ferro‑ossigeno ruota in un’orientazione dove può estrarre un idrogeno da entrambe le posizioni, creando una biforcazione nel percorso reattivo. La modifica di singoli residui nella rete metionina–triptofano spinge il substrato più vicino a un sito o all’altro, semplificando la miscela di prodotti o addirittura facendo collassare il comportamento di OkaE verso una singola reazione principale.
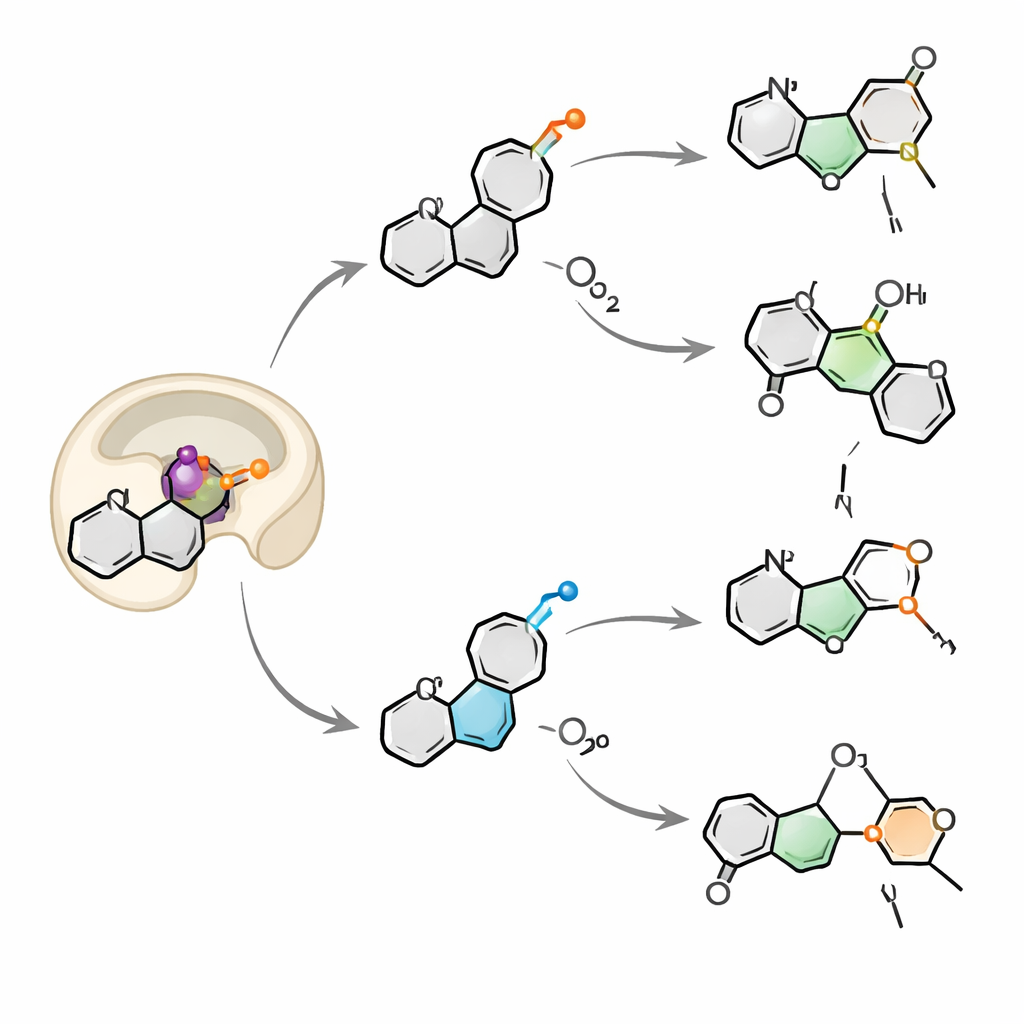
Inspirare due ossigeni contemporaneamente
Tracciando atomi di ossigeno etichettati con l’isotopo più pesante 18O, il team ha scoperto che OkaE attinge ossigeno sia dall’ossigeno molecolare nell’aria sia dall’acqua in soluzione. Per la maggior parte dei prodotti, l’ossigeno legato al ferro può scambiare con l’acqua prima di finire nella molecola, spiegando i pattern di etichettatura misti. Un prodotto, neuokaramine IV, si è distinto: il suo pattern poteva essere spiegato solo se una seconda molecola di ossigeno fosse catturata e incorporata nello stesso substrato all’interno di un singolo ciclo catalitico, formando e poi rompendo un delicato ponte perossido. Questo meccanismo a “doppio respiro” è estremamente raro per questa famiglia enzimatica e sottolinea quanto OkaE possa orchestrare in modo flessibile intermedi radicalici e carichi positivi all’interno dello stesso sito attivo.
Cosa significa per il design futuro
In termini pratici, OkaE è un coltellino molecolare. Non solo può assemblare un anello difficile che i chimici faticano a ottenere, ma può anche riforgiare quell’anello e l’intorno in diversi scaffolds distinti—tutto funzionando con aria, ferro e un semplice acido cellulare. Rivelando come una specifica rete di interazioni nella proteina posizioni il suo substrato e come un’unità ferro‑ossigeno rotante apra diversi canali reattivi, questo lavoro fornisce un progetto per l’ingegneria di biocatalizzatori “programmabili”. Enzimi su misura di questo tipo potrebbero semplificare la modifica in fase avanzata di prodotti naturali, aiutando i chimici a costruire farmaci e insetticidi migliori con meno spreco e maggiore precisione.
Citazione: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Parole chiave: biosintesi dell’azetidina, enzima non eme a ferro, insetticidi okaramine, ingegneria dei biocatalizzatori, reazioni a cascata ossidative