Clear Sky Science · pt
Percepções estruturais e mecanísticas sobre a enzima αKG-NHFe OkaE associada à azetidina com catálise multifuncional
Por que uma enzima minúscula importa para medicamentos e pesticidas do futuro
Muitos fármacos e inseticidas potentes dependem de moléculas complexas em anel que são difíceis de construir pelos químicos. Este estudo revela como uma única enzima fúngica, chamada OkaE, pode esculpir um desses anéis—uma azetidina de quatro membros, surpreendentemente tensionada—e então remodelar a molécula de várias maneiras diferentes. Entender como a OkaE funciona pode inspirar rotas mais verdes para novos medicamentos e agentes de controle de insetos altamente seletivos que poupem humanos e outros vertebrados.
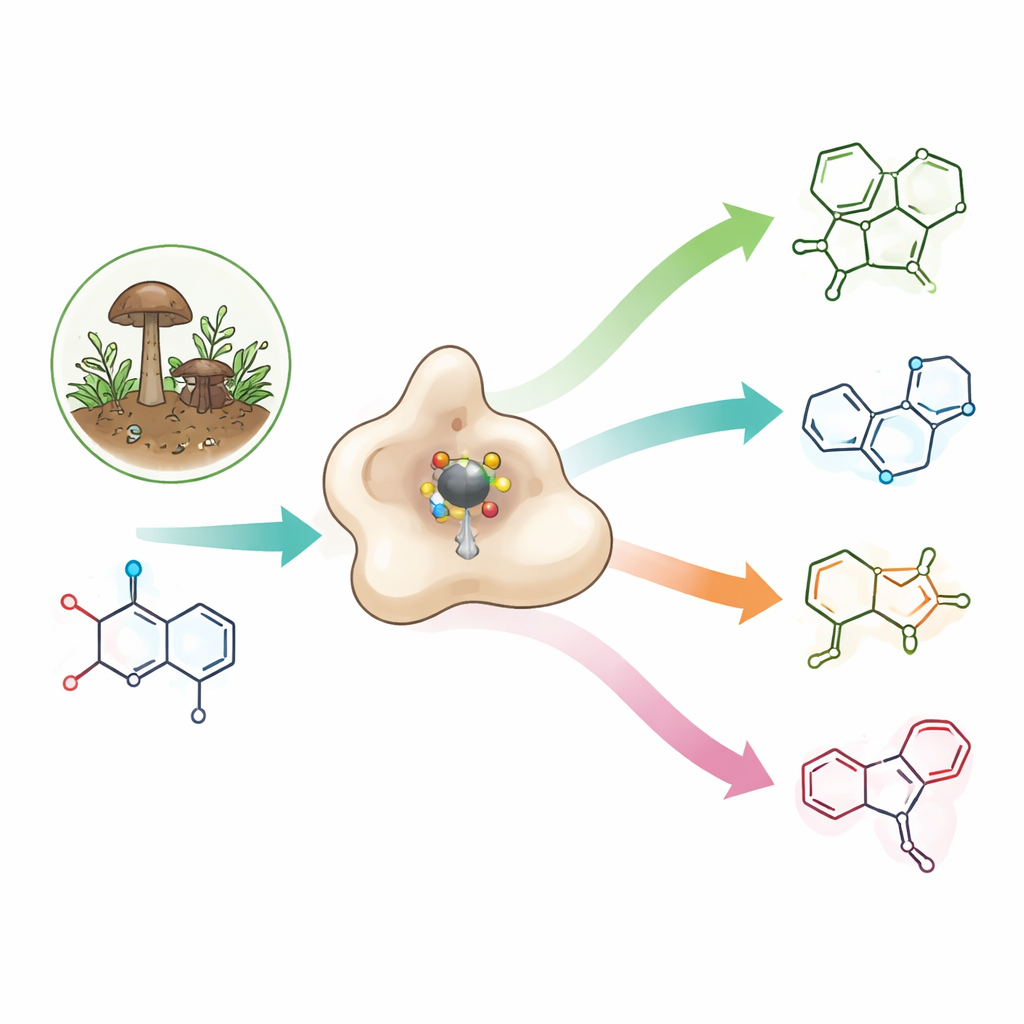
Um bloco de construção raro com grande promessa farmacêutica
Azetidinas são minúsculos anéis de nitrogênio de quatro membros que acumulam muita tensão em um espaço pequeno. Essa tensão frequentemente se traduz em propriedades úteis: azetidinas podem melhorar o encaixe de moléculas medicamentosas em seus alvos, sua movimentação pelo corpo e sua solubilidade em água. Já aparecem em antibióticos experimentais, agentes anticâncer e potenciais fármacos para Alzheimer, além das okaraminas—inseticidas naturais produzidos por certos fungos que desativam seletivamente canais nervosos de invertebrados deixando os canais humanos intactos. Ainda assim, porque os anéis de azetidina são tão tensionados e instáveis, os químicos geralmente precisam de vários passos energeticamente intensivos e condições severas para sintetizá‑los.
A solução incomum da natureza: a enzima OkaE
Fungos enfrentam esse desafio com enzimas especializadas. A maioria das enzimas conhecidas que formam azetidina une um átomo de carbono a um átomo de nitrogênio usando um cofator celular comum chamado SAM. A OkaE quebra essa regra. Ela pertence a uma grande família de enzimas dependentes de ferro que normalmente inserem átomos de oxigênio em moléculas. A OkaE usa ferro e uma molécula auxiliar, o alfa‑cetoglutarato, para gerar uma espécie ferro–oxigênio altamente reativa capaz de arrancar átomos de hidrogênio de seu substrato, a okaramina A. Ao contrário de suas parentes, a OkaE forja o anel de azetidina criando uma nova ligação carbono–carbono dentro desse já complexo produto natural, caracterizando‑a como uma exceção mesmo dentro de uma família enzimática muito versátil.
Uma enzima, muitos truques químicos
Quando os pesquisadores estudaram a OkaE purificada em tubo de ensaio, esperavam apenas a formação da azetidina e uma simples oxidação. Em vez disso, encontraram uma pequena fábrica química. Partindo da okaramina A, a OkaE produziu pelo menos quatro novas moléculas, chamadas neuokaraminas I–IV, além de intermediários já conhecidos. Esses produtos mostraram que a OkaE pode realizar uma cascata de transformações: formar o anel de azetidina, adicionar grupos hidroxila, converter um álcool em um ácido carboxílico, abrir ligações na estrutura original e até instalar um pequeno anel oxigenado de três membros (um epóxido). Variando a quantidade de seu co‑substrato, o alfa‑cetoglutarato, e alimentando a OkaE com diferentes intermediários, a equipe mapeou como essas reações se ramificam a partir de uma única molécula inicial dentro de um ou poucos ciclos enzimáticos.
Como forma e movimento orientam as reações
Para ver como a OkaE seleciona entre essas possibilidades, os autores resolveram estruturas cristalinas de alta resolução da enzima ligada ao metal, ao cofator e à okaramina A, e as combinaram com simulações computacionais em nível quântico. A OkaE tem o clássico dobramento em “jelly‑roll” de sua família enzimática, mas seu sítio ativo é decorado com resíduos de metionina que contêm enxofre e um triptofano que encaixam uma extremidade da okaramina por sutis interações “Met–π” entre átomos de enxofre e anéis aromáticos. Essa rede mantém o substrato de modo que duas posições específicas—uma em um carbono próximo ao anel de azetidina e outra em um grupo hidroxila próximo—fiquem voltadas para o centro reativo ferro–oxigênio. Simulações mostram que, após a ativação do oxigênio, o fragmento ferro–oxigênio gira para uma orientação em que pode abstrair um hidrogênio de qualquer um dos dois sítios, criando uma bifurcação na via reacional. Alterar resíduos individuais na rede metionina–triptofano empurra o substrato para mais perto de um sítio ou de outro, simplificando a mistura de produtos ou até colapsando o comportamento da OkaE para uma única reação principal.
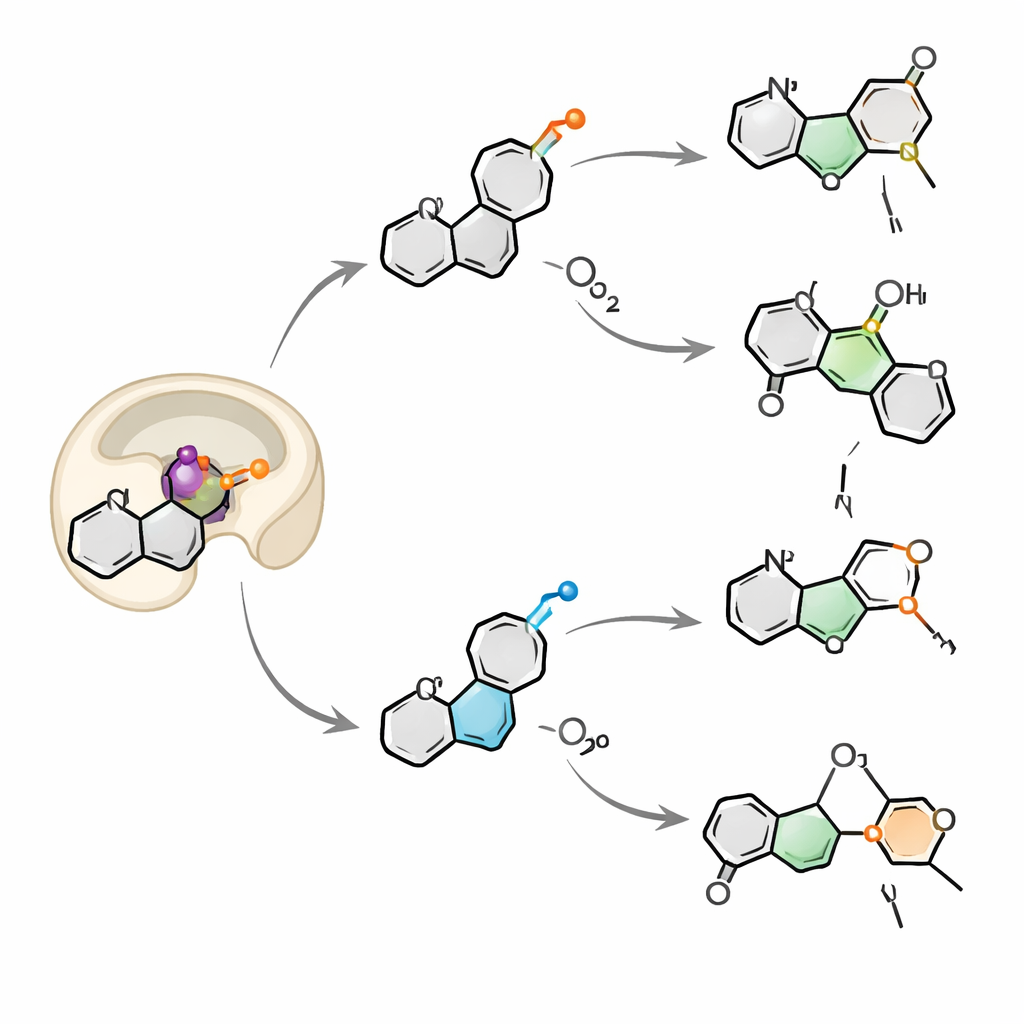
Inspirando dois oxigênios de uma vez
Rastreando átomos de oxigênio marcados com o isótopo mais pesado 18O, a equipe descobriu que a OkaE incorpora oxigênio tanto do oxigênio molecular do ar quanto da água em solução. Para a maioria dos produtos, o oxigênio ligado ao ferro pode trocar com a água antes de acabar na molécula, explicando os padrões mistos de marcação. Um produto, a neuokaramina IV, destacou‑se: seu padrão só pôde ser explicado se uma segunda molécula de oxigênio fosse capturada e incorporada ao mesmo substrato dentro de um único ciclo catalítico, formando e depois rompendo uma frágil ponte de peróxido. Esse mecanismo de “duas inspirações” é extremamente raro para essa família enzimática e ressalta quão flexivelmente a OkaE pode coreografar intermediários radicais e com carga positiva dentro do mesmo sítio ativo.
O que isso significa para projetos futuros
Em termos simples, a OkaE é uma ferramenta molecular multifuncional. Ela não apenas pode montar um anel difícil que os químicos têm dificuldade em sintetizar, como também remodelar esse anel e seu entorno em vários andaimes distintos—tudo isso funcionando com ar, ferro e um simples ácido celular. Ao revelar como uma rede de interações específica na proteína posiciona seu substrato e como uma unidade ferro–oxigênio giratória abre diferentes canais reacionais, este trabalho fornece um roteiro para engenharia de biocatalisadores “programáveis”. Enzimas assim adaptadas poderiam simplificar a modificação em etapas finais de produtos naturais, ajudando químicos a construir melhores medicamentos e inseticidas com menos desperdício e maior precisão.
Citação: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Palavras-chave: biossíntese de azetidina, enzima não-heme de ferro, inseticidas okaraminas, engenharia de biocatalisadores, reações de cascata oxidativa