Clear Sky Science · de
Strukturelle und mechanistische Einblicke in das azetidin‑assoziierte αKG‑NHFe‑Enzym OkaE mit multifunktionaler Katalyse
Warum ein winziges Enzym für künftige Medikamente und Pestizide wichtig ist
Viele wirksame Medikamente und Insektizide beruhen auf komplexen, ringförmigen Molekülen, die für Chemiker schwer zu synthetisieren sind. Diese Studie zeigt, wie ein einzelnes Pilzenzym namens OkaE einen solchen Ring – ein ungewöhnlich beanspruchtes viergliedriges Azetidin – formen kann und das Molekül anschließend auf verschiedene Weisen weiter umgestaltet. Das Verständnis, wie OkaE arbeitet, könnte umweltfreundlichere Wege zu neuen Wirkstoffen und hocheffizienten, selektiven Insektenbekämpfungsmitteln inspirieren, die Menschen und andere Wirbeltiere verschonen.
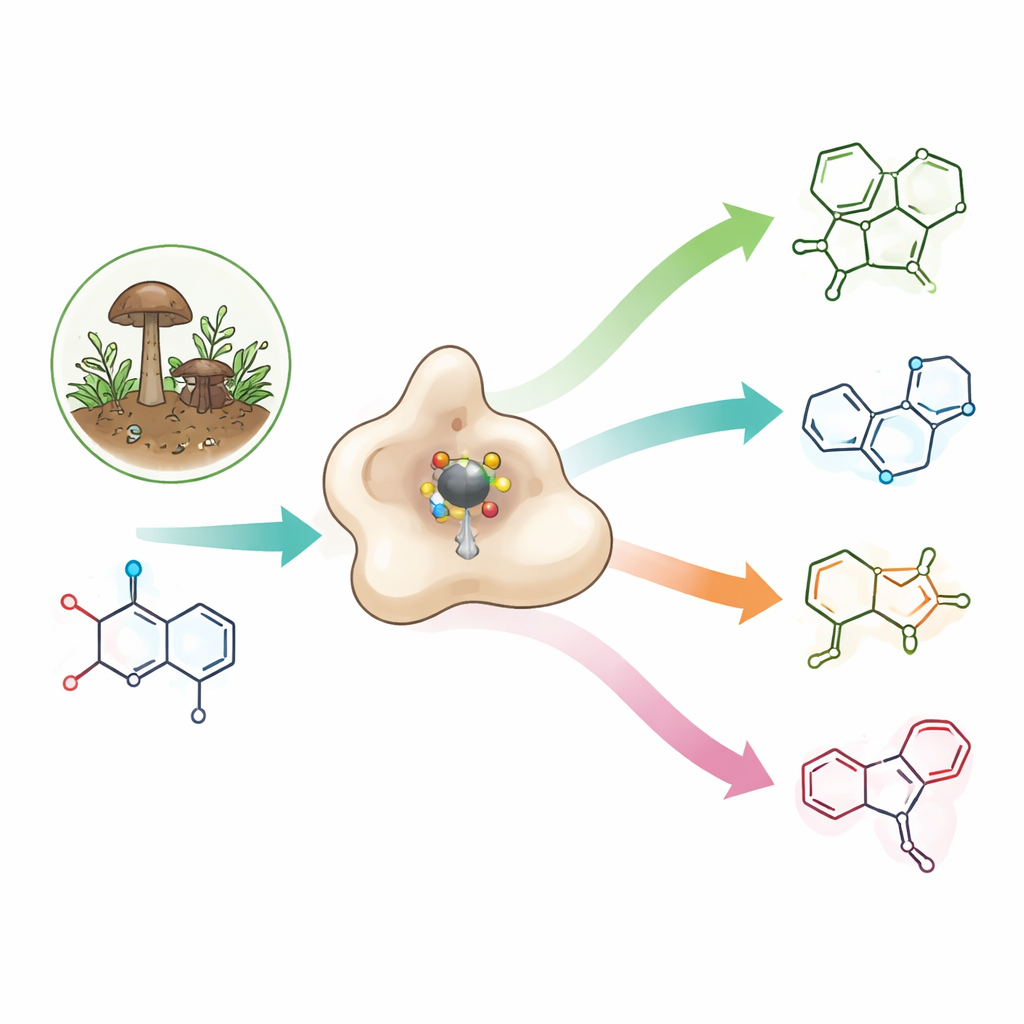
Ein seltenes Bausteinchen mit großem pharmazeutischem Potenzial
Azetidine sind winzige viergliedrige Stickstoffringe, die viel Ringspannung auf kleinem Raum speichern. Diese Spannung wirkt sich oft vorteilhaft aus: Azetidine können verbessern, wie Wirkstoffe an Zielstrukturen binden, sich im Körper verteilen und in Wasser lösen. Sie treten bereits in experimentellen Antibiotika, Krebsmedikamenten und potenziellen Alzheimer‑Medikamenten auf sowie in Okaraminen – natürlichen Insektiziden bestimmter Pilze, die Ionenkanäle bei Wirbellosen selektiv deaktivieren, während menschliche Kanäle verschont bleiben. Da Azetidinringe jedoch stark gespannt und instabil sind, benötigen Chemiker für ihre Herstellung meist mehrere energieaufwändige Schritte und harte Reaktionsbedingungen.
Natures ungewöhnliche Lösung: das Enzym OkaE
Pilze lösen dieses Problem mit spezialisierten Enzymen. Die meisten bekannten azetidinbildenden Enzyme koppeln ein Kohlenstoff‑ an ein Stickstoffatom mithilfe eines verbreiteten zellulären Kofaktors namens SAM. OkaE bricht diese Regel. Es gehört zu einer großen Familie eisenabhängiger Enzyme, die normalerweise Sauerstoffatome in Substrate einbauen. OkaE verwendet Eisen und ein Hilfsmolekül, α‑Ketoglutarat, um eine hochreaktive Eisen‑Sauerstoff‑Spezies zu bilden, die Wasserstoffatome aus dem Substrat Okaramin A abstrahieren kann. Anders als seine Verwandten formt OkaE den Azetidinring durch die Ausbildung einer neuen Kohlenstoff–Kohlenstoff‑Bindung innerhalb dieses bereits komplexen Naturprodukts und stellt damit selbst innerhalb einer sehr vielseitigen Enzymfamilie eine Ausnahme dar.
Ein Enzym, viele chemische Tricks
Als die Forscher gereinigtes OkaE im Reagenzglas untersuchten, erwarteten sie lediglich die Bildung des Azetidinrings und eine einfache Oxidation. Stattdessen entdeckten sie eine kleine Chemiefabrik. Ausgehend von Okaramin A erzeugte OkaE mindestens vier neue Moleküle, die Neuokaramine I–IV genannt wurden, zusätzlich zu bekannten Zwischenprodukten. Diese Produkte zeigten, dass OkaE eine Kaskade von Umwandlungen durchführen kann: die Bildung des Azetidinrings, Hinzufügen von Hydroxylgruppen, die Umwandlung eines Alkohols in eine Carbonsäure, das Öffnen von Bindungen im ursprünglichen Gerüst und sogar das Einführen eines zusätzlichen kleinen drei‑gliedrigen Sauerstoffrings (eines Epoxids). Durch Variation der Menge seines Co‑Substrats α‑Ketoglutarat und durch Zufüttern verschiedener Zwischenprodukte kartierte das Team, wie sich diese Reaktionen von einem einzigen Ausgangsmolekül aus verzweigen – innerhalb eines oder weniger Enzymzyklen.
Wie Form und Bewegung die Reaktionen lenken
Um zu sehen, wie OkaE zwischen diesen Möglichkeiten wählt, lösten die Autoren hochauflösende Kristallstrukturen des Enzyms mit gebundenem Metall, Hilfsmolekül und Okaramin A und kombinierten diese Daten mit quantenmechanischen Computersimulationen. OkaE zeigt die typische „Jelly‑Roll“‑Faltung seiner Enzymfamilie, doch sein aktives Zentrum ist mit schwefelhaltigen Methionin‑Resten und einem Tryptophan geschmückt, die ein Ende von Okaramin durch subtile „Met–π“‑Wechselwirkungen zwischen Schwefelatomen und aromatischen Ringen einbetten. Dieses Netzwerk hält das Substrat so, dass zwei spezifische Stellen – eine an einem Kohlenstoff neben dem Azetidinring und eine an einer benachbarten Hydroxylgruppe – dem reaktiven Eisen‑Sauerstoff‑Zentrum zugewandt sind. Simulationen zeigen, dass nach der Sauerstoffaktivierung das Eisen‑Sauerstoff‑Fragment in eine Orientierung schwenkt, in der es ein Wasserstoffatom von einer der beiden Stellen abstrahieren kann und dadurch eine Gabelung im Reaktionspfad erzeugt. Das Verändern einzelner Reste im Methionin–Tryptophan‑Netzwerk schubst das Substrat näher an die eine oder andere Stelle, vereinfacht das Produktgemisch oder reduziert das Verhalten von OkaE sogar auf eine einzige Hauptreaktion.
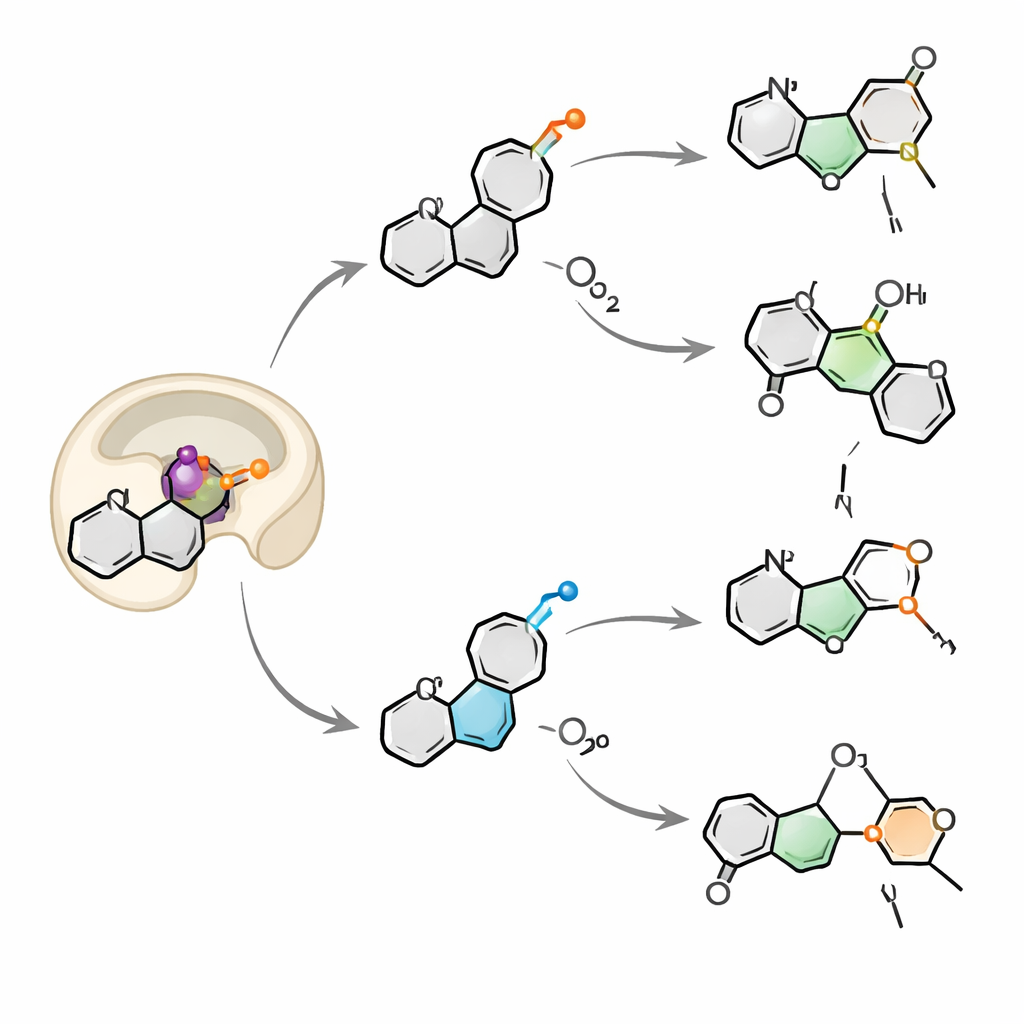
Zwei Sauerstoffe auf einmal einatmen
Durch Verfolgung mit dem schwereren Isotop 18O markierter Sauerstoffatome entdeckte das Team, dass OkaE Sauerstoff sowohl aus dem molekularen Sauerstoff der Luft als auch aus dem Wasser der Lösung bezieht. Bei den meisten Produkten kann der am Eisen gebundene Sauerstoff mit Wasser austauschen, bevor er ins Molekül eingebaut wird, was die gemischten Markierungsprofile erklärt. Ein Produkt, Neuokaramin IV, stach hervor: Sein Muster ließ sich nur dadurch erklären, dass ein zweites Sauerstoffmolekül erfasst und innerhalb eines einzelnen katalytischen Zyklus in dasselbe Substrat eingebaut wird, wobei eine empfindliche Peroxidbrücke gebildet und wieder gespalten wird. Dieser „Zweifach‑Atem“‑Mechanismus ist für diese Enzymfamilie extrem selten und unterstreicht, wie flexibel OkaE radikalische und positiv geladene Zwischenstufen im selben aktiven Zentrum koordinieren kann.
Was das für zukünftiges Design bedeutet
Einfach gesagt ist OkaE ein molekulares Multifunktionswerkzeug. Es kann nicht nur einen schwierig herzustellenden Ring montieren, den Chemiker sonst nur mit Mühe bauen, sondern diesen Ring und seine Umgebung auch in mehrere unterschiedliche Gerüste umformen – und das alles mit Luft, Eisen und einer einfachen zellulären Säure als Antrieb. Indem diese Arbeit zeigt, wie ein spezifisches Interaktionsnetzwerk im Protein sein Substrat positioniert und wie eine schwenkende Eisen‑Sauerstoff‑Einheit verschiedene Reaktionskanäle öffnet, liefert sie eine Blaupause für das Engineering „programmierbarer“ Biokatalysatoren. Solche maßgeschneiderten Enzyme könnten die späte Modifikation natürlicher Produkte effizienter machen und Chemikern helfen, bessere Medikamente und Insektizide mit weniger Abfall und höherer Präzision zu entwickeln.
Zitation: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Schlüsselwörter: Azetidin‑Biosynthese, nicht‑häme‑Eisen‑Enzym, okaramin‑Insektizide, Biokatalysator‑Engineering, oxidative Kaskadenreaktionen