Clear Sky Science · ru
Структурные и механистические сведения о связанной с азетидином αKG‑NHFe ферменте OkaE с многофункциональным каталитом
Почему небольшой фермент важен для будущих лекарств и пестицидов
Многие мощные лекарства и инсектициды основаны на сложных циклических молекулах, которые химикам трудно синтезировать. В этом исследовании показано, как один грибный фермент, называемый OkaE, способен сформировать одну из таких колец — необычно напряжённый четырёхчленный азетидин — а затем дополнительно перестраивать молекулу несколькими разными способами. Понимание работы OkaE может подсказать более экологичные пути к созданию новых лекарств и высокоселективных средств борьбы с вредителями, не затрагивающих людей и других позвоночных.
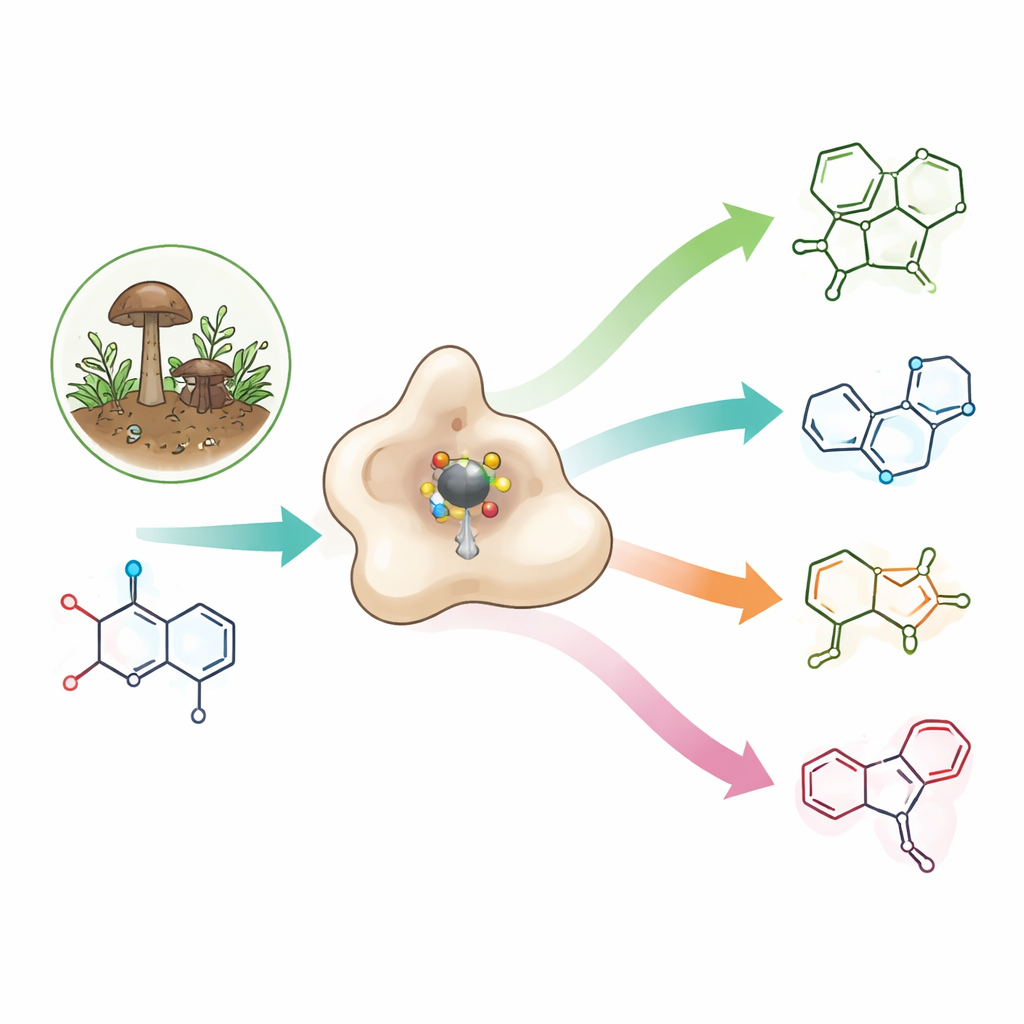
Редкий строительный блок с большим фармацевтическим потенциалом
Аzetидины — это крошечные четырёхчленные азотсодержащие кольца, в которые сосредоточено много напряжения. Это напряжение часто даёт полезные свойства: азетидины могут улучшать сопряжение лекарственной молекулы с её мишенью, её распределение в организме и растворимость в воде. Они уже встречаются в экспериментальных антибиотиках, противораковых средствах и потенциальных препаратах против болезни Альцгеймера, а также в окариминах — природных инсектицидах, вырабатываемых некоторыми грибами и избирательно блокирующих ионные каналы беспозвоночных, не затрагивая человеческие каналы. Однако из‑за большой напряжённости и нестабильности азетидиновых колец химикам обычно требуются несколько энергозатратных шагов и жёсткие условия для их синтеза.
Необычное решение природы: фермент OkaE
Грибы решают эту задачу с помощью специализированных ферментов. Большинство известных ферментов, формирующих азетидин, соединяют углерод и азот с участием распространённого клеточного кофактора SAM. OkaE нарушает это правило. Он относится к большой семье железозависимых ферментов, которые обычно вставляют кислород в молекулы. OkaE использует железо и вспомогательную молекулу α‑кетоглутарат для образования высокореактивного железо–кислородного комплекса, способного отрывать атомы водорода от субстрата, окаримина A. В отличие от своих родичей, OkaE формирует азетидиновое кольцо путем создания новой углеродно‑углеродной связи внутри уже сложного природного продукта, что делает его аутсайдером даже в очень универсальной семейства ферментов.
Один фермент — множество химических приёмов
Когда исследователи изучали очищенный OkaE в пробирке, они ожидали лишь образование азетидина и простую окислительную реакцию. Вместо этого они обнаружили мини‑химическую фабрику. Начиная с окаримина A, OkaE дал по крайней мере четыре новых молекулы, названные неоукарамины I–IV, в дополнение к уже известным промежуточным соединениям. Эти продукты показали, что OkaE способен проводить каскад трансформаций: формирование азетидинового кольца, присоединение гидроксильных групп, превращение спирта в карбоновую кислоту, размыкание связей в исходном каркасе и даже установку дополнительного трёхчленного кислородного кольца (эпоксида). Изменяя количество своего ко‑субстрата α‑кетоглутарата и подавая OkaE разные промежуточные соединения, команда проследила, как эти реакции ветвятся от одной начальной молекулы в пределах одного или нескольких каталитических циклов фермента.
Как форма и движение направляют реакции
Чтобы понять, как OkaE выбирает между этими возможностями, авторы решили кристаллические структуры фермента с высокой разрешающей способностью, связанного с металлом, вспомогательной молекулой и окаримином A, и сопоставили их с квантово‑механическими компьютерными моделями. OkaE имеет классическую «желеобразную» (jelly‑roll) складку своей семейства, но его активный сайт украшен серосодержащими остатками метионина и триптофаном, которые охватывают один конец окаримина через тонкие «Met–π» взаимодействия между атомами серы и ароматическими кольцами. Эта сеть удерживает субстрат так, что две определённые позиции — одна на атоме углерода рядом с азетидиновым кольцом и одна на близлежащей гидроксильной группе — обращены к реактивному железо–кислородному центру. Моделирование показывает, что после активации кислорода железо–кислородный фрагмент поворачивается в положение, где он может абстрагировать водород с любой из этих позиций, создавая вилку в реакционном пути. Изменение отдельных остатков в сети метионин–триптофан немного сдвигает субстрат к одной или другой позиции, упрощая смесь продуктов или даже сводя поведение OkaE к одной преобладающей реакции.
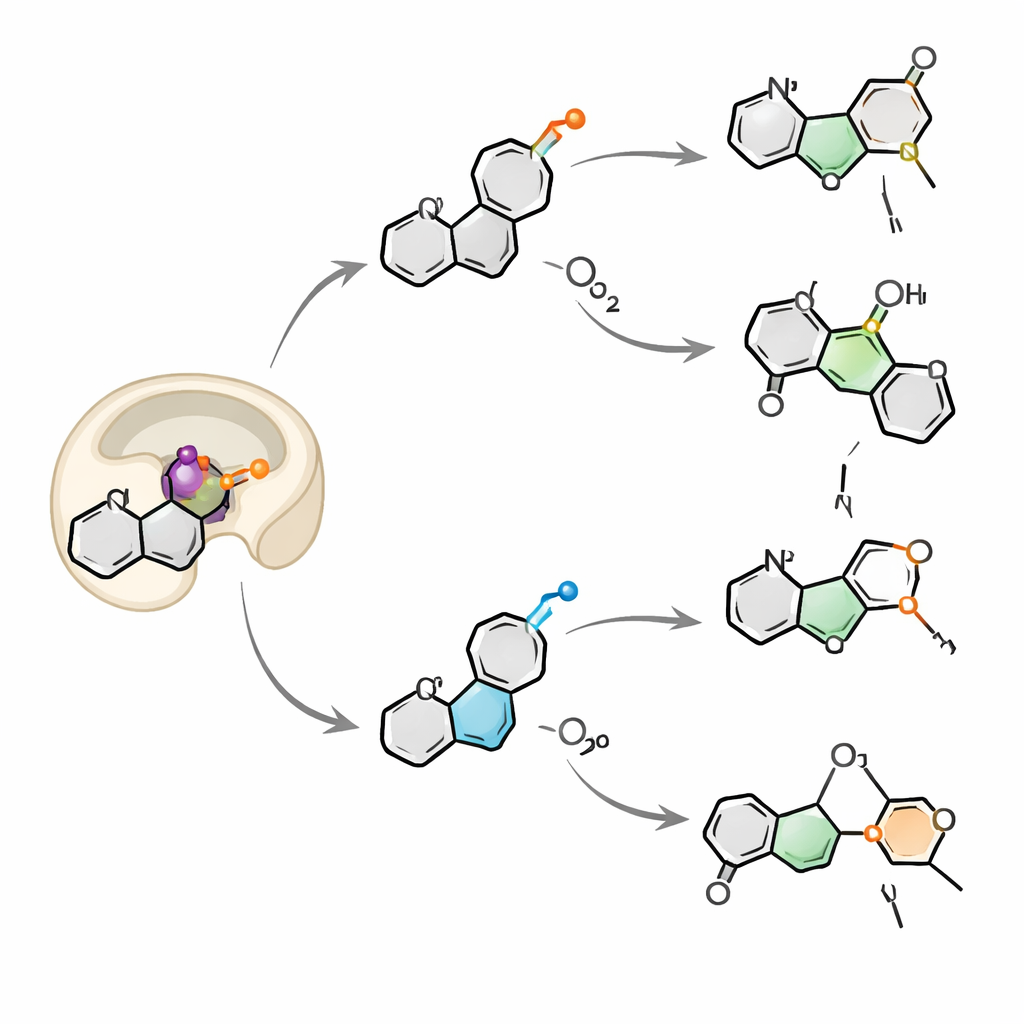
Вдыхая два кислорода одновременно
Прослеживая кислородные атомы, меченные более тяжёлым изотопом 18O, команда установила, что OkaE черпает кислород как из молекулярного кислорода воздуха, так и из растворённой воды. Для большинства продуктов кислород, связанный с железом, может обмениваться с водой до того, как попасть в молекулу, объясняя смешанные схемы метки. Один продукт, неоукарамин IV, выделялся: его распределение меток можно объяснить только в случае, если в пределах одного каталитического цикла в субстрат захватывается и включается в состав вторая молекула кислорода, образуя затем разрывающийся деликатный пероксидный мост. Этот «двойной вдох» крайне редок для этой семейства ферментов и подчёркивает, насколько гибко OkaE может координировать радикальные и положительно заряженные промежуточные состояния в одном активном сайте.
Что это значит для будущего проектирования
Проще говоря, OkaE — это молекулярный многоинструмент. Он не только способен собрать трудное для химиков кольцо, но и перестроить это кольцо и его окружение в несколько различных каркасов — при этом работая на воздухе, железе и простой клеточной кислоте. Раскрывая, как конкретная сеть взаимодействий в белке позиционирует субстрат и как вращающийся железо–кислородный фрагмент открывает разные реакционные каналы, эта работа даёт чертёж для инженерии «перенастраиваемых» биокатализаторов. Такие специализированные ферменты могут упростить поздние стадии модификации природных продуктов, помогая химикам создавать лучшие лекарства и инсектициды с меньшими отходами и большей точностью.
Цитирование: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Ключевые слова: биосинтез азетидина, безгемовый железосодержащий фермент, инсектициды окаримины, инженерия биокатализаторов, окислительные каскадные реакции