Clear Sky Science · nl
Structurele en mechanistische inzichten in azetidine-geassocieerde αKG-NHFe-enzym OkaE met multifunctionele katalyse
Waarom een klein enzym belangrijk is voor toekomstige medicijnen en pesticiden
Veel krachtige geneesmiddelen en insecticiden berusten op complexe ringvormige moleculen die moeilijk door chemici te bouwen zijn. Deze studie onthult hoe één schimmelenzym, OkaE genoemd, zo’n ring kan vormen — een ongewoon gespannen vierledige azetidine — en het molecuul vervolgens op verschillende manieren verder kan herschikken. Begrijpen hoe OkaE werkt kan leiden tot milieuvriendelijkere routes naar nieuwe medicijnen en zeer selectieve insectenbestrijdingsmiddelen die mensen en andere gewervelden sparen.
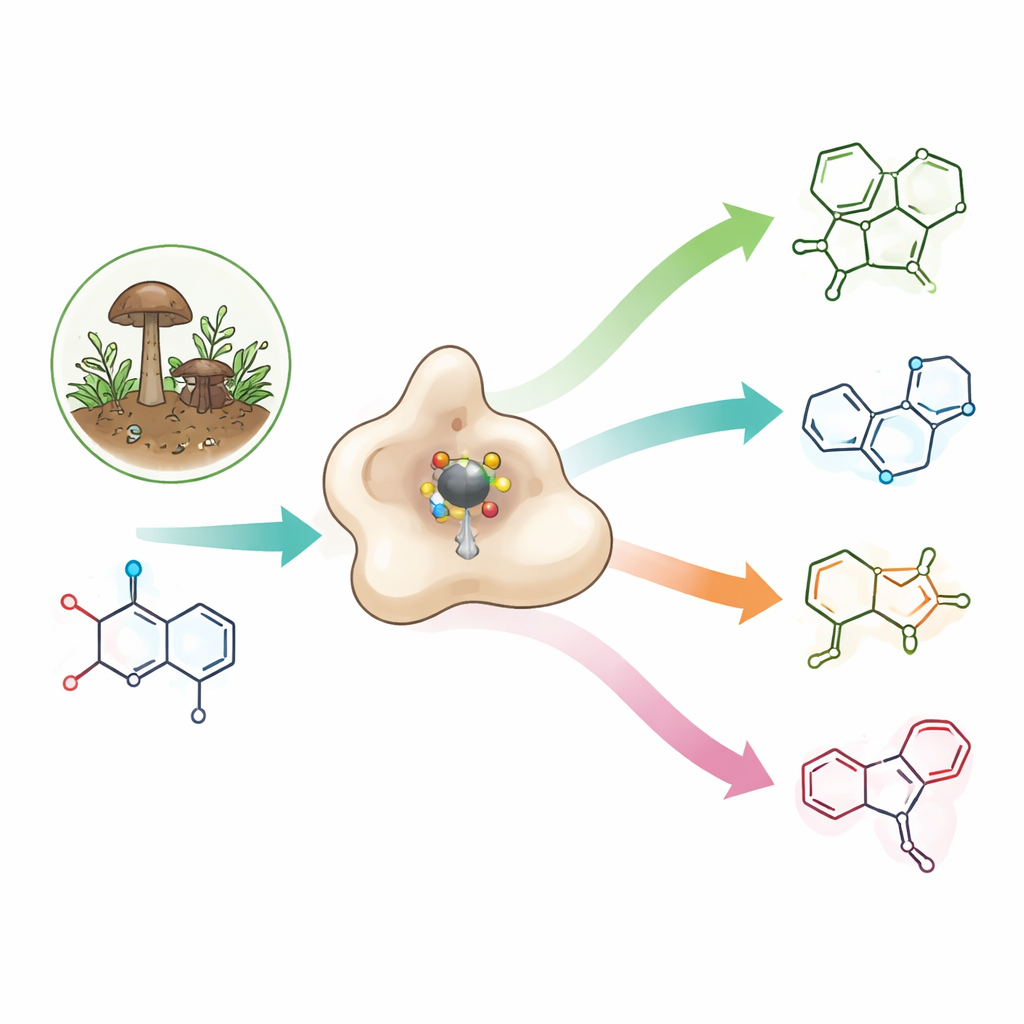
Een zeldzame bouwsteen met groot farmaceutisch potentieel
Azetidines zijn kleine vierledige stikstofringen die veel spanningsenergie in een kleine ruimte opslaan. Die spanning vertaalt zich vaak in nuttige eigenschappen: azetidines kunnen verbeteren hoe geneesmiddelen in hun doelen passen, hoe ze zich door het lichaam verplaatsen en hoe goed ze in water oplossen. Ze komen al voor in experimentele antibiotica, kankerremmers en potentiële middelen tegen Alzheimer, evenals in okaramines — natuurlijke insecticiden die door bepaalde schimmels worden gemaakt en die selectief zenuwkanalen bij ongewervelden uitschakelen terwijl ze menselijkekanalen ongemoeid laten. Omdat azetidine-ringen echter zo gespannen en onstabiel zijn, hebben chemici doorgaans meerdere energie-intensieve stappen en ruwe omstandigheden nodig om ze te synthetiseren.
Natuur’s ongebruikelijke oplossing: het enzym OkaE
Schimmels tackelen deze uitdaging met gespecialiseerde enzymen. De meeste bekende azetidine-vormende enzymen verbinden een koolstofatoom met een stikstofatoom met behulp van een veelvoorkomende cellulaire cofactor genaamd SAM. OkaE doorbreekt die regel. Het behoort tot een grote familie van ijzerafhankelijke enzymen die normaal gesproken zuurstofatomen in moleculen invoegen. OkaE gebruikt ijzer en een hulpstof, alfa‑ketoglutaraat, om een zeer reactieve ijzer–zuurstofsoort te vormen die waterstofatomen uit zijn substraat, okaramine A, kan abstraheren. In tegenstelling tot zijn verwanten smeedt OkaE de azetidine-ring door een nieuwe koolstof–koolstofbinding te vormen binnen dit reeds complexe natuurlijke product, waarmee het opvalt zelfs binnen een zeer veelzijdige enzymfamilie.
Één enzym, veel chemische trucs
Toen de onderzoekers gezuiverd OkaE in het reageerbuisje bestudeerden, verwachtten ze alleen azetidinevorming en een eenvoudige oxidatie. In plaats daarvan vonden ze een kleine chemische fabriek. Beginnend met okaramine A produceerde OkaE ten minste vier nieuwe moleculen, genoemd neuokaramines I–IV, naast bekende tussenproducten. Deze producten toonden aan dat OkaE een cascade aan transformaties kan uitvoeren: de azetidine-ring vormen, hydroxylgroepen toevoegen, een alcohol omzetten in een carboxylzuur, bindingen in het oorspronkelijke raamwerk openen en zelfs een extra kleine drieledige zuurstofring (een epoxide) installeren. Door de hoeveelheid van zijn co‑substratum, alfa‑ketoglutaraat, te variëren en OkaE verschillende tussenproducten voor te zetten, bracht het team in kaart hoe deze reacties vertakken vanuit één beginnende molecule binnen één of enkele enzymcycli.
Hoe vorm en beweging de reacties sturen
Om te zien hoe OkaE tussen deze mogelijkheden kiest, losten de auteurs hoogresolutie-kristalstructuren op van het enzym gebonden aan metaal, de hulpstof en okaramine A, en combineerden die met kwantumniveau computersimulaties. OkaE heeft de klassieke “jelly‑roll” vouwing van zijn enzymfamilie, maar zijn actieve plaats is versierd met zwavelhoudende methionineresiduen en een tryptofaan die één einde van okaramine via subtiele “Met–π”-interacties tussen zwavelatomen en aromatische ringen omsluiten. Dit netwerk houdt het substraat zodanig vast dat twee specifieke posities — één op een koolstof naast de azetidine-ring en één op een nabijgelegen hydroxylgroep — naar het reactieve ijzer–zuurstofcentrum gericht zijn. Simulaties laten zien dat, na zuurstofactivatie, het ijzer–zuurstoffragment wegdraait naar een oriëntatie waarin het een waterstof van beide sites kan abstraheren, waardoor een vertakking in het reactiepaden ontstaat. Veranderen van enkele residuen in het methionine–tryptofaan‑netwerk duwt het substraat dichter naar de ene of de andere plaats, waardoor het productmengsel eenvoudiger wordt of OkaE’s gedrag zelfs terugvalt tot één voornaamste reactie.
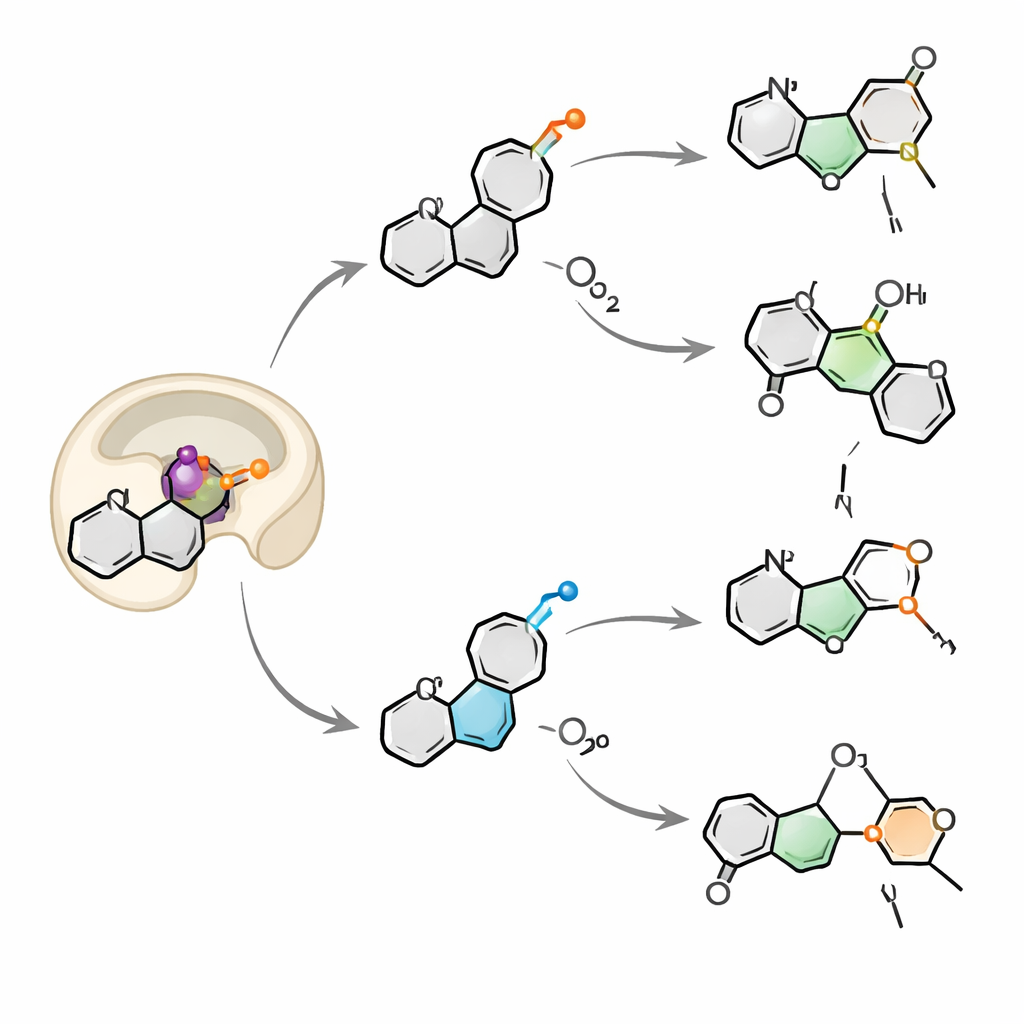
Tegelijkertijd twee zuurstofatomen inademen
Door zuurstofatomen te volgen die gelabeld waren met het zwaardere isotoop 18O, ontdekten de onderzoekers dat OkaE zuurstof zowel uit moleculaire zuurstof in de lucht als uit water in oplossing haalt. Voor de meeste producten kan de aan het ijzer gebonden zuurstof met water uitwisselen voordat het in het molecuul terechtkomt, wat de gemengde labelpatronen verklaart. Één product, neuokaramine IV, stak eruit: het labelpatroon kon alleen worden verklaard als een tweede zuurstofmolecuul wordt gevangen en in hetzelfde substraat wordt ingebouwd binnen één enkele katalytische cyclus, waarbij een fragiele peroxidebrug wordt gevormd en daarna verbroken. Dit “twee‑adem”-mechanisme is uiterst zeldzaam voor deze enzymfamilie en benadrukt hoe flexibel OkaE radicale en positief geladen tussenproducten binnen dezelfde actieve plaats kan orkestreren.
Wat dit betekent voor toekomstig ontwerp
Simpel gezegd is OkaE een moleculair multigereedschap. Het kan niet alleen een moeilijke ring assembleren die chemici moeilijk kunnen maken, maar die ring en zijn omgeving ook omvormen tot verschillende afzonderlijke bouwstenen — en dat alles draaiend op lucht, ijzer en een eenvoudig cellulair zuur. Door te laten zien hoe een specifiek interactienetwerk in het eiwit zijn substraat positioneert en hoe een wegdraaiend ijzer–zuurstof‑unit verschillende reactiekanaaltjes opent, levert dit werk een blauwdruk voor het ontwerpen van “programmeerrbare” biokatalysatoren. Dergelijke op maat gemaakte enzymen zouden de laat‑fase modificatie van natuurlijke producten kunnen stroomlijnen en chemici helpen betere geneesmiddelen en insecticiden te bouwen met minder afval en grotere precisie.
Bronvermelding: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Trefwoorden: azetidine-biosynthese, niet-heemijzerenzym, okaramine-insecticiden, biokatalysator-engineering, oxidatieve cascade-reacties