Clear Sky Science · es
Perspectivas estructurales y mecanísticas sobre la enzima αKG‑NHFe OkaE asociada a azetidina con catálisis multifuncional
Por qué una enzima diminuta importa para futuros fármacos e insecticidas
Muchos medicamentos e insecticidas potentes dependen de moléculas complejas en forma de anillo que son difíciles de construir para los químicos. Este estudio descubre cómo una única enzima fúngica, llamada OkaE, puede esculpir uno de esos anillos—una azetidina de cuatro miembros inusualmente tensa—y luego remodelar la molécula de varias maneras distintas. Entender cómo funciona OkaE podría inspirar vías más verdes hacia nuevos medicamentos y agentes de control de insectos altamente selectivos que preserven a los humanos y otros vertebrados.
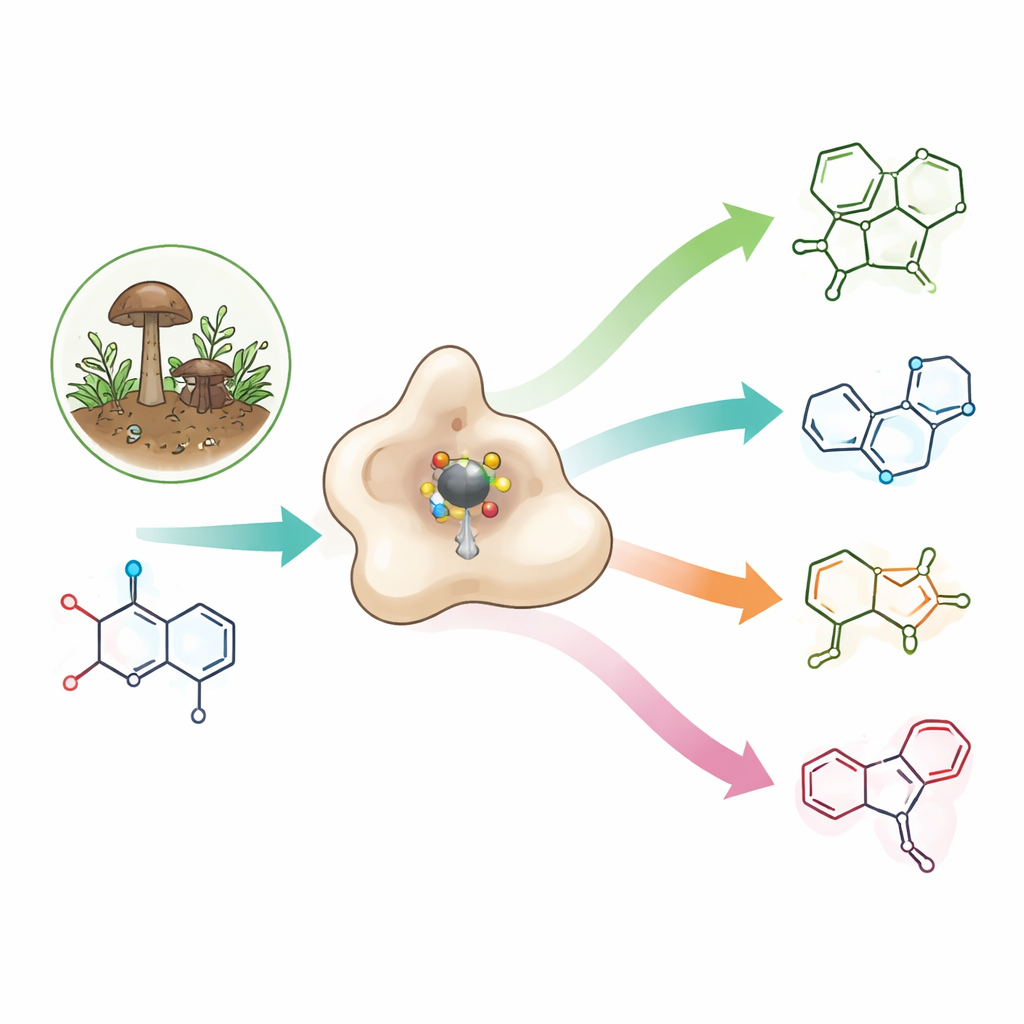
Un bloque de construcción raro con gran promesa farmacéutica
Las azetidinas son pequeños anillos de nitrógeno de cuatro miembros que concentran mucha tensión en un espacio reducido. Esa tensión suele traducirse en propiedades útiles: las azetidinas pueden mejorar cómo encajan las moléculas fármaco con sus dianas, cómo se distribuyen en el organismo y su solubilidad en agua. Ya aparecen en antibióticos experimentales, agentes anticancerosos y posibles fármacos contra el Alzheimer, así como en las okaraminas—insecticidas naturales producidos por ciertos hongos que inactivan selectivamente canales nerviosos en invertebrados sin afectar a los canales humanos. Sin embargo, dado que los anillos de azetidina son tan tensos e inestables, los químicos suelen necesitar varios pasos consumidores de energía y condiciones rigurosas para sintetizarlos.
La solución inusual de la naturaleza: la enzima OkaE
Los hongos abordan este desafío con enzimas especializadas. La mayoría de las enzimas conocidas que forman azetidinas enlazan un átomo de carbono con uno de nitrógeno usando un cofactor celular común llamado SAM. OkaE rompe esa regla. Pertenece a una gran familia de enzimas dependientes de hierro que normalmente insertan átomos de oxígeno en las moléculas. OkaE usa hierro y una molécula ayudante, el alfa‑cetoglutarato, para formar una especie hierro‑oxígeno altamente reactiva capaz de arrancar átomos de hidrógeno de su sustrato, la okaramina A. A diferencia de sus parientes, OkaE forma el anillo de azetidina creando un nuevo enlace carbono‑carbono dentro de este producto natural ya complejo, lo que la convierte en una excepción incluso dentro de una familia en extremo versátil.
Una enzima, muchos trucos químicos
Cuando los investigadores estudiaron OkaE purificada en el tubo de ensayo, esperaban solo la formación de la azetidina y una oxidación simple. En cambio, encontraron una pequeña fábrica química. Partiendo de la okaramina A, OkaE produjo al menos cuatro moléculas nuevas, denominadas neuokaraminas I–IV, además de intermediarios ya conocidos. Estos productos mostraron que OkaE puede llevar a cabo una cascada de transformaciones: formar el anillo de azetidina, añadir grupos hidroxilo, convertir un alcohol en un ácido carboxílico, abrir enlaces en el andamiaje original e incluso instalar un anillo oxirano adicional de tres miembros (un epóxido). Al variar la cantidad de su co‑sustrato, el alfa‑cetoglutarato, y alimentar a OkaE con distintos intermediarios, el equipo trazó cómo estas reacciones se bifurcan a partir de una única molécula inicial dentro de uno o pocos ciclos enzimáticos.
Cómo la forma y el movimiento dirigen las reacciones
Para ver cómo OkaE selecciona entre estas posibilidades, los autores resolvieron estructuras cristalinas de alta resolución de la enzima unida al metal, al ayudante y a la okaramina A, y las combinaron con simulaciones computacionales a nivel cuántico. OkaE presenta el plegamiento clásico tipo “jelly‑roll” de su familia enzimática, pero su sitio activo está decorado con residuos de metionina que contienen azufre y con un triptófano que acunan un extremo de la okaramina mediante sutiles interacciones “Met–π” entre átomos de azufre y anillos aromáticos. Esta red mantiene el sustrato de modo que dos posiciones específicas—una en un carbono adyacente al anillo de azetidina y otra en un grupo hidroxilo cercano—quedan orientadas hacia el centro reactivo hierro‑oxígeno. Las simulaciones muestran que, tras la activación del oxígeno, el fragmento hierro‑oxígeno gira hasta adoptar una orientación en la que puede abstraer un hidrógeno de cualquiera de los dos sitios, creando una bifurcación en la vía reactiva. Alterar residuos individuales en la red metionina–triptófano empuja el sustrato hacia un sitio u otro, simplificando la mezcla de productos o incluso colapsando el comportamiento de OkaE hacia una única reacción principal.
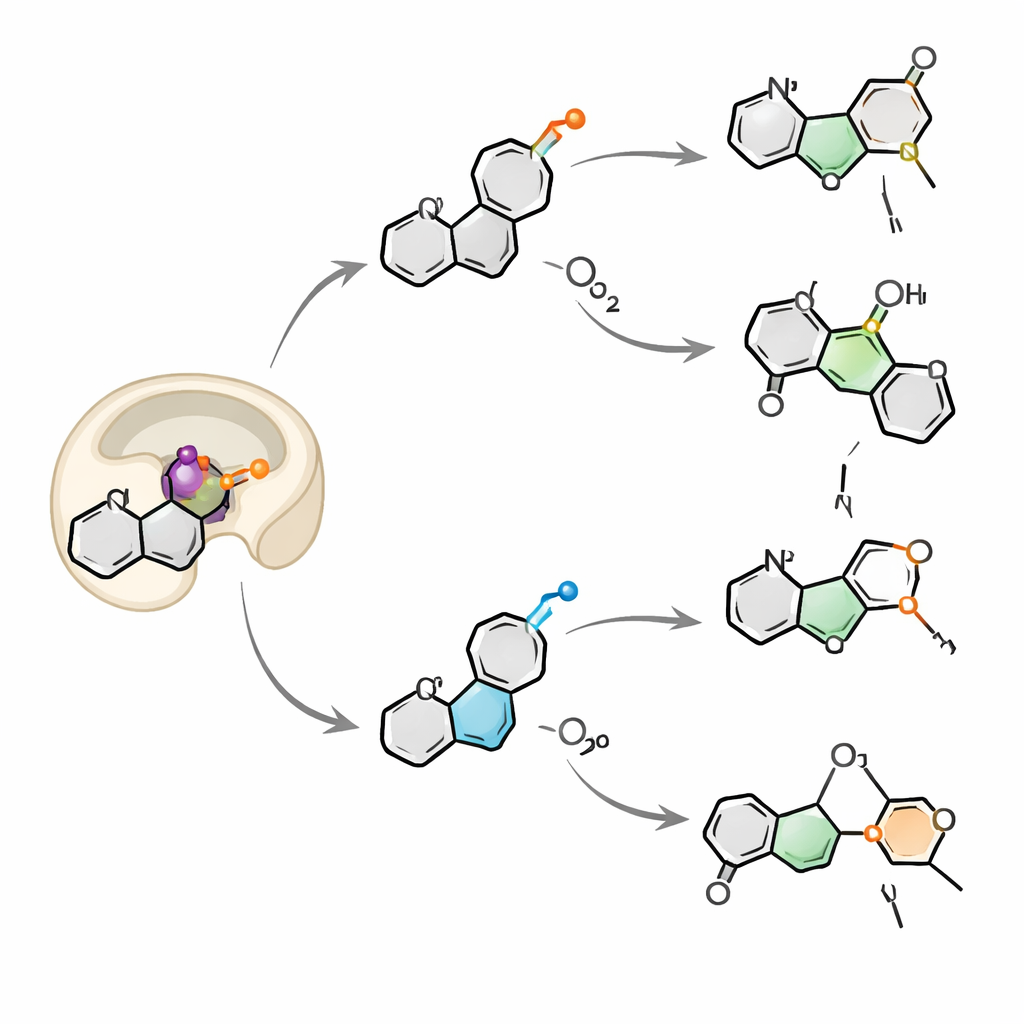
Respirando dos oxígenos a la vez
Al trazar átomos de oxígeno marcados con el isótopo más pesado 18O, el equipo descubrió que OkaE incorpora oxígeno tanto del oxígeno molecular del aire como del agua en solución. Para la mayoría de los productos, el oxígeno unido al hierro puede intercambiarse con el agua antes de quedar incorporado en la molécula, lo que explica los patrones de marcado mixtos. Un producto, la neuokaramina IV, destacó: su patrón solo podía explicarse si una segunda molécula de oxígeno es capturada e incorporada en el mismo sustrato dentro de un único ciclo catalítico, formando y luego rompiendo un delicado puente peróxido. Este mecanismo de “dos respiraciones” es extremadamente raro en esta familia enzimática y subraya la flexibilidad con la que OkaE puede coreografiar intermediarios radicalarios y con carga positiva dentro del mismo sitio activo.
Qué significa esto para el diseño futuro
En términos sencillos, OkaE es una multiherramienta molecular. No solo puede ensamblar un anillo difícil que los químicos luchan por sintetizar, sino también readaptar ese anillo y su entorno en varios andamiajes distintos—todo ello funcionando con aire, hierro y un simple ácido celular. Al revelar cómo una red de interacciones específica en la proteína posiciona su sustrato y cómo una unidad hierro‑oxígeno pivotante abre diferentes canales reactivos, este trabajo ofrece un plano para la ingeniería de biocatalizadores “programables”. Enzimas diseñadas así podrían simplificar la modificación en etapas tardías de productos naturales, ayudando a los químicos a construir mejores fármacos e insecticidas con menos residuos y mayor precisión.
Cita: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
Palabras clave: biosíntesis de azetidina, enzima de hierro no hemo, insecticidas okaramina, ingeniería de biocatalizadores, reacciones en cascada oxidativas