Clear Sky Science · ja
多機能触媒を持つアゼチジン関連αKG–NHFe酵素OkaEの構造的・機構的知見
なぜ小さな酵素が将来の医薬品や殺虫剤に重要なのか
多くの有効な薬や殺虫剤は、化学者が合成するのが難しい複雑な環状分子に依存しています。本研究は、単一の真菌性酵素OkaEが、ひとつの例外的にひずんだ四員環アゼチジンを形成し、その後さらに分子を複数の方法で改変できる仕組みを明らかにします。OkaEの働きを理解することで、より環境に優しい新薬や、ヒトや他の脊椎動物に害を与えにくい高選択的な殺虫剤の開発につながる可能性があります。
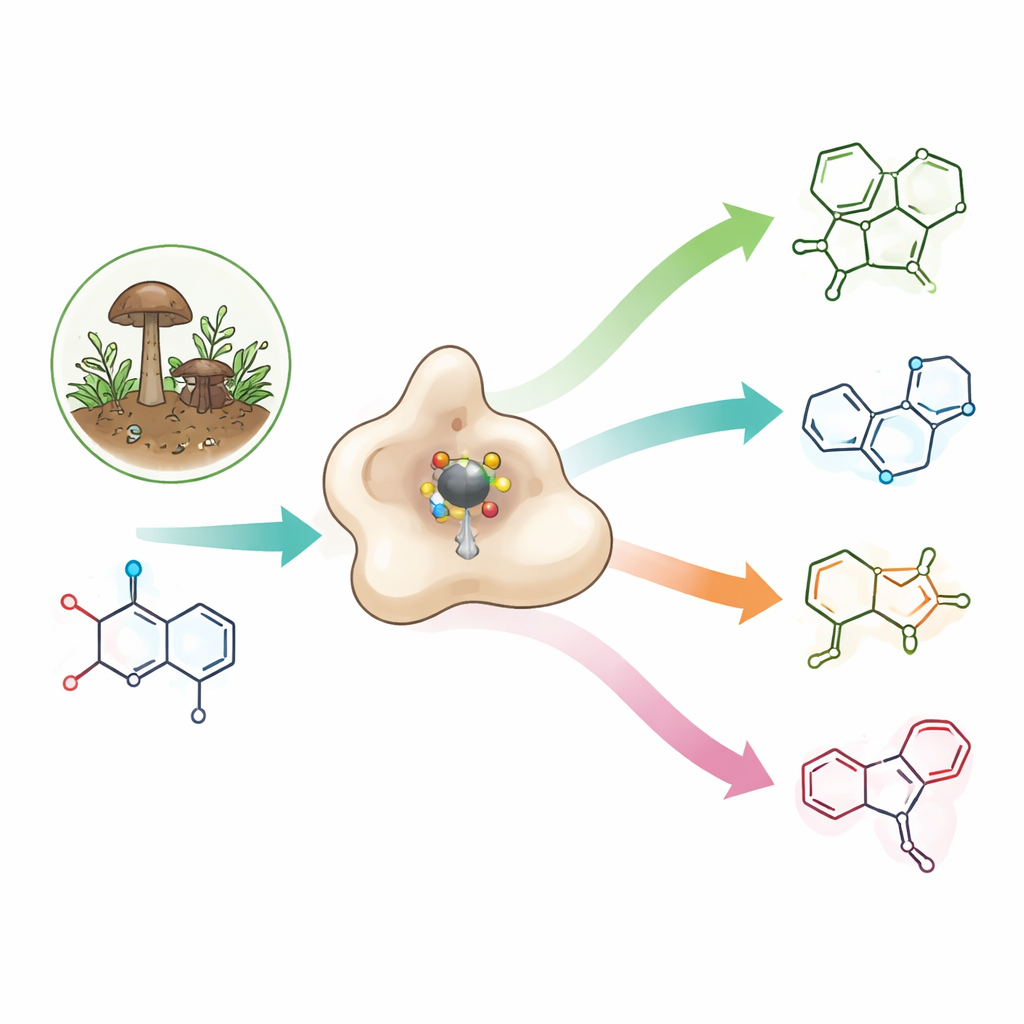
医薬的可能性が高い稀な構成要素
アゼチジンは窒素を含む小さな四員環で、多くのひずみエネルギーが詰まっています。このひずみはしばしば有用な性質につながり、アゼチジンは薬物分子が標的にフィットする様子、体内での移動、そして水への溶解性を改善することがあります。アゼチジンは実験的な抗生物質、抗がん剤、アルツハイマー病治療候補や、特定の真菌が合成する天然の殺虫剤オカラミンにも見られます。オカラミンは無脊椎動物の神経チャネルを選択的に無力化しつつヒトのチャネルを保護します。しかし、アゼチジン環は非常にひずんで不安定なため、化学合成では通常、複数のエネルギー集約的な段階と過酷な条件が必要です。
自然の異例な解決策:OkaE酵素
真菌はこの課題に対して特殊化した酵素で応えます。既知の多くのアゼチジン形成酵素は、SAMという一般的な補因子を用いて炭素と窒素を結びつけますが、OkaEはその常識を破ります。OkaEは通常分子に酸素を導入する大きなファミリーに属する鉄依存酵素です。OkaEは鉄と補助分子であるα-ケトグルタル酸を使って非常に反応性の高い鉄–酸素種を生成し、基質であるオカラミンAから水素原子を引き抜きます。類縁酵素とは異なり、OkaEはこの複雑な天然物の内部で新しい炭素–炭素結合を形成してアゼチジン環を作り出すため、この非常に多才な酵素ファミリーの中でも異例の存在です。
一つの酵素が示す多様な化学トリック
研究者たちが精製したOkaEを試験管内で調べたところ、彼らが予想していた単純なアゼチジン形成と酸化だけでなく、小さな化学工場のような挙動が見つかりました。オカラミンAから出発して、OkaEは既知の中間体に加えて少なくとも4種類の新規分子(neuokaramine I–IV)を生成しました。これらの生成物は、OkaEがアゼチジン環の形成、ヒドロキシル基の導入、アルコールのカルボン酸への変換、元の骨格の結合開裂、さらには追加の小さな三員環酸素(エポキシド)の導入といった一連の変換を行えることを示しています。補基であるα-ケトグルタル酸の量を変えたり、異なる中間体をOkaEに供給したりすることで、チームはこれらの反応がどのように単一の出発物質から分岐し、1回または数回の酵素サイクル内で進むかをマップしました。
形状と動きが反応を導く仕組み
OkaEがこうした選択をどう行うかを解き明かすために、著者らは金属、補助分子、オカラミンAを結合した酵素の高分解能結晶構造を解き、量子レベルの計算機シミュレーションと組み合わせました。OkaEはこの酵素ファミリーに共通する「ジェリーロール」フォールドを持ちますが、活性部位には硫黄を含むメチオニン残基とトリプトファンが配され、香香族環と硫黄間の微妙な“Met–π”相互作用でオカラミンの一端を抱え込んでいます。このネットワークは基質を保持し、アゼチジン環近傍のある炭素上の特定位置と、近接するヒドロキシル基上の別の位置の二つが反応性の鉄–酸素中心に面するように配置します。シミュレーションは、酸素活性化後に鉄–酸素断片が回転して、どちらかの位置から水素を抽出できる向きに入ることを示し、反応経路に分岐を生じさせます。メチオニン–トリプトファンのネットワーク中の単一残基を変えることで、基質が一方の位置により近づき、生成物混合物が単純化したり、OkaEの挙動が主に一つの反応に収束したりします。
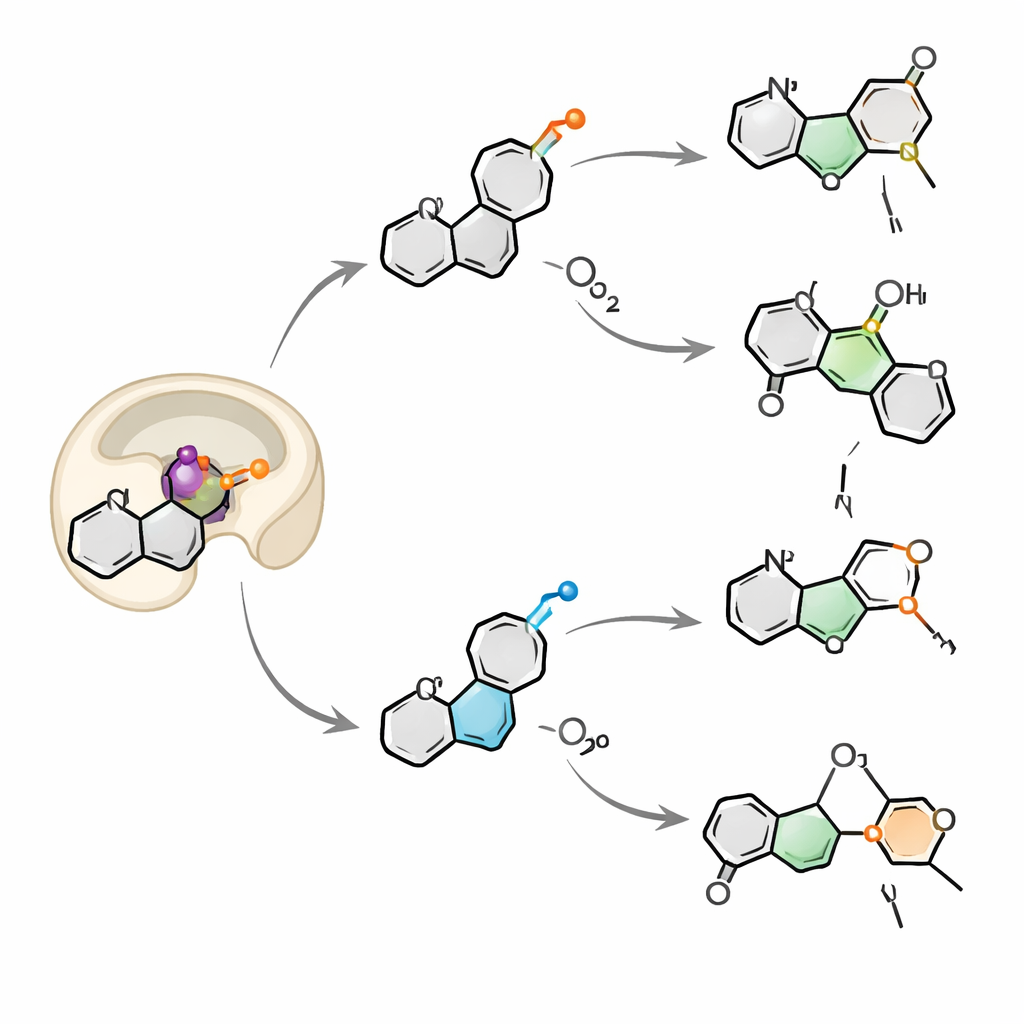
同時に二つの酸素を取り込む
重い酸素同位体18Oで標識した酸素原子を追跡することで、チームはOkaEが大気中の分子状酸素と溶液中の水の両方から酸素を取り込むことを発見しました。ほとんどの生成物では、鉄に結合した酸素が最終的に分子に取り込まれる前に水と交換できるため、混合した標識パターンが説明されます。ひとつの生成物であるneuokaramine IVは例外で、その標識パターンは、単一の触媒サイクル内で二つ目の酸素分子が捕捉されて同一基質に組み込まれ、繊細な過酸化物架橋が形成されては切断されることを仮定しなければ説明できませんでした。この「二回の呼吸」機構はこの酵素ファミリーでは極めて稀であり、OkaEが同一の活性部位内でラジカル中間体と正電荷を持つ中間体を柔軟に扱えることを示しています。
今後の設計への含意
平たく言えば、OkaEは分子のマルチツールです。化学者が合成に苦労する困難な環を組み立てられるだけでなく、その環や周辺を複数の異なる骨格へと作り変えることができ、すべて空気、鉄、そして単純な細胞内酸を使って進行します。タンパク質中の特定の相互作用ネットワークが基質をどのように位置決めし、回転する鉄–酸素ユニットがいかに異なる反応チャネルを開くかを明らかにすることにより、本研究は「プログラム可能な」バイオ触媒を設計するための青写真を提供します。こうした改変可能な酵素は、天然物の後期修飾を簡素化し、廃棄物を減らしつつ高精度でより良い医薬品や殺虫剤を作るのに役立つでしょう。
引用: Wang, X., Yu, J., Liu, T. et al. Structural and mechanistic insights into azetidine-associated αKG-NHFe enzyme OkaE with multifunctional catalysis. Nat Commun 17, 2861 (2026). https://doi.org/10.1038/s41467-026-69519-5
キーワード: アゼチジン生合成, 非ヘム鉄酵素, オカラミン系殺虫剤, バイオ触媒設計, 酸化カスケード反応