Clear Sky Science · sv
TPTE, ett testes-specifikt PTEN-familjemedlem, driver spermatogenes via PI(4,5)P2-syntes
Varför detta är viktigt för manlig fertilitet
Många par som har svårt att bli gravida får aldrig ett tydligt svar på varför spermier är få eller rör sig dåligt. Denna studie avslöjar ett tidigare mystiskt testes-specifikt enzym, kallat TPTE, som hjälper till både vid den genetiska omställningen av spermieförstadier och vid byggandet av deras pisklika svansar. Genom att visa hur TPTE formar viktiga signalmolekyler i utvecklande spermier pekar forskningen på nya molekylära förklaringar till vissa former av manlig infertilitet och antyder framtida vägar för diagnostik och behandling.
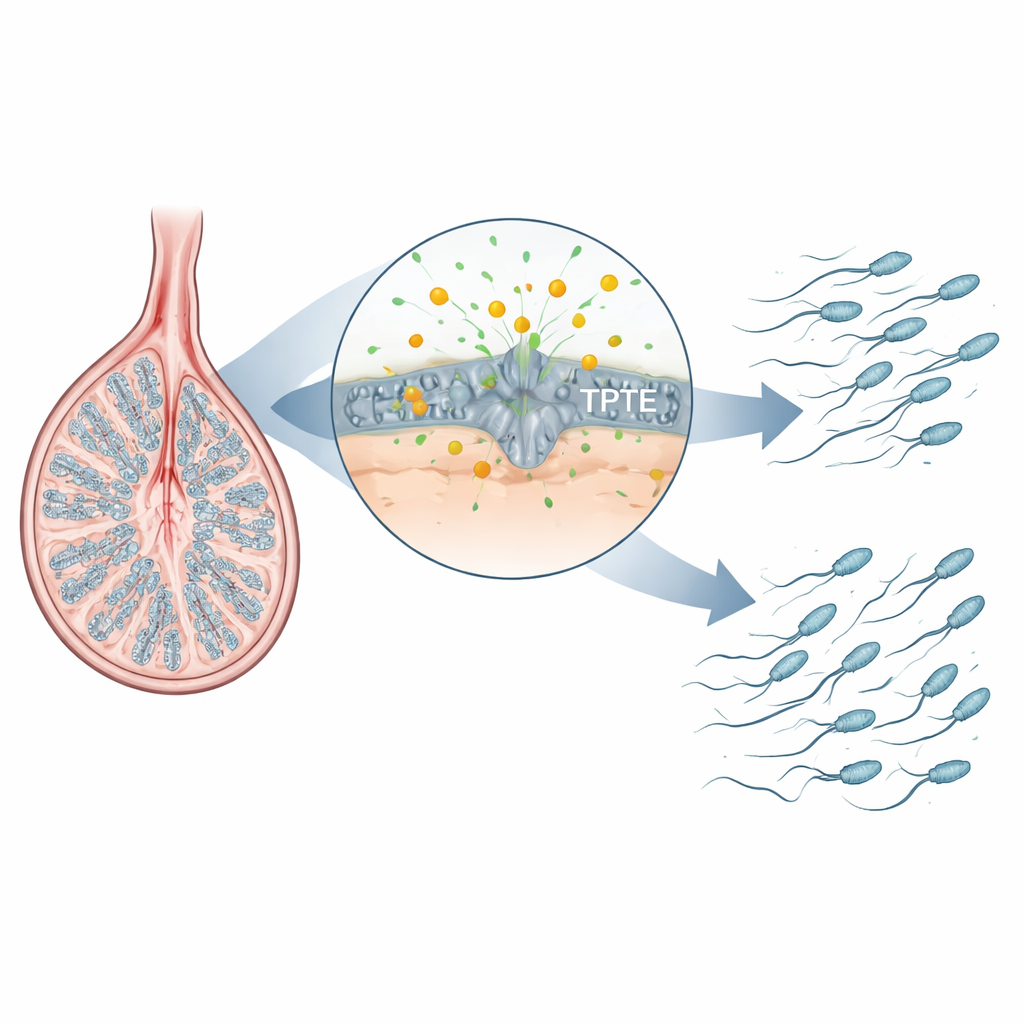
En dold hjälpare i spermutvecklingen
Spermier bildas i en noga koreograferad följd av steg i testikeln: stamceller delar sig, deras avkommor omarrangerar DNA under meiosen, och de rundade cellerna omformas till strömlinjeformade, svansförsedda spermier. Författarna fokuserade på en familj enzymer som bearbetar fettbaserade signalmolekyler i cellmembran. Ett välkänt medlem, PTEN, är viktig i många vävnader men är inte avgörande för de senare stadierna av spermatogenesen. TPTE däremot produceras nästan uteslutande i germinalceller i testikeln, och dess aktivitet var dåligt förstådd. Genom att kartlägga var en nyckelmembranlipid, PI(4,5)P2, förekommer i mus-testiklar fann forskarna att den är särskilt riklig i spermatocyter och spermatider — just de stadier där kromosomer repareras och svansar byggs — vilket antyder att TPTE och denna lipid kan vara avgörande för normal spermieutveckling.
Koppling mellan TPTE-förlust, dåliga spermier och mänsklig infertilitet
Teamet undersökte först om TPTE är förändrat hos män med svår infertilitet. Genom att omanalysiera offentliga RNA-sekvenseringsdata från testikelbiopsier fann de att TPTE-nivåerna är påtagligt reducerade hos patienter med icke-obstruktiv azoospermi och andra tillstånd märkta av skadade eller uttömda germinalceller. För att undersöka orsak och verkan raderade de Tpte-genen i möss med genombredigeringsmetoder. Hanmöss utan TPTE fick betydligt mindre kullar trots normal testikelstorlek. Deras bitestiklar innehöll färre spermier och datorassisterad analys visade nedsatt rörlighet och försämrad framåtriktad simning. Under mikroskopet hade många spermier normala, ovala huvuden men krusade eller vikta svansar, vilket tyder på att TPTE inte är nödvändigt för huvudbildning men är avgörande för att bevara spermieantalet och forma funktionella svansar.
Skydd av DNA-reparation under meios
För att förstå varför spermieantalet sjönk zoomade forskarna in på meiosen, där kromosomer utbyter segment genom noggrant kontrollerade DNA-brott och reparationer. I TPTE-bristande testiklar såg den övergripande fördelningen av germinalcellstadier liknande ut, men cellantal började falla i diplotena spermatocytstadiet och det uppstod en ökning av döende celler som fastnade i metafas I. Kromosomspreder visade defekter i den steglika strukturen som tillåter parade kromosomer att linjera upp, och en markör för DNA-brott, γ-H2AX, kvarstod onormalt länge på autosomer, vilket indikerar ofullständig reparation. Färre fokus av DNA-bindande hjälpare RPA2 och DMC1 bildades vid brottplatser. Molekylär analys pekade på överaktivering av en central tillväxtväg, AKT/mTOR, i frånvaro av TPTE, åtföljt av sänkta nivåer av RAD50, en kärnkomponent som initierar dubbelsträngsbrottsreparation. Tillsammans tyder dessa fynd på att TPTE normalt genererar PI(4,5)P2 för att hålla AKT/mTOR-aktiviteten i schack, bevara RAD50-nivåer och tillåta meiotisk DNA-reparation att fortgå, därigenom skydda tillgången på livskraftiga spermatider.
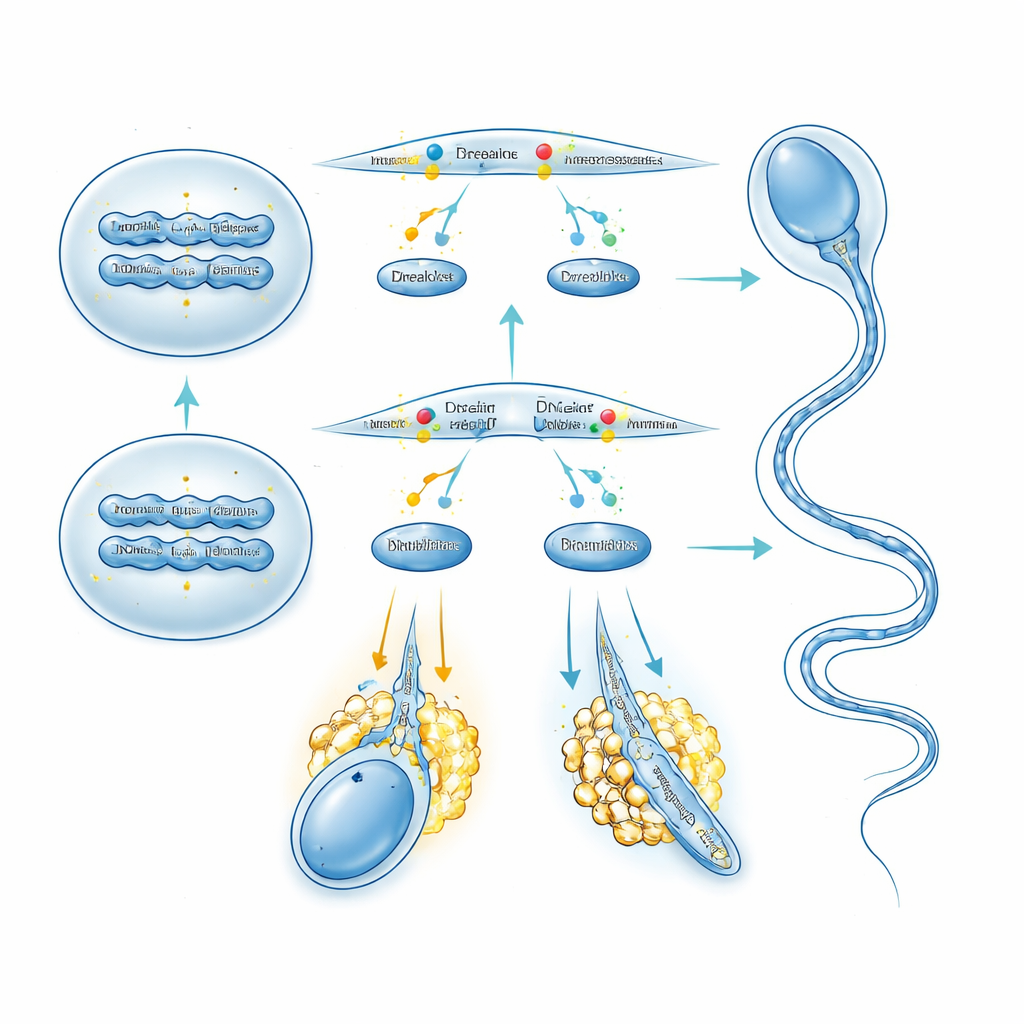
Bygga starka svansar genom kontrollerad proteinproduktion
TPTE visade sig också vara avgörande för det senare ombyggnadssteget när runda spermatider blir strömlinjeformade, rörliga spermier. Elektronmikroskopi av svansar från TPTE-fria spermier visade flera axonemala tvärsnitt inneslutna i en enda membrankanal och störda “9+2” mikrotubulusarrangemang, tillsammans med missbildade stödstrukturer. Färgning av svanskomponenter som acetylerat tubulin och det yttre täta fiberproteinet ODF2 visade fläckiga, försvagade strukturer, och fler förlängda spermatider genomgick celldöd i testikeln. Lipidfärgning visade att PI(4,5)P2 var markant reducerad och ojämnt fördelad längs flageller när TPTE saknades. För att se hur denna störning påverkade cellens proteinframställning utförde författarna kvantitativ proteomik på isolerade runda spermatider. Hundratals proteiner, inklusive flera ribosomala komponenter, var uppreglerade, och ribosomprofilering indikerade ökad polysomaktivitet, ett tecken på förhöjd translation. Bland dessa lyfte teamet fram PDLIM1, en känd broms för mikrotubulusorganisation: dess proteinnivåer ökade kraftigt utan förändring i dess budbärar-RNA, och dess transkript försköts in i tunga polysomfraktioner, vilket indikerar övertranslation. Detta mönster spårar åter till överdriven AKT/mTOR-signalering som triggas av den förändrade lipidbalansen när TPTE saknas.
Vad detta betyder för förståelsen av manlig infertilitet
Sammantaget skildrar studien TPTE som en germinalcellsvakt som stämmer av membranlipider för att dämpa AKT/mTOR-signalering, vilket möjliggör korrekt DNA-reparation och ordnad proteinsyntes. När TPTE saknas eller minskar, som observerats i flera typer av infertila mäns testiklar, löses inte DNA-brott under meios korrekt, vissa utvecklande spermier dör, och överlevarna framträder ofta med strukturellt defekta svansar som simmar dåligt. För icke-specialister är huvudbudskapet att manlig fertilitet inte bara beror på hormonhalter och spermieantal, utan också på subtila molekylära regulatorer som TPTE som samordnar genetisk integritet och svansarkitektur. I framtiden kan screening av TPTE och dess vägpartners hjälpa till att identifiera dolda orsaker till manlig infertilitet och inspirera riktade terapier som återställer balanserad signalering i testikeln.
Citering: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Nyckelord: manlig infertilitet, spermatogenes, spermierörlighet, signaltransduktion, testesspecifika gener