Clear Sky Science · ar
TPTE، عضو من عائلة PTEN الخاص بالخصية، يدفع تكوّن الحيوانات المنوية عبر تخليق PI(4,5)P2
لماذا يهم هذا للخصوبة الذكرية
العديد من الأزواج الذين يواجهون صعوبة في الإنجاب لا يحصلون على إجابة واضحة عن سبب قلة عدد الحيوانات المنوية أو حركتها الضعيفة. تكشف هذه الدراسة عن إنزيم خاص بالخصية كان غامضًا سابقًا، يُدعى TPTE، يساعد في توجيه إعادة ترتيب المادة الوراثية للخلايا المولدة للحيوانات المنوية وبناء أذيالها المُجدِفة. عبر إظهار كيف يشكّل TPTE جزيئات إشارية رئيسية داخل الخلايا المنوية النامية، تشير الدراسة إلى تفسيرات جزيئية جديدة لبعض أشكال العقم الذكوري وتقترح مسارات مستقبلية للتشخيص والعلاج.
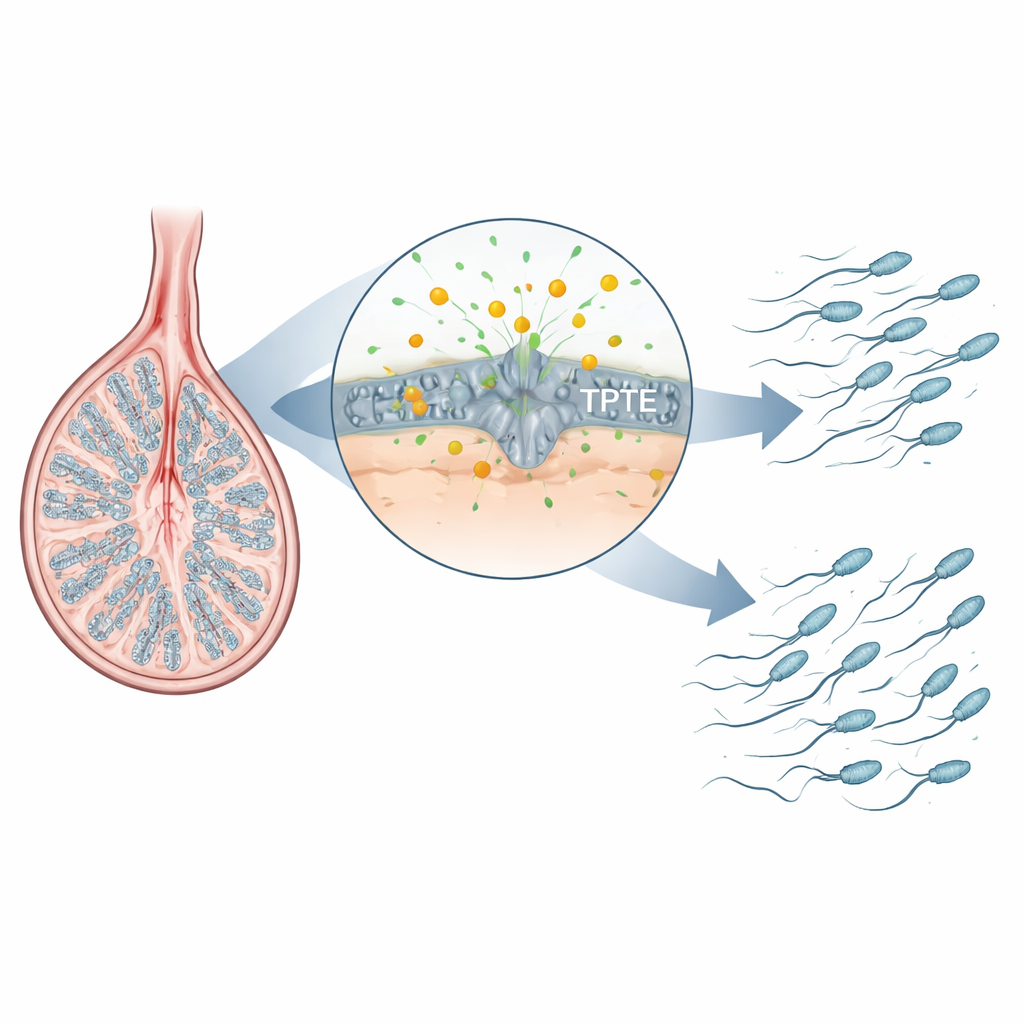
مساعد خفي في تكوّن الحيوانات المنوية
تُصنع الحيوانات المنوية في سلسلة محكمة من الخطوات داخل الخصية: تنقسم الخلايا الجذعية، ثم تُعيد سلالاتها ترتيب الحمض النووي خلال الانقسام الاختزالي، وتتحول الخلايا المستديرة الناتجة إلى حيوانات منوية انسيابية ذات ذيول. ركز المؤلفون على عائلة إنزيمات تعالج جزيئات دهنية إشارية في أغشية الخلايا. أحد الأعضاء المعروفين، PTEN، مهم في أنسجة عديدة لكنه ليس أساسيًا للمراحل المتأخرة من تكوّن الحيوانات المنوية. أما TPTE فيُنتَج تقريبًا حصريًا في الخلايا الجرثومية للخصية، وكانت وظيفته غير مفهومة جيدًا. عبر رسم خريطة لمكان تواجد الليبيد الغشائي الرئيسي PI(4,5)P2 في خصيتي الفأر، وجد الباحثون أنه يُركَّز بشكل خاص في الخلايا المنوية أثناء طور الريبوزومات وطور النطفيات—المراحل نفسها التي تُصلَح فيها الكروموسومات وتُبنى الأذيال—مشيرًا إلى أن TPTE وهذا الليبيد قد يكونان حاسِمين لتكوّن حيوانات منوية سليمة.
ربط فقدان TPTE بسوء جودة الحيوانات المنوية والعقم البشري
سأل الفريق أولاً ما إذا كان TPTE متغيرًا لدى رجال يعانون من عقم شديد. بإعادة تحليل بيانات تسلسل الرنا العامة لخزعات الخصية، وجدوا أن مستويات TPTE منخفضة بشكل ملحوظ لدى مرضى يعانون من انعدام النطاف غير الانسدادي وحالات أخرى تتسم بتلف أو نقص الخلايا الجرثومية. لاختبار السبب والنتيجة، حذفوا جين Tpte في الفئران باستخدام تعديل جيني. أنتج الذكور التي تفتقر إلى TPTE ذرية أصغر بكثير رغم حجم خصية طبيعي. احتوت البربخات على حيوانات منوية أقل، وأظهر التحليل الحاسوبي انخفاضًا في الحركة والسباحة التقدمية. تحت المجهر، كان لدى كثير من الحيوانات المنوية رؤوس طبيعية بيضاوية لكن أذيالًا ملتوية أو مطوية، مما يشير إلى أن TPTE غير ضروري لبناء الرأس لكنه حاسم للحفاظ على أعداد الحيوانات المنوية وتشكيل أذيال وظيفية.
حماية إصلاح الحمض النووي أثناء الانقسام الاختزالي
لفهم سبب انخفاض أعداد الحيوانات المنوية، ركز الباحثون على الانقسام الاختزالي، حيث تتبادل الكروموسومات مقاطع عبر كسور ومحاولات إصلاح محكومة بدقة. في خصى خالية من TPTE، بدا التوزيع العام لمراحل الخلايا الجرثومية مشابهًا، لكن أعداد الخلايا بدأت تنخفض في طور ال diplotene للسبيرموسيت، وظهر ارتفاع في الخلايا الميته الموقوفة عند الطور الانقسامي الأول. كشوفات الكروموسومات كشفت عن عيوب في البنية الشبيهة بالسلم التي تسمح بمحاذاة الكروموسومات المزدوجة، وبقيت علامة كسور الحمض النووي γ-H2AX على الصبغيات الجسدية بشكل غير طبيعي، مما يدل على إصلاح غير مكتمل. تشكلت بقع أقل من بروتينات مساعدة لالارتباط بالحمض النووي مثل RPA2 وDMC1 في مواقع الكسور. أشارت التحليلات الجزيئية إلى فرط تنشيط لمسار نمو مركزي، AKT/mTOR، في غياب TPTE، مصحوبًا بانخفاض مستويات RAD50، وهو مكوّن أساسي يبدأ إصلاح فسحات الشريط المزدوج. معًا، تقترح هذه النتائج أن TPTE عادة يُنتج PI(4,5)P2 لكبح نشاط AKT/mTOR، والحفاظ على مستويات RAD50 والسماح بإصلاح الحمض النووي الانقسالي، وبالتالي حماية مخزون السبيرماتيدات القابلة للحياة.
بناء أذيال قوية عبر ضبط إنتاج البروتين
كما ثبت أن TPTE حيوي لإعادة تشكيل السبيرماتيدات المستديرة لاحقًا إلى حيوانات منوية انسيابية متحركة. أظهر التصوير الإلكتروني لأذيال الحيوانات المنوية الخالية من TPTE مقاطع عرضية متعددة للمحور المركزي محبوسة داخل غشاء واحد وترتيبات ميكروتوبية “9+2” متعطلة، إلى جانب ألياف داعمة مشوهة. أظهر تلوين مكونات الذيل مثل التوبولين المؤكسد وبروتين الليف الكثيف الخارجي ODF2 هياكل مترهلة وضعيفة، ومات العديد من السبيرماتيدات المُطاولة أثناء وجودها في الخصية. أظهر صبغ الليبيدات أن PI(4,5)P2 كان منخفضًا وبمستوى غير منتظم على طول الأسواط عندما غاب TPTE. لرؤية كيف يؤثر هذا الاضطراب على آلات صنع البروتين في الخلية، أجرى المؤلفون تحليلات بروتينية كمية على السبيرماتيدات المستديرة المعزولة. ارتفعت مئات البروتينات، بما في ذلك عدة مكونات ريبوسومية، وأشارت دراسة الريبوسومات إلى نشاط بوليسومي معزز، وهو علامة على ترجمة متزايدة. من بين هذه البروتينات، أبرز الفريق PDLIM1، وهو مكبح معروف لتنظيم الميكروتوبيلات: ارتفعت مستويات بروتينه حدة دون تغيير في رنا المرسال الخاص به، وتحولت نسخه إلى كسور بوليسومية ثقيلة، مما يدل على ترجمة مفرطة. تعود هذه الصورة أيضًا إلى فرط إنذار AKT/mTOR الناجم عن اختلال توازن الليبيدات عند غياب TPTE.
ما الذي يعنيه هذا لفهم العقم الذكري
بشكل مجمل، تصور الدراسة TPTE كحارس في الخلايا الجرثومية يضبط الليبيدات الغشائية لكبح مسار AKT/mTOR، مما يمكّن إصلاح الحمض النووي المناسب وترجمة البروتين المنتظمة. عندما يختفي TPTE أو ينخفض مستواه، كما لوحظ في عدة أنواع من خصى بشرية عقيمة، لا تُحل كسور الحمض النووي أثناء الانقسام الاختزالي بشكل صحيح، وتموت بعض الخلايا المنوية النامية، وغالبًا ما يخرج الناجون ذوي أذيال معيبة تسبح بشكل سيء. للقراء غير المتخصصين، الرسالة الأساسية هي أن الخصوبة الذكرية تعتمد ليس فقط على مستويات الهرمونات وأعداد الحيوانات المنوية، بل أيضًا على منسِّقات جزيئية دقيقة مثل TPTE التي تُنسق سلامة الجينوم وبنية الذيل. في المستقبل، قد تساعد فحوصات TPTE وشركائه في المسار على تحديد أسباب خفية للعقم الذكري وإلهام علاجات موجهة تعيد توازن الإشارات في الخصية.
الاستشهاد: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
الكلمات المفتاحية: عقم ذكوري, تكوّن الحيوانات المنوية, حركة الحيوان المنوي, نقل الإشارات, جينات خاصة بالخصية